На данный момент одной из основных бед человечества является высокая смертность от онкологии. Ежегодно мир теряет около 8 миллионов людей, которым не удалось победить раковое заболевание. Ученые утверждают, что эти цифры в дальнейшем будут только расти и увеличатся практически в два раза к 2030 году. К счастью, в области лечения злокачественных новообразований появилось огромное количество препаратов, обладающих противоопухолевой активностью. Проведение лечения этими лекарствами называется химиотерапией. Подготовка к ней включает в себя медикаментозную поддержку организма и изменение образа жизни пациента. При соблюдении всех условий шансы побороть такое серьезное заболевание значительно увеличиваются.
Лекарственная помощь
Основная часть подготовки к химиотерапии заключается в применении определенных средств, которые помогут защитить здоровые органы от вредного воздействия препаратов, а также повысят выносливость организма и снизят проявление негативных последствий.
Каждому пациенту врач выписывает индивидуальный список лекарств и витаминов. Как правило, в него входят:
- Гепатопротекторы ("Фосфоглив", "Гептор" или "Гептрал").
- Пробиотики ("Хилак форте", "Аципол").
- Противорвотные препараты ("Навобан").
- Иммуномодулирующие препараты ("Виферон").
- От внутривенного введения некоторых лекарств у пациентов остаются следы на коже, которые успешно лечатся применением троксерутина. Поэтому лучше приобрести одну из таких мазей, на случай возникновения подобной ситуации.
- При подготовке к химиотерапии возможно введение различных внутривенных растворов ("Гемодез", "Реополиглюкин" и другие). Это поможет ускорить метаболизм организма.
- Не лишним будет применение комплекса аминокислот для защиты клеток печени, сердца и других органов.
- В последнее время врачи советуют пациентам употреблять соевый лецитин, который отлично питает клетки мозга и сосудов.
- Также в онкологии все чаще говорится о целебных свойствах экстракта грибов Рейши. Его составляющие помогают облегчить состояние пациента после лечения.

Изменение образа жизни пациента
Множество курсов химиотерапии - серьезное испытание, которое требует от человека кардинального изменения уклада жизни, отказа от вредных привычек и соблюдения ряда других правил здорового образа жизни.
- Пациенту желательно придерживаться сбалансированного рациона питания, богатого самыми разными минералами и витаминами. Особенно актуальна данная рекомендация для тех, кто задается вопросом, как подготовиться к химиотерапии при раке желудка или кишечника.
- Не рекомендуется применение тяжелой, жирной пищи, особенно накануне лечения. Это может усугубить возникновение тошноты и/или рвоты. На столе пациента должны регулярно находиться овощи, фрукты, зелень, кисломолочные продукты. Обязательно следует употреблять приготовленную на пару рыбу, отварное мясо. Из напитков особенно желательны ромашковый, имбирный, мятный чаи.
- Еще одной важной рекомендацией по подготовке к химиотерапии при раке является употребление большого количества чистой питьевой воды (около 2,5 литра в сутки). Это поможет ускорить обмен веществ и быстрее вывести лекарственные метаболиты.
- Накануне проведения курса лечения важно выспаться, быть полным сил и энергии. И вообще отлично было бы заиметь полезную привычку - спать не менее 8 часов в сутки, при этом ложиться до 22:00, а просыпаться до 08:00.
Психологические аспекты процесса
Во всех вышеперечисленных рекомендациях заключается физическая подготовка к химиотерапии. Однако не менее важна и моральная сторона процесса. Пациенту следует быть готовым ко всему и настроиться на борьбу, которую нужно выиграть во что бы то ни стало.
Если человек чувствует, что не в силах самостоятельно справиться с переживаниями по поводу своего диагноза или он теряет веру в исцеление, ему нужно немедленно обратиться за помощью к психотерапевту. Такой специалист в обязательном порядке имеется в штате любого онкологического диспансера.

Этапы химиотерапии
Проведение лечения делится на несколько курсов с перерывами длиной от двух недель до месяца. Это делается для того, чтобы организм пациента мог восстановиться и отдохнуть перед очередной порцией препаратов.
Лечение бывает двух видов:
- Монотерапия - лечение каким-либо одним препаратом.
- Политерапия - лечение двумя и более препаратами.
Всем, кому предстоят такие мероприятия, следует знать, как проходит химиотерапия. Независимо от выбранного вида лечение одинаково и состоит из следующих этапов:
- На лечение пациент приезжает в строго назначенную дату в онкологический диспансер, где он будет находиться в течение нескольких дней (в среднем один курс длится от трех до семи дней).
- Перед каждым курсом больной должен сдавать ряд анализов: общий и биохимический анализ крови, общий анализ мочи и другие. При необходимости проводится ЭКГ сердца, УЗИ некоторых органов (печени, почек и т. д.) и прочие процедуры.
- Онколог проверяет результаты всех обследований, измеряет вес, спрашивает об общем самочувствии больного, выслушивает жалобы. Также врач узнает, как прошел процесс восстановления после предыдущего курса. Если все в порядке, пациент размещается в палате и ожидает лечения.
- Сначала ему назначаются для химиотерапии. Они бывают в виде инъекций, таблеток и капсул. Выбор лекарственной формы зависит от диагноза и стадии заболевания и осуществляется лечащим врачом.

- Так как химиотерапия проходит с использованием ядовитых лекарств, у многих пациентов возникает тошнота и рвота. Поэтому им предлагаются медикаменты, способные облегчить данное состояние.
- В некоторых случаях онколог назначает проведение инфузий физическим раствором. Делается это для "промывания" организма, очистки его от лишних токсинов и метаболитов лекарства. Например, после лечения "Цисплатином" при раке желудка или кишечника ставят две такие капельницы.
- Следующим этапом является оценка общего самочувствия больного. Если все в порядке, ему назначается дата следующего приезда, и он отправляется домой восстанавливать силы. Количество курсов и их периодичность устанавливается индивидуально для каждого человека и может изменяться по ходу лечения.
- Периодически между курсами проводится мониторинг процесса выздоровления. Делается это с помощью лабораторных анализов крови на онкомаркеры, а также обследований с использованием компьютерной и магнитно-резонансной томографией. По итогу всех процедур врач судит об успехе проводимого лечения и может изменить курс, продолжительность лечения или вовсе отменить его.

Какие бывают препараты для химиотерапии?
У каждого онкологически больного человека своя индивидуальная схема лечения, которая зависит от диагноза, стадии заболевания и текущего прогресса лечения.
В настоящее время существует множество препаратов, направленных на борьбу со злокачественными клетками. Объединяет их всех одно - доказанное лечебное действие с высокой эффективностью. Различаются они между собой механизмом действия и составом.
1. Алкилирующие препараты. Появившись самыми первыми, они до сих пор не утратили своей актуальности. Связывая ДНК с помощью образования ковалентных связей, они вызывают гибель опухолевых К данной группе относятся такие препараты, как: "Циклофосфамид", "Хлорамбуцил", “Прокарбазин”.
2. Антиметаболиты. Останавливают образование ДНК в злокачественных клетках. Сюда относятся: “Метотрексат”, “Фторурацил”, “Меркаптопурин”, “Тиогуанин”.

3. Антимикротубулиновые лекарства. Нарушают процесс роста опухоли за счет препятствия синтезу микротрубочек - клеточных органоидов, без которых невозможно нормальное деление.
Делятся данные лекарства на две подгруппы, в зависимости от происхождения:
- Натуральные. Образованы из алкалоидов барвинка. ("Винбластин", "Винкристин").
- Синтетические препараты ("Винфлунин”, “Винорелбин”, “Виндезин”).
4. Таксаны, которые нарушают образование веретена деления клеток. Они изготовливаются из другого растения (тихоокеанского или ягодного тиса). К ним относятся: “Паклитаксел”; “Доцетаксел»; “Подофиллотоксин”; “Тенипозид”; “Этопозид”.
5. Ингибиторы топоизомеразы. Тормозят синтез ферментов топоизомераза 1 и 2 типа, которые участвуют в синтезе ДНК опухолевых клеток. Торговые наименования: “Тенипозид”; “Митоксантрон”; “Этопозид”; “Доксорубицин”; “Акларубицин”; “Марборан”; “Новобиоцин”.
Наиболее эффективные противораковые лекарства
Сюда следует отнести препараты для химиотерапии на основе платины. Они обладают самой высокой противоопухолевой активностью. Механизм действия заключается в том, что они "сшивают" пары гуанина в ДНК, тем самым нарушая ее структуру и прекращая процесс деления злокачественных клеток.
Стоит напомнить, что чем эффективнее вещество уничтожает опухоль, тем более негативно оно сказывается на здоровых тканях. Поэтому у препаратов платины побочные эффекты могут проявлять себя особенно выражено. К основным лекарствам данной группы относятся: “Платин”; “Карбоплатин”; “Цисплатин".

Последствия химиотерапии
Безусловно, ни для одного человеческого организма не может пройти бесследно такое лечение, как химиотерапия при онкологии. Последствия и восстановление могут с трудом даваться ослабленному организму. Отрицательное воздействие препаратов может сказаться практически на всех органах и системах.
Какие системы могут пострадать от лечения?
Пищеварительная система. Попадает под удар первой и поражается особенно сильно. Это объясняется высокой чувствительностью слизистой тракта к препаратам. Поэтому самыми частыми жалобами пациентов является тошнота, рвота, диарея, отсутствие аппетита.
Репродуктивная система. У представителей обоих полов возможно снижение либидо, временное бесплодие.
Иммунная система. Все лекарства против рака уничтожают иммунные клетки, поэтому защитные силы организма существенно снижаются.
Кроветворная система. Анемия, нарушение процесса образования лейкоцитов, эритроцитов и других кровяных клеток.
Нервная система. В процессе лечения практически неизбежно возникновение морального истощения больного. Он может стать плаксивым, пугливым, нервным, раздражительным.
Одним из самых неприятных последствий является возможное возникновение болей. Это может быть боль в суставах или внутренних органах.
Частым последствием является выпадение волос на всем теле человека. По окончанию курса химиотерапии волосы, ресницы и брови обязательно отрастают вновь.
Заключение
Медицина в области лечения раковых заболеваний шагнула далеко вперед, открыв множество различных противораковых препаратов. Все они обладают высокой эффективностью, однако их основным минусом является агрессивное влияние на здоровые клетки. Правильная и своевременная подготовка к химиотерапии поможет защитить организм от такого негативного влияния и снизить риск развития последствий.
Catad_tema Опухоли женской половой системы - статьи
Химиотерапия паклитакселом в сочетании с препаратом платины по сравнению с обычной химиотерапией препаратом платины у женщин с рецидивом рака яичников: испытание ICON4/AGO-OVAR-2.2
Участники испытаний ICON и AGO*
РЕЗЮМЕ
История вопроса .
Несмотря на успехи в лечении рака яичников, у большинства больных в пределах трех лет после постановки диагноза развивается рецидив заболевания. Единого мнения относительно лечения второй линии в случае рецидива в настоящее время нет. Мы провели оценку комбинации паклитаксела с препаратом платины в качестве схемы для такого лечения.
Методы .
В параллельных международных многоцентровых рандомизированных испытаниях с января 1996 по март 2002 г.г. из 119 больниц пяти стран в испытание было включено 802 больных с рецидивом чувствительного к препаратам платины рака яичников. Рецидив у больных произошел после шестимесячного периода, в течение которого лечение им не проводили. Эти больные были рандомизированы на химиотерапию комбинацией паклитаксел/платина или на обычную химиотерапию препаратом платины. Анализ, за исключением учета токсических эффектов, проводился по отношению ко всем исходно намеченным для лечения больным.
Результаты .
За медианный срок наблюдения, составлявший 42 месяца, скончалось 530 больных. Кривые выживания говорят о преимуществе комбинации паклитаксел/платина (отношение риска 0,82 , р=0,02), что дает абсолютную разницу для выживания за два года, равную 7%, между группой паклитаксел/платина и группой обычного лечения (57 и 50% ), и разницу в медианном выживании, равную 5 месяцам (29 и 24 месяца) . У 717 больных отмечалась прогрессия заболевания или они скончались. Кривые выживаемости в отсутствие прогрессии заболевания обнаруживают различие в пользу комбинации паклитаксел/платина (отношение риска 0,76 , р=0,0004), что соответствует абсолютной разности для годичного выживания при отсутствии прогрессии, равной 10% (50 и 40% ) и для разности медианной выживаемости в отсутствие прогрессии заболевания, равной 3 месяцам (13 и 10 месяцев ).
Интерпретация .
Комбинация паклитаксел/платина дает лучшую, по сравнению с обычной химиотерапией препаратом платины, общую выживаемость и выживаемость без прогрессии заболевания среди больных с рецидивом чувствительного к препарату платины рака яичников.
Введение
Рак яичников является четвертым по распространенности раком среди женщин, отвечающим (по оценочным данным) за 114 000 летальных исходов во всем мире на 2000 год.1 Лечение этого заболевания на протяжении последних тридцати лет улучшилось за счет успехов в проведении хирургической операции и химиотерапии на основе препаратов платины, однако у большинства женщин с раком яичников развивается рецидив, и они умирают в пределах пяти лет.
Единое мнение относительно оптимального лечения второй линии при рецидиве заболевания отсутствует, несмотря на несколько имеющихся препаратов. Лечение первой линии осуществляют путем химиотерапии, основанной на препаратах платины, причем все чаще используют карбоплатин (в комбинации с таксаном или без него), а не цисплатин, поскольку карбоплатин обладает меньшей токсичностью при одинаковой активности.2,3 При рецидиве заболевания вероятность ответа на повторную химиотерапию, основанную на препарате платины, зависит от длительности периода, в течение которого препарат платины не применялся.4 Когда такой период превышает шесть месяцев, многие клиницисты предпочитают повторное лечение больных препаратом платины с использованием ранее применявшегося препарата или переводя больную с карбоплатина на цисплатин или наоборот. Женщины, заболевание которых прогрессировало в условиях исходного лечения препаратом платины, а также те, у которых рецидив развивается в пределах шести месяцев после исходного лечения препаратом платины, редко отвечают на продолжение лечения препаратом платины и считаются имеющими заболевание, резистентное к платине. Для таких больных в качестве активного лекарственного препарата и был впервые предложен паклитаксел.5 Этот препарат обычно хорошо переносится, наиболее частыми побочными эффектами являются алопеция, миелосупрессия и нейропатии.
У большинства больных заболевание не является резистентным к платине, однако в пределах шести месяцев или более длительного срока после лечения первой линии у них развивается рецидив.6 Неясно, будет ли применение такого препарата, как паклитаксел, обладающего иным механизмом действия, чем препараты платины, полезным для этих больных (при использовании в сочетании с платиной) в большей степени, чем повторение обычной схемы химиотерапии на основе платины. В исследованиях на больных с рецидивами заболевания, чувствительного к платине, после применения комбинации карбоплатин/паклитаксел ответ составлял до 90%.7,8 Однако нам неизвестны какие-либо проводившиеся ранее рандомизированные испытания по сравнению комбинации паклитаксел/платина и обычной химиотерапии на основе платины у больных с раком яичников, дающих рецидив через шесть или более месяцев после химиотерапии. В рандомизированных испытаниях ICON4 и AGO-OVAR-2.2 мы поставили вопрос об эффективности комбинации паклитаксел/платина у больных с ранее леченым раком яичников. Наша задача заключалась в том, чтобы выяснить, следует ли добавлять паклитаксел к препарату платины для лечения больных с заболеванием, чувствительным к платине, и которых в противном случае лечили бы обычными схемами на основе препарата платины.
Больные и методы
Испытания ICON4 и AGO-OVAR-2.2 проводились как параллельные испытания.
Испытание ICON4 координировалось Институтом Марио Негри (Милан, Италия) (IRFMN) и Отделом клинических испытаний Совета по медицинским исследованиям (Лондон, Великобритания) (MRC CTU). Испытание AGO-OVAR- 2.2 координировалось AGO (Карлсруэ, Германия).
Больные
Больных набирали в испытание в период с января 1996 года по март 2002 года из 119 больниц в пяти странах. Больных направляли на один из трех протоколов; один из них был координирован MRC CTU для больниц Великобритании, Норвегии и Швейцарии; один был координирован IRFMN для Италии, и один проводился под эгидой AGO. Критерии для включения больных в испытание были следующими: рецидивировавший эпителиальный рак яичников, требовавший химиотерапии; ранее проводившаяся химиотерапия с использованием препарата платины; отсутствие лечения в течение срока, превышавшего 6 месяцев (>12 месяцев для группы ICON4 в Италии); отсутствие одновременного или возникшего ранее злокачественного заболевания, могущего повлиять на лечение или его результаты; полученное после информирования письменное согласие больной на участие в испытании.
Критерии, которым должны были удовлетворять больные для участия в испытании слегка отличались для трех протоколов. По протоколу MRC CTU больным в прошлом могла проводиться более чем одна линия химиотерапии, в то время как больным, рандомизированным в соответствии с итальянским протоколом AGO, разрешалось иметь только одну предшествовавшую линию химиотерапии. Для больных, рандомизированных в соответствии с итальянскими протоколами, требовалось наличие измеряемой опухоли; это требование отсутствовало для протоколов MRC CTU или AGO. Диагноз рецидива заболевания на момент включения в испытание у 18 больных по протоколу MRC CTU был основан на повышенном уровне СА125. Больные, рандомизированные на протокол AGO, должны были ранее лечиться на схеме цисплатин/паклитаксел или карбоплатин/паклитаксел; в испытании ICON4 требовалось, чтобы больные прошли предшествовавшую химиотерапию препаратом платины с паклитакселом или без него.
Методы
Больных, рандомизировали на обычную химиотерапию препаратом платины или на аналогичную дозу препарата платины с паклитакселом, причем лечение начинали в возможно более короткие сроки после рандомизации. В соответствии со всеми протоколами курсы лечения проводились раз в три недели. В соответствии с протоколом MRC CTU каждой больной следовало провести по крайней мере шесть курсов. По итальянскому протоколу, больным назначалось по крайней мере три курса, а дальнейшие три курса назначались в зависимости от ответа на лечение. По протоколу AGO, больным назначалось, как минимум, шесть курсов и максимум восемь курсов лечения, оценка ответа на лечение проводилась после второго и четвертого курсов. Все препараты вводились внутривенно в первый день каждого из курсов. Дозу карбоплатина определяли с помощью метода площади под кривой (AUC), описанного Кальвертом с соавт.9, и она составляла, как минимум, 5 (СГФ+25) мг, где СГФ представляет собой СГФ, определявшуюся радиоизотопным методом или путем сбора суточной мочи. Если скорость гломерулярной фильтрации определяли по формуле Кокрофта, доза карбоплатина составляла, как минимум, 6 (СГФ+25) мг. Запланированная минимальная доза цисплатина только для больных испытания ICON4 составляла 75 мг/м2 при введении цисплатина в качестве единственного препарата, и 50 мг/м2, когда его вводили в комбинации с другими препаратами. Больные в испытании ICON4, назначенные на лечение комбинацией паклитаксел/платина, должны были получать паклитаксел в дозе 175 мг/м2 путем 3-часового вливания с последующим вливанием карбоплатина или цисплатина в вышеуказанной дозе. Больные в протоколе AGO, назначенные в группу лечения паклитакселом/карбоплатином, должны были получать паклитаксел в дозе 185 мг/м2 в форме 3-часового вливания с последующим вливанием карбоплатина в дозе, указанной выше.
Рандомизацию для трех протоколов проводили независимо. О всех больных собирали одинаковую информацию. Отношение рандомизации между группами лечения составляло 1:1. Для рандомизации, выполнявшейся по телефону или факсу, использовали метод минимизации на компьютере. В двух протоколах испытания ICON4 (MRC CTU и итальянский) стратификация проводилась в отношении одних и тех же факторов, а именно учреждения, возраста больного, последней проводившейся химиотерапии, времени после завершения последней химиотерапии и запланированного лечения препаратом платины. Запланированная схема лечения препаратом платины должна была быть определена до рандомизации. В протоколе AGO стратификацию проводили относительно времени после завершения последней химиотерапии, а также относительно того, проводилась или не проводилась больной вторая операция циторедукции (уменьшения массы опухоли.
Для испытания ICON4 был создан независимый комитет по мониторингу данных и этике, состоявший из двух клиницистов и одного статистика, не связанных с испытанием. Ход испытания и его незакрытые результаты, а также все прочие важные внешние данные рассматривались ориентировочно раз в год на протяжении периода записи больных в испытание. Комитет не следовал заранее определенным статистическим правилам для остановки. Для испытания AGO, комитет по мониторингу данных и этике не создавали, но протокол рецензировался и принимался местными комитетами по этике каждого из участвовавших центров.
Данные, относящиеся к периоду до лечения, собирали во время рандомизации.
Данные о лечении собирали для каждого курса. Данные последующих обследований собирали раз в три месяца на протяжении первых двух лет и раз в шесть месяцев в дальнейшем. Для сбора данных этих обследований мы использовали одностраничный формуляр, содержащий вопросы относительно заболевания, жизненного статуса, симптоматики, побочных эффектов и лечения, после последнего отчета. Все эти данные собирались, проверялись и хранились в электронном виде группами, участвовавшими в испытании.
Данные о качестве жизни собирали для всех больных, лечившихся по протоколу MRC CTU и AGO. Мы использовали анкету о качестве жизни QLQ-C30 (версия 2.0), разработанную Европейской организацией по исследованию и лечению рака (EORTC). Больные, лечившиеся по протоколу MRC CTU, заполняли анкету исходно, перед каждым курсом лечения по протоколу, а также во время визитов через 6, 9 и 12 месяцев. Больные, получавшие лечение по протоколу AGO, заполняли анкету исходно, перед вторым и третьим курсами лечения по протоколу, в конце лечения по протоколу и раз в три месяца на протяжении года после завершения лечения по протоколу.
Мы выполнили несколько анализов для подгрупп. Критерии для подгрупп включали группу рандомизации, время после завершения последней химиотерапии, число предшествовавших линий химиотерапии, проводившееся ранее лечение таксанами, препарат платины, запланированный для лечения, возраст и функциональный статус.
Статистический анализ
Главным учетным критерием была общая выживаемость; вторичными критериями были выживание без прогрессии заболевания и качество жизни. Когда проводились расчеты размеров исходной выборки, имелись лишь немногочисленные данные относительно исхода рецидивировавшего рака яичников. Мы ожидали, что двухлетняя выживаемость будет составлять около 5% для контрольной группы, а абсолютные различия в выживаемости за два года не будут превышать 5-10%.
Всего мы запланировали для испытания 800 больных, чтобы уверенное выявить абсолютные различия в выживаемости за два года, составляющие 5% (5-10%) с уверенностью 95% при уровне достоверности в 5%; это соответствует отношению риска 0,77. На завершающем заседании 8 февраля 2001 года Комитет по мониторингу данных и этике отметил, что выживание в контрольной группе было значительно более высоким, чем при исходных расчетах уверенности. Двухлетнее выживание в группе, где проводилось обычное лечение, составляло 50%. Поэтому мы пересмотрели этот вопрос. Мы рассчитали, что 800 больных будет достаточно для надежной идентификации абсолютных различий, составляющих 11% для выживаемости за два года (50-61%) с вероятностью 90% при уровне достоверности в 5%, что дает отношение риска, равное 0,71. Поэтому запланированное для испытания число больных осталось без изменений.
Мы сравнили кривые Каплана-Мейера для общей выживаемости и выживаемости без прогрессии заболевания с вариантом лог- рангового критерия Мантел-Кокса при стратификации на три группы рандомизации. Общее выживание определялось как время от момента рандомизации до летального исхода от любой причины; больные, о которых было известно, что они живы на момент анализа, учитывали на момент последнего обследования. Мы определили время выживания без прогрессии заболевания как время от момента рандомизации до первого проявления прогрессии заболевания или летального исхода от любой из причин; больные, о которых было известно, что они живы и не имеют признаков прогрессии заболевания на момент анализа, учитывали на момент проведения последнего обследования. Само по себе повышение концентрации СА125, т.е.
повышение при отсутствии клинических или радиологических признаков прогрессирующего заболевания, не считалось указанием на прогрессию заболевания. Абсолютное преимущество на конкретный момент времени рассчитывалось по выживаемости, оцененной в контрольной группе по Каплану- Мейеру на этот момент времени (выживание в контроле) и отношению риска с использованием следующего выражения: абсолютное преимущество=exp(отношение риска х log[выживание в контроле])- выживание в контроле.
Этот же подход был принят для выживания без прогрессии заболевания. Хотя такой подход косвенно предполагает наличие пропорциональных рисков, он является более предпочтителен чем учет различий между кривыми по Каплану- Мейеру в индивидуальные моменты времени. Мы рассчитывали различия в отношении медиан аналогичным образом, однако, с использованием выражения: разность медиан=(медиана контроля/отношение риска) – медиана контроля. Этот подход исходит из тог, что значения времени выживания имеют приблизительно экспоненциальное распределение.
Мы оценили относительные преимущества химиотерапии препаратами платины для выживания в опытном порядке в подгруппах, определенных на основе группы рандомизации, времени после завершения последней химиотерапии, числа предыдущих линий химиотерапии, предшествовавшего применения таксанов, препарата платины, запланированного для лечения, т.е. карбоплатина или цисплатина, возраста и функционального статуса. Для того, чтобы оценить различия в относительной величине эффекта для различных подгрупп, мы использовали критерий χ2 для взаимодействия или, в тех случаях, когда это было возможно, критерий χ2 для тренда.
Для анализа данных по качеству жизни, как это было рекомендовано, мы использовали пять функциональных шкал (физическую, ролевую, эмоциональную, когнитивную и социальную), девять шкал симптоматики (чувство усталости, тошнота и рвота, боли, одышка, бессонница, потеря аппетита, запор, понос и финансовые трудности), а также общий статус здоровья. С учетом характера рака яичников нас особенно интересовали чувство усталости, тошнота/рвота и болевая симптоматика, а также общее (глобальное) состояние здоровья в качестве общего критерия. Для каждого критерия мы анализировали два набора суммарных статистических параметров: наихудший балл и площадь под кривой за первые шесть месяецв.11 Для анализа использовался непараметрический критерий Манна- Уитни.12 Мы выбрали значение р=0,005 в качестве значения для выявления достоверности (из-за множественных сравнений).
Анализы проводились для всех больных, включенных в испытание (в англоязычной литературе -- критерий "намерение лечить"), за исключением анализа токсических эффектов. Анализы в отношении токсических эффектов ограничивались больными, получившими по крайней мере один курс назначенного лечения. Все значения р являются двусторонними. Анализ был проведен с помощью пакета SAS (версия 8.20).
Роль источника финансирования
Спонсоры испытания не играли роли в планировании испытания, сборе данных, анализе данных, интерпретации данных или написании отчета.
Результаты
В испытание было включено 802 больных. Длитеьность периода поступления больных в испытание варьировал для трех протоколов: для итальянской группы ICON4 – с января 1996 по март 2002 г.г.; для группы MRC CTU ICON4 – с мая 1996 по март 2002 г.г., и для AGO – с октября 1996 по сентябрь 1999 г.г. Четыреста десять больных было включено в группу, получавшую обычную химиотерапию на основе препаратов платины, и 392 больных в группу паклитаксел/платина (Рис. 1).
Характеристики до лечения были одинаковыми для обеих групп (Таблица 1).
Типы полученного лечения указаны в Таблице 2. 580 больных (72%) в обеих группах лечения получили минимум шесть курсов химиотерапии (Рис. 1). Причины незавершения шести курсов лечения включали следующее: прогрессия заболевания или летальный исход (109 ), токсические эффекты во время лечения 77 ) и желание больной (9 ). Только три больные не получили назначенной химиотерапии (Рис. 1). 123 (41%) из 300 больных в группе, получавшей обычное лечение, и 129 (40%) из 322 больных, получавших лечение паклитакселом и карбоплатином, получили более 90% запланированной общей дозы, а 54 (18%) из 300 больных и 76 (23%) из 330 больных, соответственно, получили более 90% общей дозы карбоплатина. Соответствующие цифры для паклитаксела в группе, получавшей паклитаксел/карбоплатин, составляли 266 (71%) из 376 больных в отношении общей дозы и 160 (43%) из 376 в отношении общей интенсивности дозы.
В Таблице 3 приведена доля больных, у которых во время лечения отмечался умеренный или тяжелый побочный эффект. Как и можно было ожидать, комбинация паклитаксел/платина давала более высокий процент алопеции по сравнению с обычной химиотерапией препаратом платины. Процент токсических эффектов умеренной или тяжелой степени в отношении кроветворения был более высоким среди больных, получавших обычную химиотерапию препаратом платины, по сравнению с группой, где лечение проводилось комбинацией паклитаксел/платина. Умеренные или тяжелые неврологические токсические эффекты отмечались у 76 (20%) больных, получавших комбинацию паклитаксел/платина. Прочие токсические эффекты были редкими в обеих группах лечения.
К марту 2003 года (среднее медианное время наблюдения 42 месяца) умерли 530 больных (66%). Кривые выживаемости соответствуют отношению риска 0,82 (95% ДИ 0,69-0,97, р=0,02; Рис. 2), что соответствует абсолютной разности в двухгодичной выживаемости, составляющей 7% в пользу химиотерапии комбинацией паклитаксел/препарат по сравнению с обычным лечением (57 и 50% ). Для медианного выживания отношение риска соответствует разности, равной 5 месяцам (29 и 24 месяца ). У 717 больных (89%) развилось прогрессирующее заболевание или они скончались. Кривые выживания без прогрессии заболевания, приведены на Рис. 3. Отношение риска, составляющее 0,76 (0,66-0,89, р=0004) в пользу схемы паклитаксел/препарат платины, соответствует оценочной абсолютной разности значений годичного выживания без прогрессии заболевания, составляющей 10% (40 и 50% ). Этот результат соответствует абсолютной разности для медианного выживания без признаков прогрессии заболевания, составляющей 3 месяца в пользу схемы паклитаксел/препарат платины (9 и 12 месяцев ).
У 69 (54%) из 128 больных в группе, получавшей обычную химиотерапию, наблюдался полный или частичный ответ на лечение, по сравнению с 78 (66%) из 119 больных в группе, получавшей схему паклитаксел/препарат платины.
Соответственно, ответ на лечение представляется лучшим для группы паклитаксел/препарат платины (разность 12% [-0,1% до 24%], р=0,06). Мы не отметили каких-либо четких признаков того, что схема паклитаксел/платина была более эффективной или менее эффективной по сравнению с обычной химиотерапией препаратом платины для любой из подгрупп по критериям общей выживаемости или выживаемости без признаков прогрессии заболевания (Рис. 4 и 5).
Детали лечения, проводившегося во время прогрессии заболевания, имелись для 437 из 536 больных. Всего 70 (31%) больных в обычной группе лечения получали при прогрессии лечение на основе препаратов таксана. В группе, получавшей комбинацию паклитаксел/платины, 16 (8%) больных продолжали получать при прогрессии дальнейшее лечение схемой на основе таксана.
В группе, использовавшей протокол MRC CTU ICON4, 482 (90%) из 536 больных заполнили анкету по оценке качества жизни исходно до начала лечения. Все шкалы для двух групп лечения были сбалансированными. Большинство больных не имели функциональных затруднений или они были незначительны, число симптомов умеренной или большой тяжести исходно было невелико. На протяжении первых шести месяцев после рандомизации значения наихудшего балла и площадей под кривыми не отличались для двух групп лечения по всем пяти функциональным шкалам, восьми из девяти шкалам симптоматики и по глобальному статусу здоровья. Единственным исключением была тошнота и рвота, которая была более тяжелой для больных, получавших обычную химиотерапию (р=0,0014 для наихудшего балла, р=0,005 для площади под кривой). На Рис. 6 приведены значения балла во времени для трех симптомов, наиболее типичных для рака яичников – чувства усталости, тошноты и рвоты, а также для боли и глобального статуса здоровья. Для глобального статуса здоровья отмечалось незначительное снижение доли больных, определяемых как имеющие нехорошее самочувствие или очень низкий статус здоровья на протяжении первых шести месяцев. Аналогичная тенденция отмечалась для чувства усталости. Напротив, болевая симптоматика в обеих группах возвращается к значениям, характерным для периода до лечения.
Хотя имеются определенные указания на различия по тошноте и рвоте в пользу группы, получавшей паклитаксел/платина, такие различия носят временный характер, относясь лишь к первым 15 неделям.
Обсуждение
С учетом данных по выживаемости без прогрессии заболевания и общей выживаемости, в нашем испытании достаточно число больных выжило и находилось в группе риска на 4-летний срок, чтобы сделать вывод о том, что общие результаты на этот срок являются надежными. Девяносто процентов больных было рандомизировано после первого рецидива, а 75% более чем через 12 месяцев после завершения химиотерапии препаратом платины. Считается, что такие больные имеют разумный прогноз. То обстоятельство, что наше испытание является крупномасштабным, позволило нам проанализировать подгруппы для оценки того, насколько однотипным является эффект комбинации паклитаксел/ платина. Тем не менее, многие из подгрупп невелики по численности и поэтому возможность выявления реальных различий невелика. Но, как бы то ни было, хорошие данные в пользу большего эффекта или меньшего эффекта комбинации паклитаксел/платины по сравнению с обычным лечением в любой из подгрупп отсутствуют. Величина эффекта комбинации паклитаксел/платина близка для разных групп рандомизации, несмотря на различия в критериях, использованных для включения больных в испытание, и факторы стратификации. Далее, нет указаний на то, что эффект комбинации паклитаксел/платина отличался для больных, которые получали таксаны в качестве составной части лечения первой линии (около 40% общего числа рандомизированных больных) и тех больных, которые таксаны не получали.
Паклитаксел в качестве индивидуального препарата сравнивался с циклофосфамидом, доксорубицином и цисплатином (схема САР) среди больных, давших ответ на химиотерапию первой линии препаратом платины, однако заболевание у которых рецидивировало после более чем 12-месячного периода отсутствия лечения.13 В испытании, о котором идет речь, у 97 больных с оцениваемым заболеванием монотерапия паклитакселом давала медианный срок без прогрессии заболевания, составлявший 9 месяцев, по сравнению с 15,7 месяцами для схемы САР (отношение риска 0,69 ). Средняя общая выживаемость составляла 25,8 месяца для монотерапии паклитакселом и 34,7 месяца для схемы САР (0,58 ). Хотя число больных недостаточно велико, чтобы сделать окончательные выводы, эти результаты позволяют полагать, что химиотерапия на основе препарата платины является важным компонентом химиотерапии при рецидиве, если заболевание остается чувствительным к платине.
Наши результаты указывают на аддитивный эффект платины и паклитаксела.
Сходные данные были отмечены в ряде испытаний первой линии (комбинация циклофосфамид 750 мг/м2 в сочетании с цисплатином 75 мг/м2 использовалась в испытании группы GOG-11114 и в испытании OV1015), но не в других испытаниях (монотерапия цисплатином в дозе 100 мг/м2; испытание GOG-13216 и карбоплатин с минимальным значением до AUC 5 или комбинация циклофосфамида 500 мг/м2, доксорубицина 20 мг/м2 и цисплатина 50 мг/м2, использовавшаяся в испытании ICON36)17. Результаты испытаний ICON3 и GOG-132 отличаются от положительного результата, отмеченного в нашем испытании, в котором 85% больных в группе паклитаксел/платина получали комбинацию карбоплатина и паклитаксела. Однако исследованные контингенты больных группы довольно различны. Женщины в нашем исследовании могут считаться имеющими чувствительное к платине заболевание и имеющими высокую вероятность ответа на дальнейшее назначение препарата платины, однако их заболевание, вероятно, менее чувствительно к платине, чем у больных, которым химиотерапия не проводилась вообще. В пользу этой теории говорит ответ на обычную химиотерапию, равный в наших условиях 54%, что слегка ниже, чем ожидается для лечения первой линии.14 Среди больных, давших рецидив заболевания, чувствительного к платине, паклитаксел может компенсировать относительное снижение чувствительности к платине. Другое возможное объяснение заключается в том, что количество платины, которое эти больные могут получить во время терапии второй линии ограничено по сравнению с количеством, которое они могут получить во время терапии первой линии. Например, лишь 40% наших больных получили более 90% общей запланированной дозы карбоплатина. Для сравнения укажем, что примерно 75% больных получили более 90% запланированной общей дозы карбоплатина в испытании ICON3 при терапии первой линии.6 Предварительные результаты испанского рандомизированного испытания по сравнению карбоплатина с комбинацией паклитаксел/карбоплатин у 81 больной с теми же самыми критериями включения в испытание, что и в протоколе MRC CTU, близки к нашим результатам в отношении процента реагирования, времени выживания без прогрессии заболевания и токсических эффектов.18 Паклитаксел в сочетании с препаратом платины обычно является более токсичной схемой, по сравнению с обычной схемой химиотерапии на основе платины, вызывая большую алопецию и неврологические токсические эффекты. Неврологические токсические эффекты отмечались у 20% больных, что близко к цифрам, наблюдающимся при лечении первой линии.6 Эта доля меньше по сравнению с ожидаемой, в частности поскольку треть больных ранее получала препарат таксана. Опыт исследований Дизона и соавт.8 является сходным, и применение доцетаксела у 3% наших больных могло внести определенный, хотя и незначительный вклад в меньший процент периферического неврита. Однако соблюдение назначенных правил лечения было хорошим, причем 72% больных завершили по крайней мере шесть курсов лечения. Другой причиной, конечно, могло быть то, что больные со склонностью к развитию нейропатий не вошли в испытание из-за опыта полученного ими во время лечения первой линии. Обычная химиотерапия препаратом платины связана с более серьезными токсическими эффектами в отношении кроветворения по сравнению со схемой паклитаксел/платина, что глвлрит в поддержку опубликованных ранее сообщений, что паклитаксел может оказывать защитное воздействие на костный мозг.19 Лечение рецидивов рака яичников содержит значительный паллиативный компонент. Поэтому оценка больной собственного качества жизни является важной, чтобы сказать, будет ли схема паклитаксел/платина иметь какие-либо недостатки по отношению к обычной химиотерапии препаратом платины (или наоборот) с точки зрения связанных с лечением токсических эффектов и бессимптомного интервала. Мы не обнаружили ясных указаний, что какая-то из использованных схем является хуже другой в отношении функциональных аспектов, симптоматики или глобального статуса здоровья.
Наши результаты говорят о положительном эффекте комбинации паклитаксел/платина на общую выживаемость и выживаемость без прогрессии заболевания в группе больных с рецидивом чувствительного к платине рака яичников. Паклитаксел чаще всего комбинировали с карбоплатином, а наиболее часто применявшаяся обычная схема химиотерапии препаратом платины включала использование карбоплатина в качестве единственного агента. Поэтому мы полагаем, что все женщины, у которых рецидив развивается позже, чем через 6 месяцев после завершения химиотерапии препаратом платины, должны рассматриваться в качестве кандидатов на комбинированную химиотерапию платиной и паклитакселом, даже если они получали паклитаксел в качестве составной части схемы лечения первой линии.
Заявление о конфликте интересов J.A.Lederman получил небольшой гонорар за специальные консультации компании Бристол-Майерс Сквибб.
Таблица 1. Группы рандомизации и исходные характеристики больных
|
Характеристика |
Обычная ХТ |
Паклитаксел+платина |
|
Численность в группе рандомизации |
||
|
Возраст (годы) |
||
|
Функциональный статус по ВОЗ |
||
|
Планируемый препарат платины |
||
|
Карбоплатин |
||
|
Цисплатин |
||
|
Последняя химиотерапия |
||
|
Паклиатаксел и карбоплатин |
||
|
Карбоплатин |
||
|
Паклитаксел и цисплатин |
||
|
Доцетаксел и карбоплатин |
||
|
Другие препараты на основе платины |
||
|
Другие препараты |
||
|
Число предшествующих линий химиотерапии |
||
|
Неизвестно |
||
|
Время после завершения последней химиотерапии (месяцы) |
||
Таблица 2. Лечение по протоколу во время испытания
|
Обычная ХТ |
Паклитаксел+платина |
|
|
Лечение |
||
|
Карбоплатин (моно) |
||
|
Карбоплатин и цисплатин* |
||
|
Цисплатин и доксорубицин |
||
|
Цисплатин (моно) |
||
|
Карбоплатин в комбинации (не с таксаном) |
||
|
Паклитаксел и карбоплатин |
||
|
Паклитаксел и цисплатин |
||
|
Паклитаксел, карбоплатин и цисплатин* |
||
|
Паклитаксел (моно) |
||
|
Лечение не проводится или неизвестно |
||
Таблица 3. Умеренные или тяжелые побочные эффекты во время лечения
|
Токсические эффекты |
Обычная ХТ |
Паклитаксел+платина |
|
Неврологические (степени 2-4) |
||
|
Неизвестно |
||
|
Гематологические* |
||
|
Неизвестно |
||
|
Инфекции* |
||
|
Неизвестно |
||
|
Неизвестно |
||
|
Мукозиты (степени 2/3) |
||
|
Неизвестно |
||
|
Тошнота и рвота (степени 2-4) |
||
|
Неизвестно |
||
|
Алопеция (степени 2-4) |
||
|
Неизвестно |
Литература
1 Parkin DM, Bray FI, Devesa SS. Cancer burden in the year 2000: the global picture.Eur J Cancer
2001; 37:
S4–66.
2 The ICON collaborators. ICON2: randomised trial of single-agent carboplatin against three-drug combination of CAP (cyclophosphamide, doxorubicin, and cisplatin) in women with ovarian cancer. Lancet
1998; 352:
1571–76.
3 Advanced Ovarian Cancer Trialists’ Group. Chemotherapy in advanced ovarian cancer: four systematic meta-analyses of individual patient data from 37 randomized trials. Br J Cancer
1998; 78:
1479–87.
4 Markman M, Reichman B, Hakes T, et al.
Second-line platinum therapy in patients with ovarian cancer previously treated with cisplatin. J Clin Oncol
1991; 9:
389–93.
5 Trimble EL, Adams JD, Vena D, et al.
Paclitaxel for platinum-refractory ovarian cancer: results from the first 1,000 patients registered to National Cancer Institute Treatment Referral Center 9103. J Clin Oncol
1993; 11:
2405–10·6
6 The International Collaborative Ovarian Neoplasm (ICON) Group. Paclitaxel plus carboplatin versus standard chemotherapy with either single-agent carboplatin or cyclophosphamide, doxorubicin, and cisplatin in women with ovarian cancer: the ICON3 randomised trial. Lancet
2002; 360:
505–15.
7 Rose PG, Fusco N, Fluellen L, et al. Second-line therapy with paclitaxel and carboplatin for recurrent disease following first-line therapy with paclitaxel and platinum in ovarian or peritoneal carcinoma. J Clin Oncol
1998; 16:
1494–97.
8 Dizon DS, Hensley ML, Poynor EA, et al. Retrospective analysis of carboplatin and paclitaxel as initial second-line therapy for recurrent epithelial ovarian carcinoma: application toward a dynamic disease state model of ovarian cancer. J Clin Oncol
2002; 20:
1238–47.
9 Calvert AH, Newell DR, Gumbrell LA, et al. Carboplatin dosage: prospective evaluation of a simple formula based on renal function. J Clin Oncol
1987; 7:
1748–56.
10 Parmar MKB, Machin D. Survival analysis: a practical approach. Chichester: John Wiley, 1995.
11 Fayers PMF, Aaronson NK, Bjordal K, Curran D, Groenvold M, on behalf of the EORTC Quality of Life Study Group. EORTC QLQ-C30 scoring manual, 3rd edn.
Brussels: European Organisation for the Research and Treatment of Cancer, 2001: 86.
12 Girling D, Parmar MKB, Stenning S, Stephens R, Stewart L. Clinical trials in cancer.
Oxford: Oxford University Press, 2003.
13 Cantu MG, Buda A, Parma G, et al. Randomized controlled trial of single-agent paclitaxel versus cyclophosphamide, doxorubicin, and cisplatin in patients with recurrent ovarian cancer who responded to first-line platinum-based regimens. J Clin Oncol
2002; 20:
1232–37.
14 McGuire WP, Hoskins W, Brady MF, et al. Cyclophosphamide and cisplatin compared with paclitaxel and cisplatin in patients with stage III and stage IV ovarian cancer. N Engl J Med
1996; 334:
1–6.
15 Piccart MJ, Bertelsen K, James K, et al. Randomized intergroup trial of cisplatinpaclitaxel versus cisplatin-cyclophosphamide in women with advanced epithelial ovarian cancer: three-year result. J Natl Cancer Inst
2000; 92:
699–708.
16 Muggia FM, Braly PS, Brady MF, et al. Phase III randomized study of cisplatin versus paclitaxel versus cisplatin and paclitaxel in patients with suboptimal stage III or IV ovarian cancer: a gynecologic oncology group study. J Clin Oncol
2000; 18:
106–15.
17 Sandercock J, Parmar MKB, Torri V, et al. First-line treatment for advanced ovarian cancer: paclitaxel, platinum and the evidence. Br J Cancer
2002; 87:
815–24.
18 Gonzalez Martin AA, Calro E, Bover I, et al. Randomised phase II study of carboplatin versus paclitaxel-carboplatin in platinum-sensitive recurrent advanced ovarian carcinoma with assessment of quality of life: a GEICO study (Spanish Group for Investigation on Ovarian Carcinoma). Proc ASCO
2003; 22:
(abstr 1812).
19 van Warmerdam LJ, Huizing MT, Giaccone G, et al. Clinical pharmacology of carboplatin administered in combination with paclitaxel. Semin Oncol
1997; 24
(suppl 2):
97–104.
Рис. 1. Профиль испытания
Рис. 2. Общая выживаемость 
Рис. 3. Выживание без прогрессии 
Рис. 4. Эффект XT комбинацией Т+платина на общую выживаемость в подгруппах 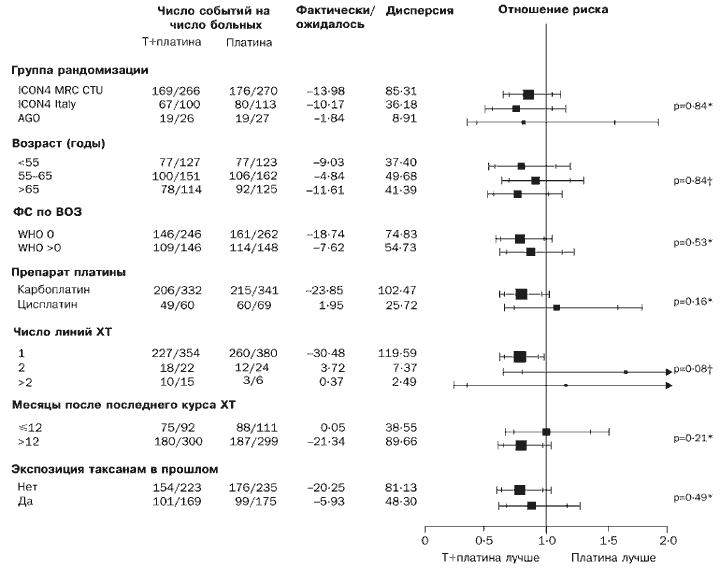
*Взаимодйствие
Тренд
Сокращения: Т - паклитаксел; XT - химиотерапия; ФС - функциональный статус.
Это основное лечение или дополнение к ключевому хирургическому методу в случае эффективности проведения операции.
В зависимости от механизма воздействия все препараты для химиотерапии по классификации разделены на цитостатики, противораковые антибиотики, платиновые, антрациклины, таксаны, винкалкалоиды, антрациклины, алкилирующие агенты, хотя степень воздействия на клеточные процессы и опухоль у них разная.
Лучшие препараты при химиотерапии
Согласно исследованиям, эффективно при химиотерапии использование иммуностимуляторов с широким спектром воздействия на опухоль в организме. Сегодня разработано множество эффективных химиопрепаратов с целью:
- воздействия на активную фазу клеточного цикла G2;
- стимуляцией ДНК структур и митозных белков.
Наиболее эффективные препараты для химиотерапии нового поколения:
- алкилирующие агенты (Ифосфамид, Мелфалин, Прокарбазин, Циклофосафамин, Бусульфан, Декарбазин) как противоопухолевые мощные средства в составе с азотистыми и планиновыми ядовитыми соединениями, направленные на устранение подавление опухоли любых размеров и любого типа рака, в частности лейкоза и отрицательно воздействующими на заряженные частицы в ДНК молекулах;
- антиметаболиты (Антифолат, Метротрахаит, Фторурацил, Тимидин, Гемцитабин, (Цитарабин) как аналоги фолиевой кислоты, применимые при лечении детской лейкемии, способствуют репарации ингибированию синтеза в ДНК, улучшению гематологического уровня в крови, внедрению в метаболические процессы, созданию новых ДНК структур. Применимы при лечении рака молочной железы, головы и шеи, поджелудочной железы, желудка, анального отверстия, пищевода, толстой кишки;
- антрациклины как мощные противораковые препараты (в частности Даунорубицин), приводящие к образованию свободных радикалов кислорода, ингибированию синтеза синтеза ДНК, ферментации топоизомеразы, репарации ДНК. Даунорубицин токсичен для сердечной мышцы, что должны принимать во внимание онкологи при назначении препарата, а также Бидарубицина, Эпирубицина, Митоксантрона;
- антибиотики противораковые (Блеомицин, Адриамицин, Метотрексат Видарабин, Тимидин, Фторурацил, Гемцитабин, Кладрибин, Фторурацил) как препараты нового поколения, но могут приводить к побочным реакциям: тяжелейшей интоксикации в ЖКТ, судорогам, подавлению костного мозга;
- винкаалкалоиды (Тубулин, Винорельбин, Винбластин, Винкристин) как менее токсичные препараты растительного происхождения с экстрактом барвинка (листьев) для уничтожения раковых клеток;
- платиновые препараты, приводящие к разрушению их ДНКструктур, подавлению функций и гибели злокачественных клеток. Проводится химиотерапия и платина как действующее вещество в составе: Оксалиплатина, Карбоплатина, Цисплатина способна оказать сильнейший платиновый эффект, но возможно токсическое поражение почечных структур, развитие невропатии;
- цитостатики с комбинированным воздействием (Дакарбазин, Прокарбазин, Гидроксимочевина, Капецитабин, Гемзар, Гемцитабин Фторурацил 5), способствующие встраиванию в генетический аппарат раковых клеток, препятствующие их делению;
- антрациклины (Адрибластин, Рубомицин, Подофиллотоксин) для сбора свободных радикалов, ингибиции топоизомеразы, приводящей к гибели раковых ДНК клеток и структур.
При проведение терапии в курс могут быть включены топоизомеразы2 с целью встраивания в ДНК структуры, оказания подавляющего воздействия на раковые клетки и метастазы, стабилизации микротрубочек полимеразы. Все химиопрепараты отличны по принципу действия и наличию побочных эффектов. При их назначении врачами в первую очередь разрабатываются лечебные протоколы, дабы не причинить сильный вред организму больного при их введении.
Какие препараты помогут восстановиться после химиотерапии
В целях реабилитации больным назначаются фитопрепараты для восстановления организма, в частности почек в случае поражения, когда у больного наблюдаются признаки диареи, рвоты. Назначается:
- Уромитексан как средство для восстановления состава крови при появлении отечности, инфильтрации и некроза эпителиальных клеток в ЖКТ;
- Филстим для восстановления микрофлоры в иммунной системе после проведённой химиотерапии;
- Лактогон, Нейрорубин, аскорбиновая кислота, витамины группы B, Лактовит форте;
- Гепадиф, Глутаргин, Карсил, Эссенциале форте Н для восстановления клеток печени, когда токсические вещества приводят к сильнейшей нагрузке печени, затруднению функций гепатоцитов, изменению параметров крови;
- кардиотоники для восстановления пораженной сердечно-сосудистой системы;
- Квамател, Нексиум, Проксиум для восстановления кишечной функции.
Многие пациенты после химиотерапии начинают страдать депрессией, в частности дуоденальной, в случае выброса большого количества гормонов в 12-перстную кишку, развития воспалительного процесса и нарушения баланса нейропептидов. В данном случае назначаются нестероидные, противовоспалительные средств, антиоксиданты.
Ни для кого не секрет, что даже единственный курс химиотерапии приводит не только к побочным эффектам, но и пагубно отражается на организме в целом. Основная задача врачей при разработке лечения при онкологии – оказать максимальное воздействие на раковые клетки, снизить их степень размножения, предотвратить распространение метастаз по всему организму.
Именно прием химиопрепаратов в комплексе позволит добиться устойчивой ремиссии, предотвратить размножение опухоли и дачу метастаз, тем самым продлить жизнь больному. В то же время лекарства при проведении химиотерапии – это сильнейший удар по иммунной системе, многим органам: сердцу, почкам, печени. Убивают не только патологические, но и здоровые клетки в организме. Что же делать? Для продления жизни ничего иного не остается и это лучшее противоядие (в частности препараты платины) в борьбе с опухолевыми клетками в организме на сегодняшний день. Пока ничего иного и лучшего онкологами не придумано.
Химиотерапию заменят на новое лекарство
Специалистами в области борьбы с раком создано новое лекарство, позволяющее эффективно лечить лейкемию. При этом важно, что выживаемость пациентов возрастает на девяносто процентов. По мнению экспертов, данный препарат можно считать настоящим открытием, так как он практически завершает эру химиотерапии.
Как известно, при лечении лейкемии химиотерапия представляет собой неотъемлемую часть лечения. Для уничтожения раковых клеток используются токсичные препараты. Не секрет, что они вредят не только клеткам опухоли, но и организму в целом. Побочных эффектом немало, и самые известные из них - это общая слабость, выпадение волос, болезненные состояния, развитие инфекционных болезней. Все это время пациенты находятся в депрессивном состоянии. Причем, некоторые пациенты настолько плохо переносят химиотерапию, что нередко отказываются от подобного лечения, предпочитая умереть без лишних мучений.
Разработанный учеными препарат имеет название ибрутиниб. Его испытания показали невероятную эффективность в терапии лейкемии. Особенно радует, что в значительной мере увеличилась выживаемость, по сравнению с ранее применяемой химиотерапией.
Использование ибрутиниба привело к удивительным результатам, и почти все больные, получавшие препарат, перешли в состояние ремиссии. Следует отметить, что использование обычной химиотерапии не позволяло достичь подобных результатов. К тому же, у некоторых пациентов к химиотерапии возникает резистентность, и в этом случае ибрутиниб дает им надежду.
Учеными в Мельбурне были проведены исследования с участием триста девяноста пациентов, диагнозом которых являлась хроническая лимфоцитарная лейкемия. Результаты показали, что благодаря новому препарату выживаемость поднялась до девяноста процентов. Это на восемьдесят один процент выше, чем при лечении химиотерапией. Кроме того, благодаря использованию ибрутиниба была обеспечена ремиссия для сорока процентов в течение года, хотя обычно при химиотерапии этот показатель составляет лишь четыре процента.
По мнению автора исследования, доктора Кон Там из Австралии, со временем ибрутинибом можно полностью заменить химиотерапевтическое лечение, когда речь идет о лейкемии. Кроме того, врач считает, что со временем от химиотерапии можно будет отказаться навсегда.
Популярные статьи
Новое
Популярное
Спасибо за вопрос
Ваш вопрос был получен и отправлен нашему специалисту.
Минусы химиотерапии с помощью таблеток
Как лечение рака с помощью химиотерапии в виде может влиять на собственные результаты показало новое исследование, провеленное в Университете штата Мичиган. Исследование подчеркивает, с какими проблемами сталкиваются пациенты при применении таблетированной химиотерапии за пределами контролируемой среды онкологической клиники.
Диагностка и лечение онкологии в медицинских центрах Израиля подробная информация
Если у вас есть вопросы к врачам онкологам вы можете задать у нас на сайте в разделе консультации
Какие препараты используются при проведении химиотерапии?
Химиотерапия является одним из ведущих направлений в сфере лечения онкологических патологий. Чаще всего в отношении пациентов применяется полихимиотерапия, предполагающая введение нескольких противоопухолевых препаратов различных групп.
Химиотерапевтическое воздействие может использоваться как основное лечение либо в качестве дополнения к хирургическому и лучевому методу терапии.
Виды препаратов для химиотерапии
Все химиотерапевтические препараты классифицируются на несколько групп, в соответствии с механизмом их действия:
- Алкилирующие агенты;
- Антрациклины;
- Платиновые препараты;
- Противораковые антибиотики;
- Винкалкалоиды;
- Цитостатики;
- Таксаны и пр.
Каждая группа лекарств способна воздействовать на разные фазы клеточных процессов и жизненных циклов.
Алкилирующие агенты
Принцип действия препаратов этой группы основан на образовании ковалентных связей с ДНК цепью.
Еще не определено, как именно происходит гибель клеточных структур после алкилирующего воздействия, но точно ясно, что эти препараты вызывают ошибку в процессах считывания генетической информации, что приводит к подавлению образования соответствующих белков.
Однако существует глутатионовая система – естественный иммунитет от алкилирующих агентов, поэтому при повышенном содержании глутатиона эффективность алкилирующих агентов в отношении злокачественной опухоли будет пониженной.
Но вследствие приема этих препаратов существует вероятность возникновения вторичного рака, самой распространенной формой которого является лейкемия, проявляющая через несколько лет после химиотерапии.
Основными представителями этой группы являются препараты вроде Циклофосфамида, Эмбихина и Ифосфамида, Хлорамбуцила и Бусульфана, Прокарбазина и BCNU, средств на основе нитрозомочевины.
Противораковые антибиотики
Эти препараты никак не связаны с общеизвестными антибиотическими средствами. Механизм их воздействия заключается в замедлении генного деления онкоклеточных структур.
Противораковые антибиотики способны влиять на различные клеточные фазы, поэтому иногда механизмы их воздействия несколько отличаются. Препараты этой группы в плане побочных реакций наиболее опасны для легочных структур, потому как из-за образования свободных кислородных радикалов они оказывают токсическое воздействие на легкие.
Самыми известными противораковыми антибиотиками считаются Адриамицин и Блеомицин. Чаще всего его применяют в полихимиотерапии вместе с Цитотоксином.
Не нужно путать антибиотики с антиметаболитами, активные вещества которых встраиваются в генетический клеточный аппарат. В результате при делении раковой клеточной структуры происходит ее уничтожение.
Это препараты Метотрексат, Гемзар, Гемцитабин, Флударабин и Кладрибин, 5-Фторурацил и пр. Последний препарат в качестве побочных реакций может подавлять костный мозг, вызывает тяжелейшие интоксикации системы ЖКТ, провоцирует появление нейротоксинов, вызывающих приступы судорог и состояние комы.
Для исключения подобных последствий в качестве противоядия онкопациентам назначается Тимидин. Аналогом 5-Фторурацила, принимаемым перорально, является Капецитабин, но он имеет идентичные побочные последствия.
Антрациклины
К медикаментам этой группы относят Адрибластин и Рубомицин. В их составе присутствует специфическое антрациклиновое кольцо, взаимодействующее с ДНК клетками.
Коме того, компоненты этих препаратов могут подавлять химические реакции, протекающие при образовании фермента топоизомеразы (II), и образовывать радикалы свободной группы, которые повреждают структурную основу ДНК раковых клеток.
Препараты Даунорубицин и Доксорубицин также относятся к антрациклиновой группе и имеют природное происхождение – их активный компонент был выделен из почвенных грибков. Они образуют свободные кислородные радикалы, нарушающие целостность и ингибирование синтеза ДНК.
Антрациклины весьма эффективны в отношении раковых процессов, однако, имеют немало опасных побочек вроде сердечной токсичности. Свободные радикалы, образуемые этими препаратами, способны повреждать клеточные структуры миокарда. Поэтому применение средств данной группы требует особого контроля со стороны врача.
Винкаалкалоиды
Это противоопухолевые препараты, имеющее растительное происхождение (на основе экстракта листьев барвинка).
Компоненты этих медикаментов способны связывать тубулин (специфический белок), из которого формируется цитоскелет.
Он необходим клеткам на любой фазе, а его разрушение нарушает хромосомные перемещения при делении, что приводит онкоклетки к уничтожению.
Винкаалкалоиды отличаются еще тем, что злокачественно-аномальные клеточные структуры наиболее чувствительны к винкалкалоидам, нежели нормальные клетки.
Для препаратов винкаалкалоидной группы в качестве побочного эффекта наиболее характерна нейротоксичность. Самыми известными винкаалколоидами являются препараты вроде Виндезина и Винорелбина, Винкристина и Винбластина.
Платина
Препараты платины относится к токсичным тяжелым металлам и воздействует на организм по аналогичному с алкилирующими агентами механизму.
После проникновения в организм компоненты платиновых препаратов начинают взаимодействовать с ДНК молекулами, разрушая их функции и структуры, что вызывает гибель злокачественной клетки.
Среди наиболее применяемых в химиотерапии препаратов платины можно выделить:
- Цисплатин (особенно используется при раке яичек и легкого), но он часто вызывает почечные повреждения;
- Карбоплатин – это второе поколение платиновых препаратов, имеет значительно меньший токсический эффект на почечные структуры;
- Оксалиплатин – представитель третьего поколения, наиболее эффективен при толстокишечном раке, он не токсичен для почек, но способен вызывать невропатии.
Цитостатики
Эти препараты обладают комбинированным механизмом действия, схожим с уже описанными медикаментозными средствами. Некоторые из них похожи на алкилирующие агенты (к примеру, Дакарбазин и Прокарбазин).
Есть цитостатики, действующие по аналогии с антиметаболитами (Гидроксимочевина). Отличными цитостатическими свойствами наделены и кортикостероидные препараты, часто применяющиеся в противораковой терапии.
К часто применяемым цитостатикам относят препараты вроде Апецитабина, Таксола и пр.
Таксаны
Это медикаментозные средства, воздействующие на микротрубочки, имеющиеся в каждой клеточной структуре. В результате происходит нарушение процессов клеточного деления и дальнейшая гибель клеток.
К подобной группе противоопухолевых препаратов относят: Доцетаксе, Паклитаксел и пр.
Таксаны имеют достаточно широкий спектр применения: при раке легкого и молочной железы, простаты и головы, пищевода и пузыря, а также при яичниковых и желудочных злокачественных онкопатологиях. Самой характерной побочной реакцией таксанов считается снижение количества кровяных клеток.
Препараты последнего поколения
Исследование противораковой активности различных веществ продолжаются.
Выходят противоопухолевые препараты новых поколений, обладающие большим терапевтическим эффектом и меньшим числом побочных токсических реакций.
К таким средствам относятся:
Все чаще специалисты стараются использовать таргетную химиотерапию, предполагающую использование препаратов последнего поколения.
Кселокс химиотерапия: схема
Химиотерапия по схеме Кселокс предполагает пероральный прием препарата Кселода с Оксалиплатином. Подобная схема лечения наиболее эффективна в отношении распространенного рака колоректальной сферы.
Но в последнее время было сделано немало открытий, которые позволили несколько изменить комбинацию Кселокс. Обычно она применяется для лечения метастазирующего кишечного рака, ярко выраженной желудочной и молочножелезистой злокачественной онкологии.
Обновленное химиотерапевтическое лечение по схеме XELOX дает пациентам новые возможности, ведь при добавлении к полихимиотерапии Оксалиплатиной и Кселодой препарата Авастин показатели выживаемости заметно повышаются, а прогрессирование онкопатологии отсутствует.
Средства для восстановления
Поскольку химиотерапия сопровождается массой побочных эффектов, а раковые процессы сильно подрывают здоровье, то после противоракового лечения необходимо помочь организму в восстановлении.
Для этого онкопациентам назначаются традиционные медикаменты и фитопрепараты. Каждому больному схема восстановительного лечения подбирается индивидуально.
Обычно восстановительная терапия назначается уже во время химиотерапии или сразу после нее, чтобы снизить выраженность побочной симптоматики и исключить поражения внутриорганических структур от токсического воздействия противораковых средств.
Повышения лейкоцитов
Поскольку на фоне химиотерапевтического лечения происходит угнетение кроветворных функций, то число кровяных клеток значительно снижается, в т. ч. и лейкоцитов.
У всех пациентов, прошедших химиотерапевтический курс лечения развивается лейкопения, сопровождающаяся критически низкими показателями иммунного статуса.
Поэтому таким больным крайне важно нормализовать лейкоцитарный уровень.
В норме уровень лейкоцитов составляет порядка 4-9 х 10 9 /л, однако, после противораковой терапии они сокращаются впятеро.
Иммунитет патологически понижен, а ведь он так необходим для дальнейшего противостояния злокачественным опухолевым процессам. Для восстановления прежнего уровня лейкоцитов пациентам назначаются препараты вроде Имунофала или Полиоксидония.
При их неэффективности показаны более мощные препараты, например, Батилол, Лейкоген, Цефарансин, Метилурацил и пр. Кроме того, повышение лейкоцитов достигается путем экстракорпоральной фармакотерапии, предполагающей введение лекарственных препаратов в кровоток совместно с вливанием донорских эритроцитов.
Печень
На печеночные структуры в ходе химиотерапевтического лечения ложится серьезная нагрузка, ведь противоопухолевые препараты разрушают и здоровые структуры. В организме скапливаются токсины, вывод которых осуществляется печенью.
Для восстановления печени пациентам назначают гепатопротекторные препараты вроде:
Чтобы скопившиеся в печени токсины скорее выводились, рекомендуется обильно и часто пить различные жидкости: отвар шиповника, воду, клюквенный морс и пр.
Иммунитет
У всех пациентов вследствие пониженного иммунитета развиваются инфекционные процессы, а имеющиеся в организме условно-патогенные микроорганизмы приобретают болезнетворный статус. Поскольку организм подвергается общему токсическому воздействию, развиваются инфекции грибкового характера.
По статистике, 100% больных сталкиваются с кандидозом, нередко их беспокоят и стафилококковые инфекции, которые приводят образованию воспалительных и некротических очагов, тромбозов, кровотечений и сепсиса.
Отсутствие необходимого восстановительного лечения в большинстве случаев заканчивается летально. Поэтому столь важное значение имеет поддержка иммунитета с помощью таких препаратов, как Полиоксидоний и Антиокс. Также назначаются биоактивные иммуномодуляторы Биск, Нутримакс, Урсул и пр.
Лекарства от побочек
Химиотерапия сопровождается массой побочных реакций вроде анемии и тошноты, облысения и ломкости ногтей, вкусовых изменений и проблем с аппетитом, желудочно-кишечных расстройств и задержки жидкости, мочеиспускательных нарушений и пр.
Поэтому для облегчения состояния больным назначаются дополнительные препараты для купирования побочной симптоматики.
Таблетки от тошноты
Обычно причиной появления тошноты являются токсины, которые выделяются при распаде раковой опухоли и поступают в организм с химиотерапевтическими препаратами. Это нормальная реакция организма.
Для облегчения тошнотного синдрома назначаются специальные препараты вроде:
Также сократить тошноту помогут лекарства вроде Вистарила, Компазина и Торекана.
Лучше остановить выбор на ректальных суппозиториях, поскольку они напрямую всасываются через кишечную слизистую, не вызывая дополнительного раздражения желудка. Наиболее эффективными свечами являются Компазин и Китрил.
Противорвотное средство
Поскольку онкопациентов после химиотерапии мучает не только тошнота, но и рвота, то им назначаются и противорвотные препараты.
Особенно сильная рвота наблюдается после препаратов цитостатической группы вроде Цисплатина. При введении этого препарата у всех больных отмечалась рвота до 20 раз за сутки.
Для подавления острой рвоты, которая возникает в первые сутки после химиотерапии, показан прием Трописетрона, Гранисетрона либо Эметрона, Доласетрона или Ондасетрона. Также назначаются противорвотные средства: Лоразепам, Маринол, Галоперидол и пр.
Витамины при онкологии
После химиотерапии организму необходимы витамины. Лучше всего их получать из натуральных источников, поскольку в процессе восстановления после химиотерапевтического лечения запрещено принимать поливитаминные комплексы, как правило, содержащие витамины В группы, а именно – В 6 , В 2 и В 1 , которые способствуют росту злокачественных онкоклеток.
А вот витаминами вроде токоферола (Е), аскорбиновой кислоты, ретинола (А) и витамина D организм после химиотерапевтического лечения необходимо обогащать. Их можно принимать в форме препаратов или употреблять в пищу богатые ими продукты.
Противоязвенный препарат Омез часто назначается пациентам после химиотерапии.
Целью подобного назначения является защита желудочных структур от побочных реакций токсических противораковых препаратов.
Препарат обычно назначается дня за 3 до химиотерапии, его прием продолжается в течение недели после лечения.
Гептрал
Гептрал является сильным гепатопротекторным препаратом, предназначенным для защиты печени. Его часто назначают пациентам после химиотерапии в составе восстановительного лечения.
Гептрал нормализует метаболические процессы в печеночных тканях и стимулирует восстановление гепатоцитов.
Препарат принимают в таблетированной форме между пищеприемами. Суточная дозировка составляет 2-4 капсулы или 0,8-1,6 г. Если после химиотерапии пациент переживает тяжелые формы холестаза, то Гептрал назначается в инъекционной форме.
Реабилитация после химии в домашних условиях
Реабилитационный период после химиотерапии сопровождается достаточно широким спектром осложнений, наиболее распространенными среди которых являются энтеропатические поражения и тошнотно-рвотный синдром, алопеция и снижение иммунитета.
Энтеропатия возникает на фоне скопления токсических веществ, проникающих в организм вместе с химиотерапевтическими препаратами.
Полисорб
Выпускается препарат в форме белого порошка диоксида кремния. Его принимают внутрь в суспензионной форме, предварительно растворив порошок в воде. Действующее вещество проникает в ЖКТ, где находятся самые большие токсические скопления.
Молекулы Полисорба связывают токсины и выводят их с каловыми массами. Причем сам диоксид кремния не накапливается в организме и не нарушает обменные и пищеварительные процессы.
Энтеросгель
Препарат производится в форме пасты, которая уже готова к применению. Обычно препарат назначается сроком на 1-2 недели. Принимать его нужно трижды за сутки примерно за пару часов до пищеприема или приема лекарств.
Разовая доза составляет 15 г. Если последствия после химиотерапевтического лечения тяжелые, то допускается увеличение дозировки вдвое, но только на первые 3 дня приема, затем ее постепенно сокращают до нормы.
Отзывы
Кто сталкивался с подобным лечением, наверняка, вздрагивает при одном только слове химиотерапия. Первой мне проводили красную химиотерапию, самую убойную. После нее я полностью лишилась волос, причем на всем теле и лице. Кроме того, постоянно тошнило и рвало, нарушилась двигательная координация, появились ЖКТ проблемы и много чего еще. В моем случае целью химиотерапии, к сожалению, является максимально возможное продление жизни, поскольку вылечиться я уже не смогу. У меня слишком слабый организм, поэтому теперь я прохожу химиотерапевтические курсы препаратами в таблетках (Капецитабин, Кселода, Тутабин + гормонотерапия). Процедура очень тяжелая, но без нее никак нельзя выжить.
Когда у меня обнаружили РШМ, для меня это буквально шоком стало. Никак не ожидала, что в моем возрасте, мне 39, можно столкнуться с таким заболеванием. Онколог предложил химиотерапию платиной. Наслушавшись рассказов об этом жутком лечении, я приготовилась к самому худшему, но после укола совершенно не было недомоганий, остался прежний аппетит, а тошноты и рвоты, как ни странно не было совсем. Прошла уже два курса с месячным перерывом. Начали выпадать волосы, кровь стала совсем никакой, как и иммунитет, но обещанных проблем с желудком и кишечником, к счастью, так и не было. Осталось еще 2 курса. Надеюсь на лучшее, но поживем – увидим.
Цена лекарств
Цены на химиотерапевтические препараты достаточно разные и зависят от группы и поколения медикамента.
- Винбластин – от 145 рублей;
- Винкристин – от 100 рублей;
- Винорельбин – от 6914 рублей.
- Митомицин – от 4250 рублей;
- Эпирубицин – от 280 рублей.
- Адрибластин – от 230 рублей;
- Заведос – от 2800 рублей;
- Циклофосфамид – от 20 рублей;
- Доксорубицин – от 100 рублей.
- Метотрексат – от 99 рублей;
- Фторурацил – от 260 рублей;
- Кселода – от 2380 рублей;
- Меркаптопурин – от 860 рублей;
- Цитарабин – от 720 рублей;
- Фторафур – отрублей.
- Цисплатин – от 140 рублей;
- Карбоплатин – от 430 рублей;
- Оксалиплатин – от 1210 рублей.
Цена на химиотерапевтические препараты может изменяться в зависимости от производителя, аптеки, в которой он продается, от объема и формы выпуска медикамента. Выше приведены лишь примерные цены.
Как делают химиотерапию
Мое общение с людьми выявило, что большинство на вопрос как делают химиотерапию, дают только один ответ: “Капают лекарство”. Дальше этой невнятной формулы познания не идут. По этой причине пришлось провести поиск нужной информации и вот что из этого получилось.
Почему химиотерапия проводится по-разному?
Химиотерапия может быть проведена по-разному, в зависимости от типа рака, который у вас диагностирован и используемых химиопрепаратов:
- Чаще всего химиотерапия проводится с помощью инъекции в вену (внутривенно). Это вариант известен как внутривенная химиотерапия.
- Некоторые препараты представлены в виде таблеток или капсул (перорально).
- Некоторые препараты вводятся в мышцы (внутримышечно).
- Часть препаратов могут быть введены под кожу (подкожные инъекции).
Препараты, применяемые в вышеуказанных способах, всасываются в кровь и распространяются по всему телу, чтобы они могли добраться до всех раковых клеток. Для некоторых типов рака, химиотерапия может быть реализована введением препарата в жидкость вокруг позвоночника. Этот способ известен как интратекальная химиотерапия.
Иногда проведение химиотерапии может касаться ограниченных полостей тела, например, полости малого таза и мочевого пузыря: этот способ известен как внутрирезонаторная химиотерапия. Препараты, применяемые в данном варианте, имеют тенденцию оставаться в той области, в которую они введены и не влияют на клетки в других частях тела. Химиотерапия с помощью кремов может быть использована для некоторых видов рака кожи: она влияет только на клетки в области кожи, на которую наносят крем. Иногда два или более типов химиотерапии можно использовать вместе. Например, внутривенная и пероральная химиотерапии.
Внутривенная химиотерапия
Есть четыре способа введения химиотерапевтических препаратов непосредственно в вену. Для этого используются следующие приспособления:
- Канюля - небольшая трубка, которая вводится в вену на руке или тыльной стороной ладони.
Канюля
Медсестра или врач ставит короткую, тонкую трубку (канюля) в вену с тыльной стороны ладони или предплечья. Вы можете почувствовать неудобство или небольшую боль, но это не будет занимать много времени и боль скоро пройдет. После того, как канюля была введена в нужное место, она будет зафиксирована пластырем и будет надежно держаться на месте. Если боль не проходит после фиксации канюли, можно наложить обезболивающий крем на кожу, чтобы заранее обезболить нужную область. Крем начинает работать черезминут.
Химиотерапевтический препарат может вводиться через канюлю. Обычно капельница прикрепляется к канюле, и некоторые препараты вводятся с помощью инъекции через резиновую пробку капельно. Это может занять от нескольких минут до 20 минут. Некоторые химиотерапевтические препараты разводят в специальном мешочке, и тонкая трубка из него прикрепляется к канюле. Этот вариант может занимать от 20 минут до нескольких часов, а иногда дней. Если вы чувствуете дискомфорт или заметите изменения в ощущениях, покраснение или припухлость вокруг области канюли (или вдоль вашей руки) в то время как вводится препарат, необходимо незамедлительно дать знать вашей медсестре или врачу.
Центральные линии (туннель центрального венозного катетера)
Центральная линия является длинной, тонкой пластиковой трубкой, которая вводится в вену на груди. Наиболее распространенные типы линий - Hickman® или Groshong®. Врач или медсестра химиотерапевтического отделения объяснит вам суть процедуры. Вам будет предоставлена общая или местная анестезия перед установкой центральной линии.
После того, как трубка находится в месте, ее приклеивают липкой лентой к груди накрепко, чтобы ее нельзя было вытащить из вены. Она может остаться в вене в течение многих месяцев и это предполагает, что вы не должны использовать канюли, поскольку у вас есть своя внутривенная химиотерапия. С помощью этой трубки можно также взять кровь для тестирования. Вы сможете купаться или принимать душ. Хотя вы должны предотвратить попадание воды в район, где трубка входит в кожу. Для этого можно использовать пластиковую повязку. Для использования в повседневной жизни ограничений мало. Внимательно следите за состоянием трубки.
Существуют две потенциальные проблемы с центральными линиями: закупорка и инфекция. Один или два раза в неделю линия должна быть промыта гепарином, препаратом, который предотвращает свертывание. Ваша медсестра может научить вас, как это сделать.
Если вы заметили покраснение, потемнение или болезненность кожи вокруг центральной линии, или если у вас появилась высокая температура, сообщите врачу, поскольку это может быть признаком того, что у вас есть инфекция в линии. Если произошел такой случай, необходимо будет ввести антибиотики через линию, чтобы устранить инфекцию.
Врач и медсестра вашей больнице подскажет вам, какая температура допустима.
PICC линии
Ваш врач может предложить вам ввести в вену на сгибе руки длинную, тонкую трубку. Это называется периферийно установленный центральный венозный катетер (PICC). Ваш врач или медсестра из химиотерапевтического отделения объяснит вам назначение этой процедуры. Вам будет предоставлена местная анестезия перед установкой катетера.
После того, как он находится на месте, линия PICC накрепко прикрепляется к руке, чтобы предотвратить его вытаскивание из вены. Он может остаться в вене в течение многих месяцев. Как с центральной линией, это означает, что вы не должны иметь вставленные канюли, когда у вас есть свой внутривенный ввод химиопрепаратов. Через этот катетер также может быть взята кровь для тестирования. Вы должны будете сгибать руку, если надумаете принимать душ. В любом случае вы должны избегать попадания воды на область вокруг трубки. Для этого может быть использована любая пленка.
принципе вставленный катетер не налагает особых ограничений в повседневной жизни. Перед тем, как идти домой, убедитесь, что вы уверены в крепости прикрепления катетера. В ходе лечения медсестра может промыть катетер и сменить повязку, или эту процедуру можно научит делать друга или родственника.
Возможные проблемы с PICC линий такие же, как для центральных линий: закупорки и инфекции.
Имплантируемый порт (Portacath)
Имплантируемый порт представляет собой тонкую, мягкую пластиковую трубку, которая вводится в вену и заканчивается отверстием (порт) под кожей на груди или руке. Порт имеет тонкий резиновый диск, через который может вставляться игла, чтобы ввести лекарство в вену или взять кровь.
Трубка длинная, тонкая полая, еще называемая катетер и порт, который представляет собой диск от 2,5 до 4 см в диаметре. Катетер обычно вставляется (туннель) под кожу груди. Кончик катетера помещают в большую вену чуть выше сердца, а другой конец соединяется с портом, который располагают под кожей на верхней части грудной клетки. Порт будет ощущаться как маленький бугорок под кожей, но снаружи на теле не будет ничего видно. Возможные проблемы такие же, как для центральных линий: закупорки и инфекции.
Инфузионные насосы
Инфузионные насосы могут быть использованы, чтобы дать некоторые виды химиотерапии. Существуют различные типы портативных насосов. Они дают контролируемое количество химиотерапевтического препарата в кровоток в течение определенного периода времени (от нескольких дней до нескольких недель). Инфузионный насос соединен с центральной линией или линией PICC. Это означает, что вы можете идти домой с насосом, при этом вам можно реже посещать больницу. Насос достаточно мал, чтобы поместиться в карман и может располагаться в сумке или на ремне.
Химиотерапевтические препараты готовятся в больнице. Вы, и, возможно, член семьи или друг, научатся ухаживать за насосом. Некоторые насосы с батарейным питанием и уход должен быть правильным, чтобы не замочить их, если вы, например, стираете белье. Ваши медсестры или аптечный персонал дадут вам подробные инструкции. Некоторые насосы одноразовые.
Химиотерапия в таблетках
Вам может быть назначена химиотерапия в таблетках, которые можно принимать у себя дома, как все или часть вашего лечения. Препарат может быть не только в таблетках, но и в капсулах. Таблетки или капсулы, известны как пероральная химиотерапии. Вам скажут, когда их приобрести и будут даны другие указания, такие как, стоит ли принимать их с пищей. Если вы не можете принимать лекарства по любой причине, вы должны немедленно обратиться к врачу за советом. Препараты, которые вам дали в больнице составляют полный курс лечения, и важно, чтобы взять их именно так, как они были предусмотрены. Всегда читайте этикетки на коробках, прежде чем покинуть больницу - если инструкции не ясны, попросите медсестру, врача или фармацевта разъяснить вам неясные моменты.
Если вам нужны дополнительные поставки химиотерапевтических препаратов или других медикаментов, важно получить их от вашего специалиста из больницы, а не от вашего лечащего врача или местного фармацевта.
Внутримышечные инъекции
Возможно проведение химиотерапии и достаточно привычным путем. Некоторые химиотерапевтические препараты вводятся с помощью инъекции в мышцу. Врач или медсестра объяснить процедуру вам. Препарат вводится в мышцы ноги или ягодицы. Это может быть болезненным или неудобным, но действует только в течение короткого времени.
Подкожные инъекции
Некоторые препараты могут быть введены в виде инъекций под кожу. Очень тонкой иглой, и это может быть неудобным в течение короткого времени.
Внутрирезонаторная химиотерапия
При этом типе химиотерапии, чтобы ввести химиотерапевтический препарат, в полость пораженного органа (например, мочевой пузырь) вставляется трубка. Через вставленную трубку доставляется химиотерапевтический препарат. Препарат может быть залит один раз в течение заданного периода времени. Препараты, применяемые в этом случае, могут вызывать раздражение или воспаление в области, в которую они введены, но они не имеют тенденцию вызывать побочные эффекты в других частях тела.
Интратекальное введение (в жидкость вокруг спинного мозга)
В некоторых условиях, таких как лейкемия или лимфома (рак, который начинается в лимфатической системе) раковые клетки могут пройти в жидкость, которая окружает мозг и спинной мозг. Жидкость известная как спинномозговая жидкость или CSF. Чтобы предотвратить развитие онкологии, или лечить ее, если развитие уже произошло, химиотерапевтический препарат может быть введен в CSF. Для этого вы, как правило, должны лечь на бок с сомкнутыми ногами. Врач будет использовать местную анестезию, чтобы обезболить область кожи над позвоночником. Игла вставляется в пространство между двух позвонков и достигает спинномозговой жидкости. Химиотерапевтический препарат вводят в спинномозговую жидкость через иглу.
Эта процедура занимает от 15 до 30 минут, и вы, возможно, должны лежать после нее в течение нескольких часов. Важно пить много жидкости, чтобы уменьшить шансы получить головную боль. Если вы получите головную боль, она может длиться в течение нескольких часов. Чтобы облегчить состояние могут быть даны обезболивающие. Химиотерапия, приведенная для этого случая обычно не вызывает никаких других побочных эффектов.
Химиотерапия Кремы
Химиотерапия кремами используется для некоторых видов рака кожи. Крем наносится на пораженный участок кожи тонким слоем и, возможно, его потребуется использовать регулярно в течение нескольких недель. Кремы могут вызвать некоторые болезненные ощущения или раздражение кожи в зоне воздействия, но не вызывают побочных эффектов в других частях тела. В то время как вы используете химиотерапию кремами, вам может понадобиться наложение специальной повязки на пораженном участке кожи для постоянного ношения.
Вот как делают химиотерапию при различных формах рака. Теперь вы знаете к чему готовиться и какие вопросы задать, если что-то вдруг непонятно.
Возможно вам эти статьи будут полезны
В списке открытий 2013 года вакцина от рака
Метод Шевченко водка с маслом
Проблемы со сном (бессонница) при раке
Онкология и мифы 2
7 комментариев
Как никто другой я знакома с этой процедурой из-за болезни сестры. У нее рак молочной железы, боремся уже 10 лет.Три года назад уже переживали 4 курса химиотерапии, но сейчас все гораздо сложнее. Разумеется, что все курсы разные в зависимости от типа рака и от степени запущенности заболевания. Сестре назначена полихимиотерапия и препарат против метастаз в костях. Лечение проходит через капельницы. Соседка по палате с циррозом печени принимает лечение в таблетках.
Технология проведения химиотерапия просто поражает воображение. Что касается внутримышечных и подкожных инъекций то, как и любой укол в той или иной мере болезненный. Химиотерапия в таблетках, использование всевозможных кремов - это не сложно, главное следовать предписаниям врача. Ну а внутривенная терапия вообще доставляет пациенту массу неприятных и болезненных ощущений. Как можно вести мало-мальски нормальный образ жизни, если в тебя ввели длинные трубки и катетеры. Интратекальное введение - это по моему самый болезненный способ введения препаратов. И хотя оно не вызывает побочных эффектов, однако я думаю что не каждый больной в силе это стерпеть, в особенности дети.
У моего друга отец болел, царство ему небесное… В то время интернет не был так развит как сейчас, вот вы в одной статье описали все, и все вроде как понятно. Я проходил курсы фармацевтов для устройства на работу. Естественно нам там много что могли объяснить и дать в столь сжатые сроки.
Знаю лишь одно - любая химия убивает как раковые так и живые клетки организма. При идеальном здоровье печени и высоком иммунитете она дает многим отсрочку, а то и шанс на выздоровление. Но не имея этого человеку остается лишь надеяться, надеяться дескать на авось.
Еще будучи студенткой медицинского колледжа нам много рассказывали о технологии проведения химиотерапии. Даже на практике немного видели данную процедуру. Видели метод внутривенной химиотерапии. Также нам рассказывали,что зачастую применяют в таблетках. Здесь же я увидела новые для себя методы, ранее с ними не была знакома. Очень познавательно. Я приму эту статью на заметку ведь в моей работе она очень пригодится.
Статья немного приоткрыла завесу тайны и погрузила «по ту сторону» лечения онкологии.
Я не переживала сама это заболевание, но среди родственников многие умерли от рака.
К сожалению, химиотерапия не всегда помогает, особенно на поздних стадиях, когда уже идут метастазы. Да и крутит после нее ужасно: слабость в мышцах, ломота в теле, не говоря уже о всем известном выпадении волос.
Для меня вообще не секрет, что при регулярных инъекциях ставят катетер, чтобы постоянно не колоть человека, но многие удивляются, узнав даже о подключичных катетерах, не говоря уже о подкожных портах 🙂
У меня 4 степень рака кишечника, так химиотерапевты не стали класть меня в стационар под капельницу, а ведь всё уже было готово. У вас ишемия и мы не хотим, чтобы вы умерли на столе. Вот вам 6 курсов таблеток капецитабина, проверки узи на старых компах и рентген грудной клетки(1 раз в 3 месяца после операции). Кровь с мочой от меня требует только моя участковая врач, разбирает там что-то, объясняет, утешает. Врачи в поликлинике онкоцентра (республиканского) с нашими пациентами вообще не разговаривают: они там что-то пишут на компьютере себе одно и то же, а пациентам все разъясняют медсестры, если снизойдут, часто путают назначения по датам и мн. др. Разве так должно проходить лечение химией, да еще проблема с таблетками: достанутся - не достанутся, а для этого надо пройти МСЭК и стать инвалидом, а это такая волокита….Сейчас у меня 5-й курс, потом 6-й. Мой вопрос: что будет дальше, какие процедуры обязаны назначить, какие желательно назначить, но по мере возможности?
Уважаемая Алла! Не знаю в каком Вы возрасте, но так или иначе скажу несколько слов.
Прежде всего, ответить на ваш вопрос о дальнейших действиях ваших врачей нет возможности. Процедуры, как правило, стандартизированы для каждого конкретного онкологического центра. Когда я изучал этот вопрос, мне показалось, что стандартизация проходит на основе имеющейся команды онкологов и их квалификации, но не относительно текущей региональной ситуацией с заболеваемостью раком, типами рака, которые наиболее прогрессируют в регионе и т.д.
Вы должны понимать, что, получив 4-ю стадию, можно вести разговор только об увеличении срока выживаемости. Полное излечение с большой вероятностью не состоится. Но вот за выживаемость на мой взгляд можно побороться. Как боролась та женщина, о которой я писал в одной из статей. Которой онкологи отмерялимесяца, а она прожила полтора года общаясь со мной (причем активной жизнью) и после уверовав в себя, отошла от меня. Дальнейшую судьбу ее не знаю.
Так вот. Прочитайте материалы сайта. Прочитайте важную статью по ссылке
и займитесь собой сами. Никакой онколог не будет воспринимать вашу проблему как свою!
детоксикация канцерогенных веществ. Я бы рекомендовал «Кору муравьиного дерева». Мы это с той женщиной прошли.
Можно еще какие-либо вещества включить, но Кора, на мой взгляд, имеет исключительные способности.
Диета - важнейший момент, тем более при вашем виде рака. Категорически исключите из потребления красное мясо. Можно употреблять куриное мясо. Больше овощей, фруктов. Скажете зима.. Капуста есть всегда, корень сельдерея, ну и так далее. Не килограммами, а немножко того, немножко другого. Обязательно сушеные зерна абрикоса и миндаля. Дорого? Да. Но ведь в день достаточно позернышек. Не знаю ваши цены, но по нашим это около 200 рублей в месяц. О диете можно писать много, да и на сайте я писал. Поищите.
Займитесь медитациями. Найдите в интернете информацию и то, что вам подойдет пробуйте. Главное успокоить себя.
И главное! Физические упражнения. Поймите, что, если Вы будете лежать и глотать таблетки, то большинство ваших мышц начнут приходить в дряблое состояние и далее атрофироваться, фактически отмирать за ненадобностью. Все это скажется и на жизненной функции. Ваш организм подумает, что пора ликвидироваться и так и произойдет. Нужно бороться (при желании). Найдите сначала простую форму физических упражнений. Например бодифлекс. На ютьюбе много курсов. Найдите и потихоньку начните их выполнять. Через неделю Вы почувствуете прилив энергии. Кислород начнет пожирать раковые клетки (это доказано давно и даже вручена Нобелевская премия).
Copyright ©17 Рак излечим
Научный центр терапии рака Венского университета и MedUni Vienna получили новые данные о лечении рака химиотерапией на основе платины. Этот метод давно используется в медицине, но считалось, что его применение приводит к повреждению иммунной системы. Был отмечен цитотоксический эффект повреждения здоровых клеток.
Однако, последние исследования выявили, что химиотерапия с платиной делает раковые клетки более видимыми для лейкоцитов и борьба происходит эффективнее.Пациенты с раком легких, которые получали химиотерапию на основе платины, с большей вероятностью выживали через 6, 12 и 24 месяца после лечения по сравнению с пациентами, которые получали лечение не на основе платины. Плоскоклеточный рак легких и другие его виды являются одной из причин смерти от онкологии во всем мире. Ежегодно умирают 1,76 млн. человек. Поэтому так важно найти наиболее эффективные методы лечения для пациентов с этим заболеванием.
Химиотерапия на основе платины показала более высокую частоту полного ответа опухоли (полное исчезновение опухолей, по крайней мере, в течение определенного периода времени после лечения) по сравнению с химиотерапией не на основе платины. Недостаток терапии состоит в том, что она чаще вызывала некоторые побочные эффекты, включая тошноту и рвоту, а также низкий уровень тромбоцитов. Эти явления не опасны, но снижают качество жизни больных.
Вальтер Бергер, заместитель руководителя Венского института онкологических исследований MedUni считает, что будущее лечения рака за комбинацией иммунотерапии с химиотерапией на основе платины. Злокачественная опухоль разрастается после проигрыша иммунной системы при активизации раковых клеток. Новообразование ослабляет организм и тормозит лечебное действие лейкоцитов, которые не могут распознать чужеродные агенты. Лейкоциты перестают обнаруживать переродившиеся клетки и прекращают борьбу.
Химиотерапия с платиной разрушает раковые клетки и как бы делает их видимыми для лейкоцитов. Происходит самообновление иммунной системы, которая начинает активно бороться с болезнью. Раковые клетки склонны к мутации, но активировавшиеся лейкоциты уже способны распознать и новые разновидности. Если подкрепить химиотерапию иммунокрректорами, то лечение будет более эффективным.
Несмотря на побочные эффекты, применение химиотерапии с платиной в комбинации с препаратами для усиления иммунного ответа считается теперь перспективной методикой для борьбы с онкологией. Именно комбинированная терапия дает больным шансы на выживаемость даже с метастазами.
Целью проводимых исследований является повышение успешности лечения, в то же время, уменьшая или лучше контролируя любые связанные побочные эффекты. В долгосрочной перспективе ожидается, что комбинированная терапия вылечит большинство пациентов или, по крайней мере, приведет к долгосрочной ремиссии.





