Eeter perioodilisustabelis
Ametlikult koolides ja ülikoolides õpetatav keemiliste elementide perioodilisustabel on võlts. Mendelejev ise esitas oma teoses “Maailma eetri keemilise mõistmise katse” veidi teistsuguse tabeli (Polütehniline muuseum, Moskva):

Viimati, moonutamata kujul, nägi tõeline perioodilisustabel valgust 1906. aastal Peterburis (õpik "Keemia alused", VIII väljaanne). Erinevused on nähtavad: nullrühm viiakse 8. kohale ja vesinikust kergem element, millega tabel peaks algama ja mida tinglikult nimetatakse njuutooniumiks (eeter), on üldiselt välistatud.

Samas lauas on jäädvustatud "verine türanni" kamraad. Stalin Peterburis, Moskovski pst. 19. VNIIM neid. D. I. Mendelejeva (Ülevenemaaline metroloogia uurimisinstituut)
Monument-tabel Keemiliste elementide perioodiline süsteem D.I. Mendelejev valmistas mosaiiki Kunstiakadeemia professori V.A. juhendamisel. Frolov (Kritševski arhitektuurne disain). Monument põhineb tabelil, mis on pärit D.I. raamatu „Fundamentals of Chemistry“ 8. väljaandest (1906). Mendelejev. D.I elu jooksul avastatud elemendid. Mendelejev on märgitud punasega. Aastatel 1907–1934 avastatud elemendid , on tähistatud sinisega. Monumendi-laua kõrgus on 9 m, üldpind 69 ruutmeetrit. m
.jpg)
Miks ja kuidas see juhtus, et meile nii avalikult valetatakse?
Maailmaeetri koht ja roll D.I tõelises tabelis. Mendelejev
1. Suprema lex – salus populi
Paljud on kuulnud Dmitri Ivanovitš Mendelejevist ja tema poolt 19. sajandil (1869) avastatud "keemiliste elementide omaduste muutumise perioodilisest seadusest rühmade ja seeriate kaupa" (tabeli autori nimi on "Elementide perioodiline tabel". rühmade ja seeriate kaupa”).
Paljud kuulsid ka, et D.I. Mendelejev oli Venemaa Keemia Seltsi (alates 1872. aastast Venemaa Füüsikalis-Keemia Selts) korraldaja ja alaline juht (1869-1905), mis kogu oma eksisteerimise ajal andis kuni kuni aastani välja maailmakuulsat ajakirja ZhRFKhO. NSV Liidu Teaduste Akadeemia likvideerimine 1930. aastal – nii Selts kui ka selle ajakiri.
Kuid vähesed neist, kes teavad, et D.I. Mendelejev oli 19. sajandi lõpu üks viimaseid maailmakuulsaid vene teadlasi, kes kaitses maailmateaduses eetri kui universaalse substantsiaalse entiteedi ideed, andes sellele fundamentaalse teadusliku ja rakendusliku tähtsuse olemise saladuste paljastamisel ja inimeste majanduselu parandamine.
Veel vähem on neid, kes teavad, et pärast D.I äkilist (!!?) surma. Mendelejev (27.01.1907), keda tunnustasid tollal silmapaistvaks teadlaseks kõik teadusringkonnad üle kogu maailma, välja arvatud ainuüksi Peterburi Teaduste Akadeemia, tema peamist avastust – "perioodilist seadust" – võltsis maailm teadlikult ja kõikjal. akadeemiline teadus.
Ja väga vähesed teavad, et kõike eelnimetatut ühendab nii surematu vene füüsilise mõtte parimate esindajate ja kandjate ohverduslik teenimine rahvaste hüvanguks ja avalikuks hüvanguks, hoolimata kasvavast vastutustundetuse lainest. tolleaegses ühiskonna kõrgemates kihtides.
Sisuliselt on käesolev doktoritöö pühendatud viimase teesi igakülgsele arendamisele, sest tõsiteaduses viib igasugune oluliste tegurite tähelepanuta jätmine alati valetulemusteni. Seega on küsimus: miks teadlased valetavad?
2. Psy-faktor: ni foi, ni loi
Alles nüüd, alates 20. sajandi lõpust, hakkab ühiskond praktiliste näidete varal (ja ka siis pelglikult) aru saama, et silmapaistev ja kõrge kvalifikatsiooniga, kuid vastutustundetu, küüniline, ebamoraalne teadlane, kellel on “maailma nimi” inimestele vähem ohtlik kui silmapaistev, kuid ebamoraalne poliitik, sõjaväelane, advokaat või parimal juhul "väljapaistev" bandiit maanteelt.
Seltsi inspireeris idee, et maailma akadeemiline teaduskeskkond on taevaste, munkade, pühade isade kast, kes päeval ja öösel küpsetab rahvaste hüvanguks. Ja lihtsurelikud peaksid oma heategijatele lihtsalt suhu vaatama, alandlikult rahastades ja ellu viima kõiki oma “teaduslikke” projekte, prognoose ja juhiseid oma avaliku ja eraelu ümberkorraldamiseks.
Tegelikult ei ole maailma teadusringkondades kriminaal-kuritegelikku elementi vähem kui samade poliitikute keskkonnas. Lisaks on poliitikute kuritegelikud, asotsiaalsed teod enamasti kohe nähtavad, kuid "prominentsete" ja "autoriteetsete" teadlaste kuritegelikku ja kahjulikku, kuid "teaduslikult põhjendatud" tegevust ei tunnusta ühiskond kohe, vaid aastate möödudes. või isegi aastakümneid. , omal "avalikul nahal".
Jätkame selle ülimalt huvitava (ja salajase!) teadustegevuse psühhofüsioloogilise teguri (nimetame seda tinglikult psi-teguriks) uurimist, mille tulemusena saadakse tagantjärele ootamatu (?!) negatiivne tulemus: „meie. tahtis inimestele parimat, aga selgus nagu alati, need. kahjuks." Tõepoolest, teaduses on negatiivne tulemus ka tulemus, mis nõuab kindlasti igakülgset teaduslikku arusaama.
Arvestades psi-teguri ja riigi rahastusorgani peamise eesmärgifunktsiooni (MTF) korrelatsiooni, jõuame huvitava järelduseni: möödunud sajandite nn puhas, suur teadus on mandunud puutumatute kastiks, s.t. õukonnaravitsejate kinnisesse kasti, kes valdasid hiilgavalt pettuseteadust, kes valdasid hiilgavalt dissidentide tagakiusamise teadust ja oma võimsatele rahastajatele allumise teadust.
Samas tuleb silmas pidada, et esiteks kõigis nn. "tsiviliseeritud riigid" oma nn. "riiklikud teaduste akadeemiad" on formaalselt riiklike organisatsioonide staatuses vastava valitsuse juhtiva teadusliku ekspertorgani õigustega. Teiseks, kõik need riiklikud teaduste akadeemiad on omavahel ühendatud ühtseks jäigaks hierarhiliseks struktuuriks (mille tegelikku nime maailm ei tea), mis töötab välja kõigi riiklike teaduste akadeemiate jaoks ühise käitumisstrateegia maailmas ja ühtse nn. helistas. teaduslik paradigma, mille tuumaks pole mitte eluseaduste avalikustamine, vaid psi-faktor: teostades nn "teadusliku" katte (kindluse huvides) võimulolijate kõigi silmis ebasobivate tegude. ühiskonnale kui "õukonnaravitsejatele", et omandada preestrite ja prohvetite au, mõjutades demiurgi kombel inimkonna ajaloo liikumise kulgu.
Kõik, mis selles jaotises ülalpool mainitud, sealhulgas meie poolt kasutusele võetud termin "psi-faktor", ennustas D.I. mõistlikult suure täpsusega. Mendelejev enam kui 100 aastat tagasi (vt näiteks tema 1882. aasta analüütilist artiklit “Millist akadeemiat on Venemaal vaja?”, kus Dmitri Ivanovitš kirjeldab tegelikult psi-tegurit ja milles nad pakkusid välja programmi Venemaa Teaduste Akadeemia liikmetest koosneva suletud teaduskorporatsiooni radikaalse ümberkorraldamise eest, kes pidas Akadeemiat üksnes omakasupüüdlike huvide rahuldamiseks.
Ühes oma kirjas 100 aastat tagasi Kiievi ülikooli professorile P.P. Alekseev D.I. Mendelejev tunnistas ausalt, et on "valmis end isegi ära põletama, et kuradit välja suitsetada ehk teisisõnu muuta akadeemia alused millekski uueks, venepäraseks, omaks, mis sobib kõigile üldiselt ja eriti. teadusliku liikumise eest Venemaal.
Nagu näeme, on tõeliselt suur teadlane, kodanik ja oma kodumaa patrioot võimeline ka kõige keerukamate pikaajaliste teaduslike prognooside tegemiseks. Vaatleme nüüd selle psi-teguri muutuse ajaloolist aspekti, mille avastas D.I. Mendelejev 19. sajandi lõpus.
3. Fin de siecle
Alates 19. sajandi teisest poolest on Euroopas "liberalismilainel" toimunud intelligentsi, teadus- ja tehnikapersonali kiire arvuline kasv ning nende poolt pakutavate teooriate, ideede ning teaduslike ja tehniliste projektide kvantitatiivne kasv. personali ühiskonda.
19. sajandi lõpuks tihenes nende seas järsult konkurents “koha pärast päikese all”, s.t. tiitlitele, autasudele ja auhindadele ning selle konkursi tulemusena on süvenenud teaduspersonali polariseerumine moraalsete kriteeriumide järgi. See aitas kaasa psi-teguri plahvatuslikule aktiveerimisele.
Noorte, ambitsioonikate ja põhimõteteta teadlaste ja intelligentsi revolutsiooniline entusiasm, joovastus nende peatsest stipendiaadist ja kannatamatust soovist saada iga hinna eest teadusmaailmas kuulsaks, ei halvanud mitte ainult vastutustundlikuma ja ausama teadlaste ringi esindajaid, vaid kogu kogu. teadusringkond tervikuna koos oma infrastruktuuri ja väljakujunenud traditsioonidega, mis olid varem psi-teguri ohjeldamatu kasvu vastu.
19. sajandi revolutsioonilised intellektuaalid, troonide ja riigikorra kukutajad Euroopa riikides levitasid pommide, revolvrite, mürkide ja vandenõude abil oma ideoloogilise ja poliitilise võitluse bandiitlikke meetodeid "vana korra" vastu) ka teadus- ja tehnikategevuse valdkonda. Õpilaste klassiruumides, laborites ja teadussümpoosionidel naeruvääristati väidetavalt iganenud mõistust, väidetavalt aegunud formaalse loogika kontseptsioone – hinnangute järjekindlust, nende kehtivust. Nii tuli 20. sajandi alguses teadusvaidluste (täpsemalt lõhkemise) moodi veenmismeetodi asemel vastaste totaalne mahasurumine nende vastu suunatud vaimse, füüsilise ja moraalse vägivalla abil. , kisa ja mürinaga). Samal ajal jõudis psi-teguri väärtus loomulikult ülikõrgele tasemele, olles kogenud oma äärmust 1930. aastatel.
Selle tulemusena - 20. sajandi alguses "valgustatud" intelligents, tegelikult sunniviisiliselt, s.o. muutis revolutsioonilisel viisil tõeliselt teadusliku humanismi, valgustuse ja sotsiaalse kasu paradigma loodusteadustes omaenda püsiva relativismi paradigmaks, andes sellele üldrelatiivsusteooria (küünilisuse!) pseudoteadusliku vormi.
Esimene paradigma põhines kogemusel ja selle igakülgsel hindamisel tõe otsimise, objektiivsete loodusseaduste otsimise ja mõistmise huvides. Teine paradigma rõhutas silmakirjalikkust ja hoolimatust; ja mitte objektiivsete loodusseaduste otsimiseks, vaid omakasupüüdlike grupihuvide nimel ühiskonna kahjuks. Esimene paradigma töötas avalikkuse huvides, teine aga mitte.
Alates 1930. aastatest kuni tänapäevani on psi tegur stabiliseerunud, jäädes 19. sajandi alguse ja keskpaiga väärtusest suurusjärgu võrra kõrgemaks.
Maailma teadusringkondade (mida esindavad kõik riiklikud teadusakadeemiad) tegevuse tegelikku ja mitte müütilist panust inimeste avalikku ja eraellu objektiivsemalt ja selgemalt hinnata, tutvustame normaliseeritud kontseptsiooni. psi tegur.
Psi-teguri normaliseeritud väärtus, mis on võrdne ühega, vastab sajaprotsendilisele tõenäosusele saada selline negatiivne tulemus (st selline sotsiaalne kahju) teaduslike arengute juurutamisel, mis kuulutasid a priori positiivseks tulemuseks (st. teatud sotsiaaltoetus) üheks ajalooliseks perioodiks (ühe põlvkonna inimeste vahetus, umbes 25 aastat), mille käigus kogu inimkond sureb või mandub täielikult mitte rohkem kui 25 aasta jooksul alates teatud ploki kasutuselevõtu kuupäevast. teadusprogrammid.
4. Tapa lahkusega
Relativismi ja sõjaka ateismi julm ja räpane võit maailma teadusringkondade mentaliteedis 20. sajandi alguses on kõigi inimkonna hädade peapõhjus sellel niinimetatud "teadusliku" "aatomi", "kosmose" ajastul. ja tehnoloogiline areng". Tagantjärele mõeldes, milliseid tõendeid on meil tänapäeval veel vaja, et mõista ilmselget: 20. sajandil ei olnud loodus- ja sotsiaalteaduste vallas ühtegi ühiskondlikult kasulikku ülemaailmset teadlaste vennaskonda, mis tugevdaks elanikkonda. homo sapiens, fülogeneetiliselt ja moraalselt. Ja on just vastupidi: inimese psühhosomaatilise olemuse, tema tervisliku eluviisi ja keskkonna halastamatu sandistamine, hävitamine ja hävitamine erinevatel usutavatel ettekäänetel.
Üsna 20. sajandi alguses oli kõigil akadeemilistel võtmepositsioonidel teaduse edenemise, teemade, teadus- ja tehnikategevuse rahastamise jms juhtimisel “mõtlejate vennaskond”, kes tunnistas kaksikreligiooni. küünilisus ja isekus. See on meie aja draama.
Just sõjakas ateism ja küüniline relativism on selle pooldajate jõupingutustega need, mis meie planeedil eranditult kõigi kõrgeimate riigimeeste teadvuse mässisid. Just see kahe peaga antropotsentrismi kinnismõte tekitas ja tõi miljonite teadvusesse nn teadusliku kontseptsiooni “aine-energia lagunemise universaalsest printsiibist”, s.o. looduses varem tekkinud – ei tea kuidas – objektide universaalne lagunemine. Absoluutse fundamentaalse olemuse (globaalne sisuline keskkond) asemele pandi pseudoteaduslik energia lagunemise universaalse printsiibi kimäär koos selle müütilise atribuudiga - "entroopia".
5. Littera contra litter
Selliste minevikuvalgustite järgi nagu Leibniz, Newton, Torricelli, Lavoisier, Lomonosov, Ostrogradski, Faraday, Maxwell, Mendelejev, Umov, J. Thomson, Kelvin, G. Hertz, Pirogov, Timirjazev, Pavlov, Bekhterev ja paljud, paljud teised maailm keskkond on absoluutne fundamentaalne entiteet (= maailma substants = maailma eeter = kogu universumi aine = Aristotelese “kvintessents”), mis täidab isotroopselt ja jäljetult kogu lõpmatu maailmaruumi ja on looduses igat tüüpi energia, hävimatute "liikumisjõudude", "tegevusjõudude" allikas ja kandja.
Sellele vastandub praegu maailmateaduses domineeriva idee kohaselt matemaatiline väljamõeldis "entroopia" ja isegi mõningane "teave", mille tõsimeeli kuulutasid maailma akadeemilised valgustid hiljuti nn "entroopiaks". , kuulutati kui absoluutset põhiolemust. "Universaalne põhiolemus", vaevutamata sellele uuele terminile üksikasjalikku määratlust andma.
Eelneva teadusliku paradigma kohaselt valitseb maailmas Universumi igavese elu harmoonia ja kord, läbi pidevate lokaalsete uuenemiste (surmade ja sündide jada) erineva ulatusega üksikute materiaalsete moodustiste.
Viimase pseudoteadusliku paradigma kohaselt liigub kunagi arusaamatul viisil loodud maailm universaalse lagunemise, temperatuuride võrdsustamise universaalse, universaalse surmaga kuristikku teatud maailma superarvuti valvsa kontrolli all, mis omab ja haldab mõnda “ teave”.
Mõned näevad ümberringi igavese elu võidukäiku, teised aga lagunemist ja surma, mida kontrollib mingi Maailma Teabepank.
Nende kahe diametraalselt vastandliku ideoloogilise kontseptsiooni võitlus domineerimise nimel miljonite inimeste teadvuses on inimkonna biograafia keskne punkt. Ja selle võitluse panus on kõrgeim aste.
Ja pole sugugi juhuslik, et kogu 20. sajand on maailma teaduse institutsioon hõivatud kütuseenergia kasutuselevõtuga (väidetavalt ainuvõimalike ja paljutõotavatena), lõhkeainete, sünteetiliste mürkide ja narkootikumide, mürgiste ainete, geenitehnoloogia teooriaga. biorobotite kloonimisega, inimkonna taandarenguga primitiivsete oligofreenikute, mõõnade ja psühhopaatide tasemele. Ja ega neid programme ja plaane praegu isegi avalikkuse eest varjata.
Elutõde on see: maailma mastaabis kõige jõukamad ja võimsamad inimtegevuse valdkonnad, mis loodi 20. sajandil uusima teadusliku mõtte järgi, olid porno, narkootikumide, farmaatsiaäri, relvaäri, sealhulgas globaalne teave ja psühhotroonika. tehnoloogiaid. Nende osakaal kõigis finantsvoogudes globaalses mahus ületab oluliselt 50%.
Edasi. 1,5 sajandit Maa loodust moonutanud ülemaailmne akadeemiline vennaskond kiirustab nüüd Maa-lähedast kosmost koloniseerima ja vallutama, omades kavatsusi ja teadusprojekte muuta see ruum oma "kõrgtehnoloogiate" prügimäeks. . Need härrased-akadeemikud on sõna otseses mõttes pakatavad igatsetud saatanlikust ideest võtta enda kätte päikeselähedases ruumis, mitte ainult Maal.
Seega on ülisubjektiivse idealismi (antropotsentrismi) kivi laotud vabamüürlaste ülemaailmse akadeemilise vennaskonna paradigma ja nende nn. teaduslik paradigma toetub püsivale ja küünilisele relativismile ja sõjakale ateismile.
Kuid tõelise progressi tempo on vääramatu. Ja nagu kogu elu Maal tõmbab Valguse poole, nii tõmbab teatud osa tänapäevaste teadlaste ja loodusteadlaste meelt, keda ei koorma globaalse vennaskonna klannihuvid, igavese elu päikese, igavese liikumise päikese poole. Universum olemise põhitõdede tundmise ja liigi xomo sapiens eksistentsi ja evolutsiooni peamise sihtfunktsiooni otsimise kaudu. Nüüd, võttes arvesse psi-teguri olemust, heidame pilgu Dmitri Ivanovitš Mendelejevi tabelile.
6. Argumentum ad rem
Mida nüüd koolides ja ülikoolides esitatakse nime all "D.I. keemiliste elementide perioodiline tabel. Mendelejev”, on otsene võlts.
Viimati, moonutamata kujul, nägi tõeline perioodilisustabel valgust 1906. aastal Peterburis (õpik "Keemia alused", VIII väljaanne).
Ja alles pärast 96 aastat unustust tõuseb tõeline perioodilisustabel esimest korda tuhast tänu selle väitekirja avaldamisele Venemaa Füüsika Seltsi ajakirjas ZhRFM. Ehtne, võltsimata tabel D.I. Mendelejev "Elementide perioodiline tabel rühmade ja seeriate kaupa" (D. I. Mendelejev. Keemia alused. VIII väljaanne, Peterburi, 1906)
Pärast D.I. Mendelejevi ootamatut surma ja tema ustavate teadlaste kolleegide surma Venemaa Füüsikalis-keemiaühingus tõstis ta esimest korda käe Mendelejevi - sõbra ja kolleegi D.I. poja - surematule loomingule. Mendelejev ühiskonnast - Boriss Nikolajevitš Menšutkin. Muidugi ei tegutsenud ka see Boriss Nikolajevitš üksi – ta täitis ainult käsku. Lõppude lõpuks nõudis uus relativismi paradigma maailmaeetri idee tagasilükkamist; ja seepärast tõsteti see nõue dogma auastmele ning D.I. Mendelejev oli võltsitud.
Tabeli peamine moonutus on "nullrühma" ülekandmine. Tabelid selle lõpus, paremal ja sissejuhatus nn. "perioodid". Rõhutame, et selline (vaid esmapilgul – kahjutu) manipuleerimine on loogiliselt seletatav vaid Mendelejevi avastuse peamise metodoloogilise lüli: perioodilise elementide süsteemi selle alguses, allikas, s.o. tabeli vasakus ülanurgas peaks olema nullrühm ja nullrida, kus asub element “X” (Mendelejevi järgi - “Newtonium”), st. maailma saade.
Pealegi, kuna see element "X" on kogu tuletatud elementide tabeli ainus põhielement, on see kogu perioodilise tabeli argument. Tabeli nullrühma üleviimine selle lõppu hävitab Mendelejevi järgi kogu elementide süsteemi selle aluspõhimõtte idee.
Eelneva kinnituseks anname sõna D. I. Mendelejevile endale.
“... Kui argooni analoogid ei anna üldse ühendeid, siis on ilmne, et ühtegi varem tuntud elementide rühma ei saa kaasata ja nende jaoks tuleb avada spetsiaalne nullrühm ... See argooni asend nullrühma analoogid on perioodilise seaduse mõistmise rangelt loogiline tagajärg ja seetõttu (paigutus VIII rühma ei ole ilmselgelt õige) ei aktsepteeri seda mitte ainult mina, vaid ka Braisner, Piccini ja teised ...
Nüüd, kui on saanud väljaspool vähimatki kahtlust, et enne seda rühma I, kuhu tuleks paigutada vesinik, on nullrühm, mille esindajate aatomkaal on väiksem kui I rühma elementidel, tundub mulle võimatu. eitavad vesinikust kergemate elementide olemasolu.
Nendest pöörame esmalt tähelepanu 1. rühma esimese rea elemendile. Tähistame seda "y"-ga. Ilmselgelt kuulub ta argoongaaside ... "Koroniy" põhiomadustesse, mille tihedus on vesiniku suhtes umbes 0,2; ja see ei saa mingil juhul olla maailmaeeter. See element "y" on aga vajalik selleks, et jõuda vaimselt lähedale sellele kõige tähtsamale ja seega ka kõige kiiremini liikuvale elemendile "x", mida minu arvates võib eetriks pidada. Esialgu tahaksin nimetada seda "Newtoniumiks" - surematu Newtoni auks... Gravitatsiooniprobleemi ja kogu energiaga seotud probleeme (!!!) ei saa ette kujutada, et see päriselt lahendatakse ilma eetrist kui eetrist tõelise mõistmiseta. maailma meedium, mis edastab energiat vahemaade taha. Eetri tõelist mõistmist ei saa saavutada, kui ignoreerida selle keemiat ja mitte pidada seda elementaarseks aineks” (“Maailmaeetri keemilise mõistmise katse”, 1905, lk 27).
"Need elemendid asusid oma aatommassi poolest täpse koha halogeniidide ja leelismetallide vahel, nagu näitas Ramsay 1900. aastal. Nendest elementidest on vaja moodustada spetsiaalne nullrühm, mille 1900. aastal tunnustas esmakordselt Belgia Herrere. Pean siinkohal kasulikuks lisada, et otsustades otseselt selle järgi, et nullrühma elemente ei ole võimalik kombineerida, tuleks argooni analoogid asetada enne (!!!) rühma 1 elemente ja perioodilisuse süsteemi vaimus eeldada, et nende aatomkaal on väiksem kui leelismetallidel.
Nii see välja kukkus. Ja kui nii, siis see asjaolu kinnitab ühelt poolt perioodiliste põhimõtete õigsust ja teisest küljest näitab selgelt argooni analoogide suhet teiste varem tuntud elementidega. Selle tulemusena on võimalik analüüsitavaid põhimõtteid senisest veelgi laiemalt rakendada ning oodata nullrea elemente, mille aatomkaal on vesinikul tunduvalt väiksem.
Seega saab näidata, et esimeses reas, kõigepealt enne vesinikku, on nullrühma element aatommassiga 0,4 (võib-olla on see Yongi koroon) ja nullireas, nullrühmas, on on ebaoluliselt väikese aatommassiga piirav element, mis ei ole võimeline keemiliseks interaktsiooniks ja millel on selle tulemusena ülikiire osaline (gaasi) liikumine.
Need omadused tuleks ehk omistada kõikeläbiva (!!!) maailmaeetri aatomitele. Sellele mõttele viitan selle väljaande eessõnas ja 1902. aasta Venemaa ajakirja artiklis ... ”(“ Keemia alused. VIII väljaanne, 1906, lk 613 jj).
7. Punctum soliens
Nendest tsitaatidest tuleneb üsna kindlalt järgmine.
- Nullrühma elemendid alustavad iga teiste elementide rida, mis asuvad tabeli vasakus servas, "... mis on perioodilise seaduse mõistmise rangelt loogiline tagajärg" - Mendelejev.
- Eriti oluline ja perioodilise seaduse mõttes isegi erandlik koht kuulub elemendile "x", - "Newton", - maailmaeeter. Ja see spetsiaalne element peaks asuma kogu tabeli alguses, nn nullrea nullrühmas. Veelgi enam, kuna maailma eeter on perioodilise tabeli kõigi elementide süsteemi moodustav element (täpsemalt süsteemi moodustav üksus), on see sisuline argument kogu perioodilise tabeli elementide mitmekesisuse jaoks. Tabel ise toimib selles osas selle argumendi suletud funktsioonina.
Nüüd pöördume perioodilise tabeli esimeste võltsijate tööde poole.
8. Kuriteokoosseis
Selleks, et kõigi järgnevate teadlaste põlvkondade teadvusest välja juurida idee maailmaeetri eksklusiivsest rollist (ja just seda nõudis uus relativismi paradigma), viidi nullrühma elemendid spetsiaalselt üle. perioodilise tabeli vasak pool paremale poole, nihutades vastavad elemendid ühe rea võrra madalamale ja joondades nullrühma nn. "kaheksas". Loomulikult ei ole võltsitud tabelis elemendil "y" ega elemendil "x" enam kohta.
Kuid isegi sellest ei piisanud relativistide vennaskonna jaoks. Täpselt vastupidine, D.I. Mendelejev maailmaeetri eriti olulisest rollist. Eelkõige on perioodilise seaduse esimese võltsitud versiooni eessõnas D.I. Mendelejev, kes polnud üldse piinlik, B.M. Menšutkin nendib, et väidetavalt oli Mendelejev alati vastu maailmaeetri erilisele rollile looduslikes protsessides. Siin on väljavõte B.N. artiklist. Menshutkin:
“Nii (?!) pöördume jälle tagasi selle vaate juurde, millele (?!) D. I. Mendelejev alati (?!!!) vastu astus ja mis eksisteeris iidsetest aegadest filosoofide seas, kes pidasid kõiki nähtavaid ja teadaolevaid aineid ja kehasid koosnevaks sama kreeka filosoofide põhisubstants (kreeka filosoofide “proteule”, prima materia – rooma). See hüpotees on oma lihtsuse tõttu alati pooldajaid leidnud ja filosoofide õpetustes nimetati seda mateeria ühtsuse hüpoteesiks või ühtse mateeria hüpoteesiks.". (B.N. Menshutkin. “D.I. Mendelejev. Perioodiline seadus”. Toimetanud ja koos artikliga perioodilise seaduse hetkeseisu kohta B.N. Menšutkin. Riiklik kirjastus, M-L., 1926).
9. Rerum looduses
Hinnates D. I. Mendelejevi ja tema hoolimatute vastaste seisukohti, tuleb märkida järgmist.
Tõenäoliselt eksis Mendelejev tahtmatult selles, et "maailmaeeter" on "elementaaraine" (st "keemiline element" - selle mõiste tänapäevases tähenduses). Tõenäoliselt on "maailmaeeter" tõeline aine; ja sellisena, ranges mõttes, mitte "aine"; ja sellel ei ole "elementaarkeemiat" st. ei ole "äärmiselt madala aatommassiga" koos "ülikiire õige osalise liikumisega".
Las D.I. Mendelejev eksis eetri "substantsiaalsuses", "keemias". Lõpuks on see suure teadlase terminoloogiline valearvestus; ja tema ajal on see vabandatav, sest siis olid need terminid veel üsna ebamäärased, jõudsid alles teaduskäibesse. Kuid midagi muud on täiesti selge: Dmitri Ivanovitšil oli täiesti õigus, et "maailmaeeter" on olemus, mis moodustab kõike, kvintessents, millest koosneb kogu asjade maailm (materiaalne maailm) ja milles asuvad kõik materiaalsed moodustised. . Dmitri Ivanovitšil on õigus ka selles, et see aine edastab energiat kaugustesse ja sellel puudub igasugune keemiline aktiivsus. Viimane asjaolu ainult kinnitab meie ettekujutust, et D.I. Mendelejev tõstis teadlikult esile elemendi "x" kui erandliku üksuse.
Niisiis, "maailmaeeter", st. Universumi aine on isotroopne, tal puudub osaline struktuur, kuid see on Universumi, Universumi, absoluutne (st ülim, fundamentaalne, fundamentaalne universaalne) olemus. Ja just sellepärast, nagu D.I. Mendelejev, - maailmaeeter "ei ole võimeline keemiliseks interaktsiooniks" ega ole seetõttu "keemiline element", s.t. "elementaaraine" - nende mõistete tänapäevases tähenduses.
Dmitri Ivanovitšil oli õigus ka selles, et maailmaeeter on kauguste energiakandja. Ütleme veel: maailmaeeter kui Maailma substants ei ole looduses mitte ainult kandja, vaid ka igat liiki energia ("tegevusjõudude") "hoidja" ja "kandja".
Sajandite sügavusest D.I. Mendelejevit kordab veel üks silmapaistev teadlane – Torricelli (1608–1647): "Energia on nii peen olemuse kvintessents, et seda ei saa sisaldada üheski teises anumas, vaid ainult materiaalsete asjade sisimas olekus."
Niisiis, Mendelejevi ja Torricelli sõnul maailma saade on materiaalsete asjade sisemine aine. Seetõttu ei asu Mendelejevi "Newtoonium" lihtsalt tema perioodilise süsteemi nullrühma nullreal, vaid see on omamoodi "kroon" kogu tema keemiliste elementide tabelile. Kroon, mis moodustab kõik maailma keemilised elemendid, s.o. kogu aine. See kroon (mis tahes aine "ema", "aine-aine") on looduslik keskkond, mis on meie arvutuste kohaselt liikuma pandud ja ajendatud muutuma teise (teise) absoluutse olemuse poolt, mida me nimetasime "esmase aine oluliseks vooluks". põhiteave aine vormide ja liikumisviiside kohta universumis. Sellest lähemalt - ajakirjas "Vene mõte", 1-8, 1997, lk 28-31.
Maailmaeetri matemaatiliseks sümboliks valisime “O”, nulli ja semantilise sümbolina “süda”. Omakorda valisime substantsiaalse voo matemaatiliseks sümboliks ühiku “1” ja semantiliseks sümboliks “üks”. Seega saab ülaltoodud sümboolika põhjal võimalikuks ühes matemaatilises avaldises lühidalt väljendada looduses mateeria liikumise kõigi võimalike vormide ja meetodite kogu:
See väljend defineerib matemaatiliselt nn. kahe hulga avatud lõikumisintervall - komplektid "O" ja komplektid "1", samas kui selle väljendi semantiline määratlus on "üks emakas" või muul viisil: esmase põhiteabe oluline voog selle vormide ja meetodite kohta. Aine-substantsi liikumine läbib selle Aine-aine täielikult, st. maailma saade.
Religioossetes doktriinides on see "avatud intervall" riietatud kujundliku kujuga, mille kohaselt Jumal loob kõik maailmas oleva mateeria ainest-substantsist, millega Ta on pidevalt viljakas kooslusseisundis.
Selle artikli autor on teadlik, et see matemaatiline konstruktsioon oli taas inspireeritud temast, kui kummaline see ka ei tunduks, unustamatu D.I ideedest. Mendelejev, mida ta on väljendanud oma teostes (vt nt artiklit "Katse maailma eetri keemiliseks mõistmiseks"). Nüüd on aeg teha kokkuvõte meie selles väitekirjas esitatud uurimistööst.
10. Errata: ferro et igni
Maailmateaduse kategooriline ja küüniline ignoreerimine maailmaeetri koha ja rolli kohta looduslikes protsessides (ja perioodilises tabelis!) tekitas meie tehnokraatlikul ajastul kogu inimkonna probleemide spektri.
Peamised nendest probleemidest on kütus ja energia.
Just maailmaeetri rolli eiramine võimaldab teadlastel teha vale (ja kavala - samas) järelduse, et inimene saab oma igapäevaste vajaduste jaoks kasulikku energiat ammutada ainult põletades, s.t. aine (kütuse) pöördumatult hävitamine. Siit ka vale tees, et praegusel kütuseenergiatööstusel pole reaalset alternatiivi. Ja kui nii, siis väidetavalt jääb üle vaid üks: toota tuumaenergiat (keskkonnaliselt kõige mustem!) ja gaasi-nafta-söe tootmist, ummistades ja mürgitades tohutult oma elupaika.
Just maailmaeetri rolli eiramine sunnib kõiki kaasaegseid tuumateadlasi kavalale "päästmise" otsingule aatomite ja elementaarosakeste lõhestamisel spetsiaalsete kallite sünkrotronkiirendite juures. Nende koletiste ja tagajärgedes ülimalt ohtlike katsete käigus tahetakse avastada ja edasi kasutada nn väidetavalt "heaks". "kvark-gluoonplasma", nende valede ideede järgi - justkui "eelaine" (tuumateadlaste endi termin), nende vale kosmoloogilise teooria järgi nn. "Suure paugu universum".
Märkimist väärib meie arvutuste kohaselt, et kui see nn. "Kõigi kaasaegsete tuumafüüsikute salajaseim unistus" saavutatakse tahtmatult, siis on see suure tõenäosusega kogu maapealse elu inimtekkeline lõpp ja planeedi Maa enda lõpp - tõesti "Suur pauk" globaalsel tasandil. mastaabis, kuid mitte lihtsalt teesklema, vaid päriselt.
Seetõttu on vaja võimalikult kiiresti lõpetada see hullumeelne maailma akadeemilise teaduse eksperimenteerimine, mis on pealaest jalatallani löödud psi-faktori mürkiga ja mis tundub, et isegi ei kujuta ette nende hullude võimalikke katastroofilisi tagajärgi. parateaduslikud ettevõtmised.
D. I. Mendelejevil osutus õigus: "Gravitatsiooniprobleemi ja kogu energiatööstuse probleeme ei saa ette kujutada reaalselt lahendatavat ilma reaalse arusaamata eetrist kui maailma keskkonnast, mis edastab energiat kaugele."
D. I. Mendelejevil osutus õigus selles, et "kunagi nad arvavad, et selle valdkonna asjade üleandmine selles elavatele isikutele ei too kaasa parimaid tagajärgi, kuigi selliseid inimesi on kasulik kuulata."
„Öeldu põhiline tähendus seisneb selles, et ühised, igavesed ja püsivad huvid ei kattu sageli isiklike ja ajutiste huvidega, vaid on sageli isegi vastuolus ning minu arvates tuleb eelistada - kui on juba võimatu ühitada - esimene ja mitte teine. See on meie aja draama." D. I. Mendelejev. "Mõtted Venemaa tundmise suunas". 1906
Niisiis, maailmaeeter on mis tahes keemilise elemendi substants ja seega mis tahes ainest absoluutne tõeline mateeria kui universaalset elementi moodustav olemus.
Maailmaeeter on kogu ehtsa perioodilise tabeli allikas ja kroon, selle algus ja lõpp, Dmitri Ivanovitš Mendelejevi elementide perioodilise tabeli alfa ja oomega.
MENDELEJEVI PERIOODIKATABEL
Mendelejevi keemiliste elementide perioodilisuse tabeli konstruktsioon vastab arvuteooria ja ortogonaalsete aluste iseloomulikele perioodidele. Hadamardi maatriksite täiendamine paaris- ja paaritu järku maatriksitega loob pesastatud maatriksielementide struktuurse aluse: esimese (Odin), teise (Euler), kolmanda (Mersenne), neljanda (Hadamard) ja viienda (Fermat) järku maatriksid.
On lihtne näha, et suurusjärgus 4 k Hadamardi maatriksitele vastavad inertsed elemendid, mille aatommass on neljakordne: heelium 4, neoon 20, argoon 40 (39,948) jne, aga ka elu ja digitaaltehnoloogia alused: süsinik 12, hapnik 16, räni 28 , germaanium 72.
Tundub, et Mersenne'i järgu maatriksitega 4 k-1, vastupidi, kõik aktiivne, mürgine, hävitav ja söövitav on seotud. Kuid need on ka radioaktiivsed elemendid - energiaallikad ja plii 207 (lõppprodukt, mürgised soolad). Fluor on loomulikult 19. Mersenne'i maatriksite järjestused vastavad radioaktiivsete elementide järjestusele, mida nimetatakse aktiiniumi seeriaks: uraan 235, plutoonium 239 (isotoop, mis on uraanist võimsam aatomienergia allikas) jne. Need on ka leelismetallid liitium 7, naatrium 23 ja kaalium 39.

Gallium – aatommass 68
Tellimused 4 k–2 Euleri maatriksit (kahekordne Mersenne) vastab lämmastikule 14 (atmosfääri baas). Lauasoola moodustavad kaks "mersennilaadset" naatriumi 23 ja kloori 35 aatomit, koos on see kombinatsioon tüüpiline, just Euleri maatriksite jaoks. Massiivsem kloor kaaluga 35,4 ei küündi päris Hadamardi mõõtmeni 36. Soolakristallid: kuubik (! s.t. leebe tegelane, Hadamars) ja oktaeeder (trotslikum, see on kahtlemata Euler).
Aatomifüüsikas on raud 56 - nikkel 59 üleminek piiriks elementide vahel, mis annavad energiat suurema tuuma (vesinikpomm) sünteesil ja lagunemisel (uraanipomm). Järjekord 58 on kuulus selle poolest, et selle jaoks pole mitte ainult Hadamardi maatriksite analooge Belevitši maatriksite kujul, mille diagonaalis on nullid, vaid selle jaoks pole ka palju kaalutud maatriksiid - lähim ortogonaal W(58,53) on igas veerus ja reas 5 nulli (sügav vahe ).
Fermat' maatriksitele ja nende asendustele vastavas seerias 4 k+1, maksab saatuse tahtel 257 fermii.Ei oska midagi öelda,täpne tabamus. Siin on kuld 197. Elektroonika sümbolid vask 64 (63.547) ja hõbe 108 (107.868) ilmselt kullani ei ulatu ja vastavad tagasihoidlikumatele Hadamardi maatriksitele. Vask, mille aatommass pole kaugeltki 63, on keemiliselt aktiivne – selle rohelised oksiidid on hästi tuntud.
Suure suurendusega boorikristallid
FROM kuldne suhe boor on ühendatud - aatommass kõigi teiste elementide hulgas on lähim 10-le (täpsemalt 10,8, mõjutab ka aatommassi lähedus paaritutele arvudele). Boor on üsna keeruline element. Bohril on elu enda ajaloos segane roll. Selle struktuuride raamistik on palju keerulisem kui teemant. Ainulaadne keemilise sideme tüüp, mis võimaldab booril mistahes lisandeid absorbeerida, on väga halvasti mõistetav, kuigi suur osa teadlasi on sellega seotud uuringute eest juba saanud Nobeli preemia. Boorikristalli kuju on ikosaeeder, viis kolmnurka moodustavad tipu.
Plaatina müsteerium. Viies element on kahtlemata väärismetallid nagu kuld. Vedrustus üle Hadamardi mõõtme 4 k, 1 suurele.

Stabiilne isotoop uraan 238
Tuletage siiski meelde, et Fermat' numbrid on haruldased (lähim on 257). Looduslikud kullakristallid on kuubilähedase kujuga, kuid ka pentagramm sädeleb. Selle lähim naaber, plaatina, väärismetall, on vähem kui 4 korda väiksema aatommassiga kullast 197. Plaatina aatommass ei ole 193, vaid mõnevõrra suurenenud, 194 (Euleri maatriksite järjekord). Pisiasi, kuid see toob ta mõne agressiivsema elemendi leeri. Tasub meeles pidada, et seoses oma inertsusega (see lahustub võib-olla vees) kasutatakse plaatinat keemiliste protsesside aktiivse katalüsaatorina.
Käsnjas plaatina süütab toatemperatuuril vesiniku. Plaatina olemus pole sugugi rahulik, iriidium 192 käitub vaiksemalt (isotoopide 191 ja 193 segu). See on pigem vask, kuid kulla kaalu ja iseloomuga.
Neoon 20 ja naatrium 23 vahel ei ole elementi, mille aatommass on 22. Loomulikult on aatomkaalud lahutamatu tunnus. Kuid isotoopide seas on omakorda ka kurioosne omaduste korrelatsioon arvude ja vastavate ortogonaalsete aluste maatriksite omadustega. Tuumakütusena on enim kasutust leidnud isotoop uraan 235 (Mersenne'i maatriksite järjekord), milles on võimalik isemajandav tuumaahelreaktsioon. Looduses esineb see element stabiilsel kujul uraanina 238 (Euleri maatriksite järjekord). 13 aatommassiga elementi pole olemas. Mis puutub kaosesse, siis perioodilisuse tabeli stabiilsete elementide piiratud arv ja kolmeteistkümnendat järku maatriksites nähtava barjääri tõttu kõrget järku maatriksite leidmise raskused on korrelatsioonis.
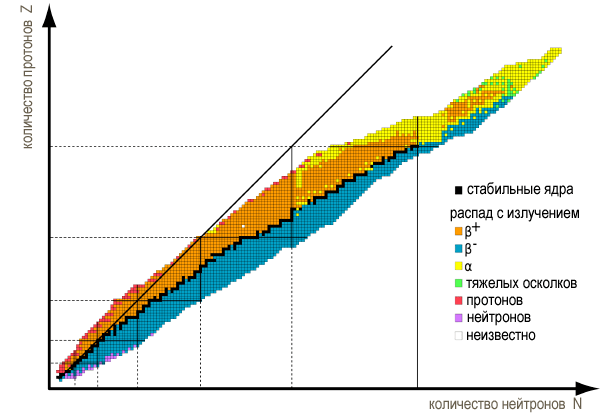
Keemiliste elementide isotoobid, stabiilsuse saar
Ta kasutas Robert Boyle'i ja Antoine Lavouzieri tööd. Esimene teadlane pooldas lagunematute keemiliste elementide otsimist. 15 Boyle'i nimekirjas 1668. aastal.
Lavuzier lisas neile veel 13, kuid sajand hiljem. Otsing venis, sest puudus ühtne teooria elementidevahelise seose kohta. Lõpuks astus "mängu" Dmitri Mendelejev. Ta otsustas, et ainete aatommassi ja nende koha vahel süsteemis on seos.
See teooria võimaldas teadlasel avastada kümneid elemente ilma neid praktikas, vaid looduses avastamata. See pandi järeltulijate õlgadele. Aga nüüd pole asi nendes. Pühendagem artikkel suurele vene teadlasele ja tema lauale.
Perioodilise tabeli loomise ajalugu
perioodilisustabel algas raamatuga "Omaduste seos elementide aatommassiga". Teos anti välja 1870. aastatel. Samal ajal rääkis vene teadlane riigi keemiaseltsiga ja saatis tabeli esimese versiooni kolleegidele välismaalt.
Enne Mendelejevit avastasid erinevad teadlased 63 elementi. Meie kaasmaalane alustas nende omaduste võrdlemisest. Esiteks töötas ta kaaliumi ja klooriga. Seejärel võttis ta kasutusele leeliselise rühma metallide rühma.
Keemik sai spetsiaalse laua ja elementide kaardid, et need nagu pasjanss välja laotada, otsides õigeid vasteid ja kombinatsioone. Selle tulemusena tekkis arusaam: - komponentide omadused sõltuvad nende aatomite massist. Niisiis, perioodilisuse tabeli elemendid ridadesse rivistatud.
Keemia maestro avastus oli otsus jätta nendesse ridadesse tühimikud. Aatommasside erinevuse perioodilisus pani teadlase oletama, et inimkond ei ole veel kõiki elemente teada. Kaaluvahed osade "naabrite" vahel olid liiga suured.

Sellepärast, Mendelejevi perioodilisustabel sai nagu malelaud, kus oli palju "valgeid" rakke. Aeg on näidanud, et nad tõesti ootasid oma "külalisi". Näiteks muutusid need inertseks gaasiks. Heelium, neoon, argoon, krüptoon, radioakt ja ksenoon avastati alles 20. sajandi 30. aastatel.
Nüüd müütidest. Laialt arvatakse, et keemia perioodiline tabel ilmus talle unes. Need on ülikooli õppejõudude intriigid, täpsemalt üks neist - Aleksander Inostrantsev. See on vene geoloog, kes pidas loenguid Peterburi kaevandusülikoolis.
Inostrantsev tundis Mendelejevit ja käis tal külas. Kord, olles otsingutest kurnatud, jäi Dmitri otse Aleksandri ees magama. Ta ootas, kuni keemik ärkab ja nägi, kuidas Mendelejev haarab paberitüki ja kirjutab üles tabeli lõpliku versiooni.
Tegelikult polnud teadlasel lihtsalt aega seda teha, enne kui Morpheus ta kinni püüdis. Inostrantsev tahtis aga oma õpilasi lõbustada. Geoloog mõtles nähtu põhjal välja ratta, mille tänulikud kuulajad kiiresti massidesse levitasid.
Perioodilise tabeli omadused
Alates esimesest versioonist 1969. aastal järguline perioodilisustabel paranenud mitu korda. Niisiis oli väärisgaaside avastamisega 1930. aastatel võimalik tuletada elementide uus sõltuvus – nende seerianumbritest, mitte massist, nagu väitis süsteemi autor.
Mõiste "aatommass" asendati mõistega "aatomnumber". Oli võimalik uurida prootonite arvu aatomite tuumades. See number on elemendi seerianumber.
20. sajandi teadlased uurisid ka aatomite elektroonilist ehitust. See mõjutab ka elementide perioodilisust ja kajastub hilisemates väljaannetes. perioodilised tabelid. Foto Loetelu näitab, et selles sisalduvad ained on aatommassi kasvades järjestatud.
Põhiprintsiipi ei muudetud. Mass suureneb vasakult paremale. Samas ei ole tabel ühekordne, vaid jagatud 7 perioodiks. Sellest ka nimekirja nimi. Periood on horisontaalne rida. Selle algus on tüüpilised metallid, lõpp on mittemetalliliste omadustega elemendid. Langus on järk-järguline.

On suuri ja väikeseid perioode. Esimesed on tabeli alguses, neid on 3. See avab 2-elemendilise perioodiga loendi. Järgnevad kaks veergu, milles on 8 üksust. Ülejäänud 4 perioodi on suured. Kuues on pikim, selles on 32 elementi. Neljandas ja viiendas on neid 18 ja seitsmendas - 24.
Saab kokku lugeda mitu elementi tabelis Mendelejev. Kokku on 112 pealkirja. Nimed. Seal on 118 lahtrit, kuid loendis on 126 väljaga variatsioone. Veel on tühjad lahtrid avastamata elementide jaoks, millel pole nimesid.
Kõik perioodid ei mahu ühele reale. Suured perioodid koosnevad 2 reast. Metallide hulk neis kaalub üles. Seetõttu on alumised read neile täielikult pühendatud. Ülemistes ridades täheldatakse metallide järkjärgulist vähenemist inertsete aineteni.
Perioodilise tabeli pildid vertikaalselt jagatud. seda rühmad perioodilisustabelis, neid on 8. Keemiliste omaduste poolest sarnased elemendid on paigutatud vertikaalselt. Need jagunevad põhi- ja sekundaarseteks alarühmadeks. Viimased algavad alles 4. perioodist. Põhilistesse alarühmadesse kuuluvad ka väikeste perioodide elemendid.
Perioodilise tabeli olemus
Periooditabeli elementide nimetused on 112 positsiooni. Nende ühtsesse loendisse paigutamise olemus on esmaste elementide süstematiseerimine. Nad hakkasid selle pärast võitlema isegi iidsetel aegadel.
Aristoteles oli üks esimesi, kes mõistis, millest kõik olemasolev koosneb. Ta võttis aluseks ainete omadused - külm ja kuumus. Empidokles tõi elementide järgi välja 4 põhiprintsiipi: vesi, maa, tuli ja õhk.
Metallid perioodilisustabelis, nagu ka teised elemendid, on põhiprintsiibid, kuid tänapäevasest vaatenurgast. Vene keemikul õnnestus avastada enamik meie maailma komponente ja oletada veel tundmatute primaarsete elementide olemasolu.

Selgub, et perioodilisuse tabeli hääldus- meie reaalsuse teatud mudeli väljaütlemine, selle komponentideks lammutamine. Nende õppimine pole aga lihtne. Proovime ülesannet lihtsamaks muuta, kirjeldades paari tõhusat meetodit.
Kuidas õppida perioodilisustabelit
Alustame kaasaegsest meetodist. Arvutiteadlased on välja töötanud mitmeid välkmänge, mis aitavad Mendelejevi nimekirja pähe õppida. Projektis osalejatel pakutakse elemente leida erinevate võimaluste järgi, näiteks nime, aatommassi, tähemärgistuse järgi.
Mängijal on õigus valida tegevusala – ainult osa lauast või kogu see. Samuti jätame meie testamendis välja elementide nimed ja muud parameetrid. See raskendab otsingut. Edasijõudnutele on ette nähtud ka taimer, see tähendab, et treening toimub kiirusega.
Mängutingimused teevad õppimiseks elementide numbrid perioodilisustabelis mitte igav, vaid lõbus. Põnevus ärkab ja teadmisi peas on lihtsam süstematiseerida. Need, kes ei aktsepteeri arvuti välklampide projekte, pakuvad nimekirja meeldejätmiseks traditsioonilisemat viisi.
See on jagatud 8 rühma ehk 18 rühma (vastavalt 1989. aasta väljaandele). Mäletamise hõlbustamiseks on parem luua mitu eraldi tabelit, mitte töötada terve versiooniga. Abiks on ka iga elemendiga sobitatud visuaalsed pildid. Toetuge oma assotsiatsioonidele.
Niisiis saab ajus olevat rauda korreleerida näiteks küünega ja elavhõbedat termomeetriga. Kas elemendi nimi on võõras? Kasutame sugestiivsete assotsiatsioonide meetodit. , näiteks koostame sõnade "taffy" ja "speaker" algusest.
Perioodilise tabeli omadusedära õpi ühe istumisega. Õppetunnid on soovitatavad 10-20 minutit päevas. Alustuseks on soovitatav meeles pidada ainult põhiomadusi: elemendi nimi, tähistus, aatommass ja seerianumber.
Koolilapsed eelistavad riputada perioodilisustabeli töölaua kohale või seinale, mida sageli vaadatakse. Meetod sobib inimestele, kellel on ülekaalus visuaalne mälu. Loendi andmed jäävad tahes-tahtmata meelde isegi ilma tuupita.
Seda arvestavad ka õpetajad. Reeglina ei sunni need nimekirja pähe õppima, vaid võimaldavad seda vaadata isegi kontrollnimekirjade pealt. Pidev tabeli vaatamine on võrdväärne seinale printimise või eksamite eel petulehtede kirjutamisega.
Uuringut alustades meenutagem, et Mendelejev ei mäletanud oma nimekirja kohe. Kord, kui teadlaselt küsiti, kuidas ta laua avas, vastati: "Ma olen sellele mõelnud võib-olla 20 aastat, aga mõtlete: ma istusin ja järsku on see valmis." Perioodiline süsteem on vaevarikas töö, mida ei saa lühikese ajaga omandada.

Teadus ei salli kiirustamist, sest see viib pettekujutluste ja tüütute vigadeni. Nii et samal ajal Mendelejeviga koostas tabeli Lothar Meyer. Sakslane ei lõpetanud aga nimekirja pisutki ega olnud oma seisukoha tõestamisel veenev. Seetõttu tunnustas avalikkus vene teadlase, mitte tema Saksamaalt pärit kolleegi keemiku tööd.
Teades perioodilisuse seaduse sõnastust ja kasutades D. I. Mendelejevi elementide perioodilist süsteemi, saab iseloomustada mis tahes keemilist elementi ja selle ühendeid. Sellise keemilise elemendi omaduse on mugav plaani järgi kokku liita.
I. Keemilise elemendi tähis ja selle nimi.
II. Keemilise elemendi asukoht elementide perioodilises süsteemis D.I. Mendelejev:
- seerianumber;
- perioodi number;
- rühma number;
- alarühm (peamine või teisene).
III. Keemilise elemendi aatomi struktuur:
- aatomi tuuma laeng;
- keemilise elemendi suhteline aatommass;
- prootonite arv;
- elektronide arv;
- neutronite arv;
- aatomi elektrooniliste tasemete arv.
IV. Aatomi elektroonilised ja elektrongraafilised valemid, selle valentselektronid.
V. Keemilise elemendi tüüp (metall või mittemetall, s-, p-, d- või f-element).
VI. Keemilise elemendi kõrgema oksiidi ja hüdroksiidi valemid, nende omaduste omadused (aluselised, happelised või amfoteersed).
VII. Keemilise elemendi metalliliste või mittemetalliliste omaduste võrdlus naaberelementide omadustega perioodide ja alarühmade kaupa.
VIII. Aatomi maksimaalne ja minimaalne oksüdatsiooniaste.
Näiteks esitame järjenumbriga 15 keemilise elemendi ja selle ühendite karakteristiku vastavalt positsioonile D. I. Mendelejevi elementide perioodilises süsteemis ja aatomi ehitusele.
I. Leiame D. I. Mendelejevi tabelist lahtri keemilise elemendi numbriga, paneme kirja selle sümboli ja nimetuse.
Keemiline element number 15 on fosfor. Selle sümbol on R.
II. Iseloomustagem elemendi asukohta D. I. Mendelejevi tabelis (perioodi number, rühm, alarühma tüüp).
Fosfor on V rühma põhialagrupis, 3. perioodil.
III. Esitame keemilise elemendi aatomi koostise üldise kirjelduse (tuumalaeng, aatommass, prootonite arv, neutronid, elektronid ja elektrontasemed).
Fosfori aatomi tuumalaeng on +15. Fosfori suhteline aatommass on 31. Aatomi tuum sisaldab 15 prootonit ja 16 neutronit (31 - 15 = 16). Fosforiaatomil on kolm energiataset 15 elektroniga.
IV. Koostame aatomi elektroonilised ja elektrongraafilised valemid, märgime selle valentselektronid.
Fosfori aatomi elektrooniline valem on: 15 P 1s 2 2s 2 2p 6 3s 2 3p 3 .
Fosfori aatomi välistasandi elektrongraafiline valem: kolmandal energiatasandil on 3s alamtasandil kaks elektroni (ühte lahtrisse on kirjutatud kaks vastassuunalist noolt), kolm elektroni on kolmel p- alamtasand (üks igas kolmes lahtris on kirjutatud samas suunas osutavate nooltega).
Valentselektronid on välise tasandi elektronid, st. 3s2 3p3 elektronid.
V. Määrake keemilise elemendi tüüp (metall või mittemetall, s-, p-, d- või f-element).
Fosfor on mittemetall. Kuna fosfori aatomi viimane alamtase, mis on täidetud elektronidega, on p-alamtase, kuulub fosfor p-elementide perekonda.
VI. Koostame fosfori kõrgema oksiidi ja hüdroksiidi valemid ning iseloomustame nende omadusi (aluseline, happeline või amfoteerne).
Kõrgeim fosforoksiid P 2 O 5 omab happeoksiidi omadusi. Kõrgemale oksiidile H 3 PO 4 vastaval hüdroksiidil on happe omadused. Kinnitame need omadused keemiliste reaktsioonide tüüpide võrranditega:
P 2 O 5 + 3 Na 2 O \u003d 2Na 3 PO 4
H3PO4 + 3NaOH \u003d Na3PO4 + 3H2O
VII. Võrdleme fosfori mittemetallilisi omadusi naaberelementide omadustega perioodide ja alarühmade kaupa.
Fosfori naaber alarühmas on lämmastik. Fosfori naabrid on sellel perioodil räni ja väävel. Peamiste alarühmade keemiliste elementide aatomite mittemetallilised omadused suureneva seerianumbriga perioodide suurenemine ja rühmade vähenemine. Seetõttu on fosfori mittemetallilised omadused tugevamad kui räni omad ja vähem väljendunud kui lämmastiku ja väävli omadused.
VIII. Määrake fosfori aatomi maksimaalne ja minimaalne oksüdatsiooniaste.
Peamiste alarühmade keemiliste elementide maksimaalne positiivne oksüdatsiooniaste on võrdne rühma numbriga. Fosfor on viienda rühma põhialarühmas, seega on fosfori maksimaalne oksüdatsiooniaste +5.
Mittemetallide minimaalne oksüdatsiooniaste on enamikul juhtudel võrdne rühma numbri ja numbri kaheksa vahega. Seega on fosfori minimaalne oksüdatsiooniaste -3.
Meid ümbritseb palju erinevaid asju ja objekte, elavaid ja elutuid looduskehi. Ja neil kõigil on oma koostis, struktuur, omadused. Elusolendites toimuvad kõige keerulisemad biokeemilised reaktsioonid, mis kaasnevad elutegevuse protsessidega. Elustud kehad täidavad looduses ja biomassi elus erinevaid funktsioone ning neil on keeruline molekulaarne ja aatomkoostis.
Kuid planeedi objektidel on ühine tunnus: need koosnevad paljudest pisikestest struktuursetest osakestest, mida nimetatakse keemiliste elementide aatomiteks. Nii väikesed, et neid pole palja silmaga näha. Mis on keemilised elemendid? Millised omadused neil on ja kuidas sa nende olemasolust teadsid? Proovime selle välja mõelda.
Keemiliste elementide mõiste
Tavamõistes on keemilised elemendid vaid aatomite graafiline kujutis. Osakesed, millest koosneb kõik universumis eksisteeriv. See tähendab, et küsimusele "mis on keemilised elemendid" saab sellise vastuse anda. Need on keerulised väikesed struktuurid, aatomite kõigi isotoopide kogumid, mida ühendab ühine nimi ja millel on oma graafiline tähis (sümbol).
Praeguseks on teada 118 elementi, mis avastatakse nii looduslikes tingimustes kui ka sünteetiliselt, tuumareaktsioonide ja teiste aatomite tuumade kaudu. Igal neist on teatud omaduste kogum, selle asukoht üldises süsteemis, avastuslugu ja nimi ning neil on ka teatud roll elusolendite olemuses ja elus. Keemia on nende omaduste uurimine. Keemilised elemendid on molekulide, lihtsate ja keerukate ühendite ning sellest tulenevalt ka keemiliste vastastikmõjude loomise aluseks.
Avastamise ajalugu
Arusaamine sellest, mis keemilised elemendid on, tekkis alles 17. sajandil tänu Boyle'i tööle. Tema oli see, kes sellest kontseptsioonist esimest korda rääkis ja andis sellele järgmise definitsiooni. Need on jagamatud väikesed lihtsad ained, mis moodustavad kõik ümbritseva, sealhulgas kõik keerulised.
Enne seda tööd domineerisid alkeemikute seisukohad, kes tunnustasid nelja elemendi – Empidoklese ja Aristotelese – teooriat, aga ka neid, kes avastasid "põlevad põhimõtted" (väävel) ja "metallilised põhimõtted" (elavhõbe).
Peaaegu terve 18. sajandi oli laialt levinud täiesti ekslik flogistoni teooria. Kuid juba selle perioodi lõpus tõestab Antoine Laurent Lavoisier, et see on vastuvõetamatu. Ta kordab Boyle’i sõnastust, kuid samas täiendab seda esimese katsega süstematiseerida kõik tol ajal tuntud elemendid, jagades need nelja rühma: metallid, radikaalid, muldad, mittemetallid.

Järgmine suur samm keemiliste elementide mõistmisel tuleb Daltonilt. Teda tunnustatakse aatommassi avastamise eest. Selle põhjal jaotab ta osa teadaolevatest keemilistest elementidest nende aatommassi suurendamise järjekorras.
Teaduse ja tehnoloogia pidevalt intensiivne areng võimaldab teha mitmeid looduslike kehade koostises uute elementide avastusi. Seetõttu sai teadus 1869. aastaks - D. I. Mendelejevi suure loomise ajaks - teadlikuks 63 elemendi olemasolust. Vene teadlase töö sai nende osakeste esimeseks täielikuks ja igavesti fikseeritud klassifikatsiooniks.
Keemiliste elementide struktuur sel ajal ei olnud kindlaks tehtud. Usuti, et aatom on jagamatu, et see on väikseim ühik. Radioaktiivsuse nähtuse avastamisega tõestati, et see on jagatud struktuuriosadeks. Peaaegu kõik eksisteerivad korraga mitme loodusliku isotoobi kujul (sarnased osakesed, kuid erineva arvu neutronstruktuuridega, millest aatommass muutub). Seega oli eelmise sajandi keskpaigaks võimalik saavutada kord keemilise elemendi mõiste määratlemisel.
Mendelejevi keemiliste elementide süsteem
Teadlane võttis aluseks aatommassi erinevuse ja suutis leidlikult järjestada kõik teadaolevad keemilised elemendid kasvavas järjekorras. Tema teadusliku mõtlemise ja ettenägelikkuse kogu sügavus ja geniaalsus seisnes aga selles, et Mendelejev jättis oma süsteemi tühjad kohad, avatud rakud seni tundmatute elementide jaoks, mis teadlase sõnul tulevikus avastatakse.
Ja kõik läks täpselt nii, nagu ta ütles. Mendelejevi keemilised elemendid täitsid aja jooksul kõik tühjad rakud. Iga teadlaste ennustatud struktuur on avastatud. Ja nüüd võime julgelt öelda, et keemiliste elementide süsteemi esindab 118 ühikut. Tõsi, kolm viimast avastust pole veel ametlikult kinnitatud.
Keemiliste elementide süsteemi ennast kuvatakse graafiliselt tabelina, milles elemendid on järjestatud vastavalt nende omaduste hierarhiale, tuumade laengutele ja nende aatomite elektronkestade struktuurilistele iseärasustele. Niisiis, seal on perioodid (7 tükki) - horisontaalsed read, rühmad (8 tükki) - vertikaalsed, alarühmad (iga rühma sees põhi- ja teisene). Kõige sagedamini asetatakse tabeli alumistesse kihtidesse eraldi kaks rida perekondi - lantaniidid ja aktiniidid.

Elemendi aatommass koosneb prootonitest ja neutronitest, mille kogusummat nimetatakse "massiarvuks". Prootonite arv määratakse väga lihtsalt - see on võrdne süsteemi elemendi järjekorranumbriga. Ja kuna aatom tervikuna on elektriliselt neutraalne süsteem, see tähendab, et tal pole üldse laengut, on negatiivsete elektronide arv alati võrdne positiivsete prootoniosakeste arvuga.
Seega saab keemilise elemendi omadusi anda selle asukoha järgi perioodilisuse süsteemis. Lahtris kirjeldatakse ju peaaegu kõike: seerianumbrit, mis tähendab elektrone ja prootoneid, aatommassi (antud elemendi kõigi olemasolevate isotoopide keskmine väärtus). On näha, millisel perioodil struktuur paikneb (mis tähendab, et nii paljudes kihtides on elektronid). Samuti saate põhialarühmade elementide jaoks ennustada negatiivsete osakeste arvu viimasel energiatasemel - see on võrdne selle rühma arvuga, milles element asub.

Neutronite arvu saab arvutada, lahutades prootonid massiarvust, see tähendab seerianumbrist. Seega on iga keemilise elemendi jaoks võimalik saada ja koostada terve elektrongraafiline valem, mis kajastab täpselt selle struktuuri ning näitab võimalikke ja avalduvaid omadusi.
Elementide levik looduses
Selle probleemi uurimisega tegeleb terve teadus, kosmokeemia. Andmed näitavad, et elementide jaotus meie planeedil kordab universumis samu mustreid. Kergete, raskete ja keskmiste aatomite tuumade peamiseks allikaks on tähtede sisemuses toimuvad tuumareaktsioonid – nukleosüntees. Tänu nendele protsessidele on Universum ja avakosmos varustanud meie planeeti kõigi olemasolevate keemiliste elementidega.
Kokku avastasid inimesed 118-st teadaolevast esindajast looduslikes allikates 89. Need on põhilised, levinumad aatomid. Keemilisi elemente on sünteesitud ka kunstlikult tuumade neutronitega pommitamise teel (nukleosüntees laboris).

Kõige arvukamad on selliste elementide lihtsad ained nagu lämmastik, hapnik, vesinik. Süsinik on kõigi orgaaniliste ainete koostisosa, mis tähendab, et sellel on ka juhtpositsioon.
Klassifikatsioon aatomite elektroonilise struktuuri järgi
Süsteemi kõigi keemiliste elementide üks levinumaid klassifikatsioone on nende jaotus nende elektroonilise struktuuri alusel. Selle järgi, mitu energiataset aatomi kestas sisaldub ja milline neist sisaldab viimaseid valentselektrone, saab eristada nelja elementide rühma.
S-elemendid
Need on need, milles s-orbitaal täidetakse viimasena. See perekond sisaldab põhialarühma esimese rühma elemente (või ainult üks elektron välisel tasemel määrab nende esindajate sarnased omadused tugevate redutseerijatena.
R-elemendid
Ainult 30 tükki. Valentselektronid asuvad p-alatasandil. Need on elemendid, mis moodustavad peamised alarühmad kolmandast kaheksanda rühma, mis on seotud 3,4,5,6 perioodiga. Nende hulgas leidub vastavalt nende omadustele nii metalle kui ka tüüpilisi mittemetallilisi elemente.
d-elemendid ja f-elemendid
Need on siirdemetallid 4–7 suure perioodiga. Kokku on 32 elementi. Lihtsatel ainetel võivad olla nii happelised kui aluselised omadused (oksüdeerivad ja redutseerivad). Samuti amfoteerne, see tähendab kahekordne.
F-perekonda kuuluvad lantaniidid ja aktiniidid, milles viimased elektronid asuvad f-orbitaalidel.
Elementidest moodustunud ained: lihtsad
Samuti võivad kõik keemiliste elementide klassid eksisteerida lihtsate või keerukate ühendite kujul. Niisiis on tavaks pidada lihtsateks neid, mis on moodustatud samast struktuurist erinevates kogustes. Näiteks O 2 on hapnik või dihapnik ja O 3 on osoon. Seda nähtust nimetatakse allotroopiaks.

Lihtsad keemilised elemendid, mis moodustavad samanimelisi ühendeid, on iseloomulikud igale perioodilise süsteemi esindajale. Kuid mitte kõik need pole oma omaduste poolest ühesugused. Niisiis, on olemas lihtsad ained metallid ja mittemetallid. Esimesed moodustavad põhialagrupid grupiga 1-3 ja kõik tabelis olevad teisejärgulised alagrupid. Mittemetallid moodustavad 4-7 rühma peamised alarühmad. Kaheksas põhi sisaldab spetsiaalseid elemente - vääris- või inertgaase.
Kõigist seni avastatud lihtsatest elementidest on tavatingimustes teada 11 gaasi, 2 vedelat ainet (broomi ja elavhõbe), kõik ülejäänud on tahked.
Keerulised ühendused
Tavaliselt viidatakse neile, mis koosnevad kahest või enamast keemilisest elemendist. Näiteid on palju, sest teada on üle 2 miljoni keemilise ühendi! Need on soolad, oksiidid, alused ja happed, komplekssed kompleksühendid, kõik orgaanilised ained.





