Saada oma head tööd teadmistebaasi on lihtne. Kasutage allolevat vormi
Üliõpilased, magistrandid, noored teadlased, kes kasutavad teadmistebaasi oma õpingutes ja töös, on teile väga tänulikud.
postitatud http://www.allbest.ru/
Sissejuhatus
1. Antibiootikumide klassifikatsioon
2. Beeta-laktaamantibiootikumid
3. Penitsilliinid
4. Tsefalosporiinide rühm
5. Karbapeneemide rühm
6. Monobaktaamide rühm
7. Tetratsükliini rühm
8. Aminoglükosiidirühm
9. Levomütsetiinid
10. Glükopeptiidide rühm
11. Linkosamiidrühm
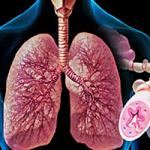
12. Tuberkuloossed keemiaravi ravimid
13. Rahvusvahelise Tuberkuloosiliidu tuberkuloosivastaste ravimite klassifikatsioon
14. Polüpeptiidid
Kirjandus
Sissejuhatus
Antibiootikumid on ained, mis pärsivad elusrakkude, enamasti prokarüootsete ja algloomade kasvu. Antibiootikumid võivad olla looduslikku (looduslikku) päritolu ja kunstlikud (sünteetilised ja poolsünteetilised).
Loodusliku päritoluga antibiootikume toodavad enamasti aktinomütseedid ja hallitusseened, kuid neid võib saada ka bakteritest (polümüksiinid), taimedest (fütontsiidid), loomade ja kalade kudedest.
Ravimitena kasutatakse antibiootikume, mis pärsivad bakterite kasvu ja paljunemist. Antibiootikume kasutatakse laialdaselt ka onkoloogilises praktikas tsütostaatiliste (antineoplastiliste) ravimitena. Viirusliku etioloogiaga haiguste ravis ei ole antibiootikumide kasutamine soovitatav, kuna need ei suuda viiruseid mõjutada. Siiski on täheldatud, et mitmed antibiootikumid (tetratsükliinid) on võimelised mõjuma suurtele viirustele.
Antibakteriaalsed ravimid on sünteetilised ravimid, millel puuduvad looduslikud analoogid ja millel on antibiootikumidele sarnane bakterite kasvu pärssiv toime.
Antibiootikumide leiutamist võib nimetada revolutsiooniks meditsiinis. Esimesed antibiootikumid olid penitsilliin ja streptomütsiin.
1. Antibiootikumide klassifikatsioon
Bakterirakule avalduva toime olemuse järgi:
1. bakteriostaatilised ravimid (peatavad bakterite kasvu ja paljunemise)
2. bakteritsiidsed ravimid (hävitavad bakterid)
Valmistamismeetodi järgi eristatakse antibiootikume:
1. loomulik
2. sünteetiline
3. poolsünteetiline
Vastavalt tegevussuunale on:
1. antibakteriaalne
2. kasvajavastane
3. seenevastane
Vastavalt toimespektrile on olemas:
1. laia toimespektriga antibiootikumid
2. kitsa toimespektriga antibiootikumid
Keemilise struktuuri järgi:
1. Beeta-laktaamantibiootikumid
Penitsilliinid toodavad seene Penicillinum kolooniad. On: biosünteetilisi (penitsilliin G - bensüülpenitsilliin), aminopenitsilliinid (amoksitsilliin, ampitsilliin, bekampitsilliin) ja poolsünteetilisi (oksatsilliin, metitsilliin, kloksatsilliin, dikloksatsilliin, flukloksatsilliin) penitsilliinid.
Tsefalosporiine kasutatakse penitsilliiniresistentsete bakterite vastu. Tsefalosporiine on: 1. (tseporiin, tsefaleksiin), 2. (tsefasoliin, tsefamesiin), 3. (tseftriaksoon, tsefotaksiim, tsefuroksiim) ja 4. (tsefepiim, tsefpiroom) põlvkond.
Karbapeneemid on laia toimespektriga antibiootikumid. Karbapeneemide struktuur määrab nende kõrge resistentsuse beeta-laktamaaside suhtes. Karbapeneemide hulka kuuluvad meropeneem (meroneem) ja imipineem.
Monobaktaamid (astreonaam)
2. Makroliidid on keerulise tsüklilise struktuuriga antibiootikumid, millel on bakteriostaatiline toime. Võrreldes teiste antibiootikumidega on need vähem toksilised. Nende hulka kuuluvad: erütromütsiin, oleandomütsiin, roksitromütsiin, asitromütsiin (Sumamed), klaritromütsiin jne. Makroliidide hulka kuuluvad ka: asaliidid ja ketoliidid.
3. Tetratsükliinid – kasutatakse hingamisteede ja kuseteede infektsioonide raviks, raskete infektsioonide, nagu siberi katk, tulareemia, brutselloos, raviks. Sellel on bakteriostaatiline toime. Need kuuluvad polüketiidide klassi. Nende hulgas on: looduslikud (tetratsükliin, oksütetratsükliin) ja poolsünteetilised (metatsükliin, kloortetriin, doksütsükliin) tetratsükliinid.
4. Aminoglükosiidid - selle antibiootikumide rühma ravimid on väga mürgised. Kasutatakse raskete infektsioonide, nagu veremürgistuse või peritoniit, raviks. Omab bakteritsiidset toimet. Aminoglükosiidid on aktiivsed gramnegatiivsete aeroobsete bakterite vastu. Nende hulka kuuluvad: streptomütsiin, gentamütsiin, kanamütsiin, neomütsiin, amikatsiin jne.
5. Levomütsetiinid – selle rühma antibiootikumide kasutamisel on oht tõsiste tüsistuste tekkeks – vererakke tootva luuüdi kahjustus. Sellel on bakteriostaatiline toime.
6. Glükopeptiidantibiootikumid rikuvad bakteriraku seina sünteesi. Sellel on bakteritsiidne toime, kuid selle rühma antibiootikumide bakteriostaatiline toime on võimalik enterokokkide, streptokokkide ja stafülokokkide suhtes. Nende hulka kuuluvad: vankomütsiin, teikoplaniin, daptomütsiin jne.
7. Linkosamiididel on bakteriostaatiline toime. Kõrgetes kontsentratsioonides võib see avaldada bakteritsiidset toimet väga tundlike mikroorganismide vastu. Nende hulka kuuluvad: linkomütsiin ja klindamütsiin
8. Tuberkuloosivastased ravimid - isoniasiid, ftivaziid, saluzid, metasiid, etionamiid, protionamiid.
9. Polüpeptiidid – selle rühma antibiootikumid sisaldavad oma molekulis polüpeptiidühendite jääke. Nende hulka kuuluvad: gramitsidiin, polümüksiinid M ja B, batsitratsiin, kolistiin;
10. Polüeenide hulka kuuluvad: amfoteritsiin B, nüstatiin, levoriin, natamütsiin
11. Erinevate rühmade antibiootikumid - Rifamütsiin, Ristomütsiinsulfaat, Fusidiin-naatrium jne.
12. Seenevastased ravimid - põhjustavad seenerakkude surma, hävitades nende membraani struktuuri. Neil on lüütiline toime.
13. Leepravastased ravimid - Diafenüülsulfoon, Solusulfoon, Diucifon.
14. Antratsükliinantibiootikumid – nende hulka kuuluvad kasvajavastased antibiootikumid – doksorubitsiin, karminomütsiin, rubomütsiin, aklarubitsiin.
2. Beeta-laktaamantibiootikumid
β-laktaamantibiootikumid (β-laktaamid), mida ühendab β-laktaamtsükli olemasolu struktuuris, on penitsilliinid, tsefalosporiinid, karbapeneemid ja monobaktaamid, millel on bakteritsiidne toime. Keemilise struktuuri sarnasus määrab kõigi β-laktaamide sama toimemehhanismi (bakteriraku seina sünteesi rikkumine), samuti mõnel patsiendil ristallergia nende suhtes.
Penitsilliinid, tsefalosporiinid ja monobaktaamid on tundlikud spetsiaalsete ensüümide – mitmete bakterite poolt toodetud β-laktamaaside – hüdrolüüsile. Karbapeneeme iseloomustab oluliselt suurem resistentsus β-laktamaaside suhtes.
Arvestades kõrget kliinilist efektiivsust ja madalat toksilisust, moodustavad β-laktaamantibiootikumid praeguses etapis antimikroobse kemoteraapia aluse, olles enamiku infektsioonide ravis juhtival kohal.
3. Penitsilliinid
Penitsilliinid on esimesed antimikroobsed ravimid, mis on välja töötatud mikroorganismide toodetud bioloogiliselt aktiivsete ainete baasil. Kõigi penitsilliinide esivanem bensüülpenitsilliin saadi XX sajandi 40ndate alguses. Praegu kuulub penitsilliinide rühma üle kümne antibiootikumi, mis olenevalt tootmisallikatest, struktuurilistest iseärasustest ja antimikroobsest toimest on jagatud mitmeks alarühmaks (tabel 1).
Üldised omadused:
1. Bakteritsiidne toime.
2. Madal toksilisus.
3. Eritumine peamiselt neerude kaudu.
4. Lai annustamisvahemik.
Ristallergia kõigi penitsilliinide ning osaliselt tsefalosporiinide ja karbapeneemide vahel.
looduslikud penitsilliinid. Looduslike penitsilliinide hulka kuuluvad sisuliselt ainult bensüülpenitsilliinid. Toimespektri põhjal võib sellesse rühma aga omistada ka prolongeeritud (bensüülpenitsilliini prokaiin, bensatiinbensüülpenitsilliin) ja suukaudsed (fenoksümetüülpenitsilliin, bensatiinfenoksümetüülpenitsilliin) derivaadid. Neid kõiki hävitavad β-laktamaasid, mistõttu neid ei saa kasutada stafülokoki infektsioonide raviks, kuna enamikul juhtudel toodavad stafülokokid β-laktamaase.
Poolsünteetilised penitsilliinid:
Antistafülokoki penitsilliinid
Laiendatud toimespektriga penitsilliinid
Antipseudomonaalsed penitsilliinid
4. Tsefalosporiinide rühm
Tsefalosporiinid on β-laktaamide esindajad. Neid peetakse üheks kõige ulatuslikumaks AMS-i klassiks. Nende madala toksilisuse ja kõrge efektiivsuse tõttu kasutatakse tsefalosporiine palju sagedamini kui teisi AMP-sid. Antimikroobne toime ja farmakokineetilised omadused määravad ühe või teise tsefalosporiini rühma antibiootikumi kasutamise. Kuna tsefalosporiinid ja penitsilliinid on struktuurilt sarnased, iseloomustab nende rühmade ravimeid sama antimikroobse toime mehhanism ja mõnedel patsientidel ka ristallergia.
Tsefalosporiine on 4 põlvkonda:
I põlvkond - tsefasoliin (parenteraalne kasutamine); tsefaleksiin, tsefadroksiil (suukaudne)
II põlvkond - tsefuroksiim (parenteraalne); tsefuroksiimaksetiil, tsefakloor (suukaudne)
III põlvkond - tsefotaksiim, tseftriaksoon, tseftasidiim, tsefoperasoon, tsefoperasoon / sulbaktaam (parenteraalne); tsefiksiim, tseftibuteen (suukaudne)
IV põlvkond - tsefepiim (parenteraalne).
Toimemehhanism. Tsefalosporiinide toime on bakteritsiidne. Bakterite penitsilliini siduvad valgud, mis toimivad ensüümidena peptidoglükaani sünteesi lõppfaasis (biopolümeer, bakteriraku seina põhikomponent), langevad tsefalosporiinide mõju alla. Peptidoglükaani sünteesi blokeerimise tagajärjel bakter sureb.
Tegevuse spekter. I kuni III põlvkonna tsefalosporiine iseloomustab kalduvus laiendada aktiivsuse ulatust, samuti antimikroobse toime taseme tõus gramnegatiivsete mikroorganismide suhtes ja aktiivsuse taseme langus grampositiivsete bakterite suhtes.
Ühine kõigile tsefalosporiinidele - see on olulise toime puudumine L.monocytogenes'i, MRSA ja enterokokkide vastu. KNS on tsefalosporiinide suhtes vähem tundlik kui S.aureus.
Esimese põlvkonna tsefalosporiinid. Neil on sarnane antimikroobne toimespekter järgmise erinevusega: parenteraalseks manustamiseks mõeldud ravimid (tsefasoliin) toimivad tugevamalt kui suukaudsed ravimid (tsefadroksiil, tsefaleksiin). Antibiootikumid on vastuvõtlikud metitsilliinitundlikele Staphylococcus spp. ja Streptococcus spp. (S.pneumoniae, S.pyogenes). Esimese põlvkonna tsefalosporiinidel on väiksem pneumokokkide vastane toime kui aminopenitsilliinidel ja enamikul järgmise põlvkonna tsefalosporiinidel. Tsefalosporiinid ei avalda üldiselt mingit mõju listeriatele ja enterokokkidele, mis on selle antibiootikumide klassi kliiniliselt oluline tunnus. On leitud, et tsefalosporiinid on resistentsed stafülokoki β-laktamaaside toime suhtes, kuid vaatamata sellele võivad mõned tüved (nende ensüümide hüpertootjad) olla nende suhtes mõõdukalt tundlikud. Esimese põlvkonna tsefalosporiinid ja penitsilliinid ei ole pneumokokkide vastu aktiivsed. I põlvkonna tsefalosporiinidel on kitsas toimespekter ja madal aktiivsus gramnegatiivsete bakterite vastu. Nende toime laieneb Neisseria spp.-le, kuid selle fakti kliiniline tähtsus on piiratud. 1. põlvkonna tsefalosporiinide aktiivsus M. catarrhalis ja H. influenzae vastu on kliiniliselt ebaoluline. M. catarrhalis'e puhul on nad looduslikult üsna aktiivsed, kuid nad on tundlikud β-laktamaaside hüdrolüüsi suhtes, tekitades peaaegu 100% tüvedest. Enterobacteriaceae perekonna esindajad on vastuvõtlikud 1. põlvkonna tsefalosporiinide mõjule: P.mirabilis, Salmonella spp., Shigella spp., E.coli ning Shigella ja Salmonella vastase toimel puudub kliiniline tähtsus. P.mirabilise ja E.coli tüvedele, mis provotseerivad kogukonnas omandatud (eriti haiglanakkusi), on laialt levinud omandatud resistentsus, mis on tingitud laiendatud ja laia toimespektriga β-laktamaaside tootmisest.
Teistes Enterobacteriaceae bakterites on mittekäärivad bakterid ja Pseudomonas spp. leiti vastupanu.
B.fragilis ja sellega seotud mikroorganismid näitavad resistentsust ning paljude anaeroobide esindajad - tundlikkust 1. põlvkonna tsefalosporiinide toime suhtes.
TsefalosporiinidIIpõlvkonnad. Tsefuroksiim ja tsefakloor, kaks selle põlvkonna esindajat, erinevad üksteisest: sarnase antimikroobse toimespektriga tsefuroksiim näitas tsefaklooriga võrreldes suuremat aktiivsust Staphylococcus spp. ja Streptococcus spp. Mõlemad ravimid ei ole aktiivsed Listeria, Enterococcus ja MRSA vastu.
Pneumokokid näitavad PR-i penitsilliini ja teise põlvkonna tsefalosporiinide suhtes. 2. põlvkonna tsefalosporiinide esindajaid iseloomustab laiem toimespekter gramnegatiivsetele mikroorganismidele kui 1. põlvkonna tsefalosporiinidele. Nii tsefuroksiim kui ka tsefakloor näitavad aktiivsust Neisseria spp. vastu, kuid ainult tsefuroksiimi toime gonokokkidele on osutunud kliiniliselt aktiivseks. Haemophilus spp. ja M. catarrhalist mõjutab tsefuroksiim tugevamalt, kuna nad on resistentsed β-laktamaaside hüdrolüüsi suhtes ja need ensüümid hävitavad osaliselt tsefakloori. Enterobacteriaceae perekonna esindajatest ei esine mitte ainult P.mirabilis, Salmonella spp., Shigella spp., E.coli, vaid ka C.diversus, P.vulgaris, Klebsiella spp. Kui ülalloetletud mikroorganismid toodavad laia toimespektriga β-laktamaase, säilitavad nad tundlikkuse tsefuroksiimi suhtes. Tsefaklooril ja tsefuroksiimil on omapära: neid hävitavad laiendatud spektriga β-laktamaasid. Mõned P.rettgeri, P.stuartii, M.morganii, Serratia spp., C.freundii, Enterobacter spp. in vitro võib tekkida mõõdukas tundlikkus tsefuroksiimi suhtes, kuid seda ravimit ei ole mõtet kasutada ülalnimetatud bakterite põhjustatud infektsioonide ravis. II põlvkonna tsefalosporiinide toime ei kehti B. fragilis rühma anaeroobide, Pseudomonase ja teiste mittekäärivate mikroorganismide suhtes.
3. põlvkonna tsefalosporiinid. III põlvkonna tsefalosporiinidel on koos ühiste tunnustega teatud tunnused. Tseftriaksoon ja tsefotaksiim on selle rühma põhilised AMP-d ja praktiliselt ei erine üksteisest oma antimikroobse toime poolest. Mõlemal ravimil on aktiivne toime Streptococcus spp.-le ning samal ajal jääb märkimisväärne osa pneumokokkidest, aga ka penitsilliini suhtes resistentsetest rohetavatest streptokokkidest tundlikuks tseftriaksooni ja tsefotaksiimi suhtes. Tsefotaksiimi ja tseftriaksooni toime mõjutab S.aureust (välja arvatud MRSA) ja vähemal määral KNS-i. Korünebakterid (va C. jeikeium) kipuvad olema tundlikud. Resistentsust näitavad B.cereus, B.antracis, L.monocytogenes, MRSA ja enterokokid. Tseftriaksoon ja tsefotaksiim näitavad kõrget aktiivsust H. influenzae, M. catarrhalis, gonokokkide ja meningokokkide vastu, sealhulgas tüvede suhtes, millel on vähenenud tundlikkus penitsilliini suhtes, sõltumata resistentsuse mehhanismist. Peaaegu kõik Enterobacteriaceae perekonna esindajad, sh. mikroorganismid, mis toodavad laia toimespektriga β-laktamaase, on vastuvõtlikud tsefotaksiimi ja tseftriaksooni aktiivsele loomulikule toimele. E. coli ja Klebsiella spp. omavad resistentsust, enamasti ESBL-i tootmise tõttu. C-klassi kromosomaalsete β-laktamaaside hüperproduktsioon põhjustab tavaliselt resistentsuse P. rettgeri, P. stuartii, M. morganii, Serratia spp., C. freundii, Enterobacter spp.
Mõnikord avaldub tsefotaksiimi ja tseftriaksooni aktiivsus in vitro teatud P. aeruginosa tüvede, teiste mittekäärivate mikroorganismide, aga ka B. fragilis'e suhtes, kuid sellest ei piisa, et neid saaks kasutada asjakohaste infektsioonide ravis. .
Tseftasidiimi, tsefoperasooni ja tsefotaksiimi, tseftriaksooni vahel on peamistes antimikroobsetes omadustes sarnasusi. Tseftasidiimi ja tsefoperasooni eristavad omadused tsefotaksiimist ja tseftriaksoonist:
Näidata suurt tundlikkust ESBL hüdrolüüsi suhtes;
Need näitavad oluliselt vähem aktiivsust streptokokkide, peamiselt S.pneumoniae vastu;
Tugev aktiivsus (eriti tseftasidiimis) P. aeruginosa ja teiste mittekäärivate mikroorganismide vastu.
Tsefiksiimi ja tseftibuteeni erinevused tsefotaksiimist ja tseftriaksoonist:
Mõlemal ravimil puudub või on väike toime P.rettgeri, P.stuartii, M.morganii, Serratia spp., C.freundii, Enterobacter spp.;
Tseftibuteen on viridestseeruvate streptokokkide ja pneumokokkide suhtes inaktiivne, tseftibuteen mõjutab neid vähe;
Staphylococcus spp. vastu olulist toimet ei ole.
IV põlvkonna tsefalosporiinid. Tsefepiimi ja kolmanda põlvkonna tsefalosporiinide vahel on palju sarnasusi. Kuid keemilise struktuuri iseärasused võimaldavad tsefepiimil suurema kindlusega tungida läbi gramnegatiivsete mikroorganismide välismembraani ning omada suhtelist resistentsust C-kromosomaalse klassi β-laktamaaside hüdrolüüsi suhtes. Põhilistel III põlvkonna tsefalosporiinidel (tseftriaksoon, tsefotaksiim) on tsefepiimil järgmised omadused:
Kõrge aktiivsus mittekäärivate mikroorganismide ja P.aeruginosa vastu;
Suurenenud resistentsus laiendatud spektriga β-laktamaaside hüdrolüüsi suhtes (see asjaolu ei määra täielikult selle kliinilist tähtsust);
Mõju järgmistele mikroorganismidele - C-klassi kromosomaalsete β-laktamaaside hüperproduktsioonidele: P.rettgeri, P.stuartii, M.morganii, Serratia spp., C.freundii, Enterobacter spp.
Inhibiitoriga kaitstud tsefalosporiinid. Tsefoperasoon / sulbaktaam on selle β-laktaamide rühma ainus esindaja. Võrreldes tsefoperasooniga on kombineeritud ravimil anaeroobsetele mikroorganismidele avalduva toime tõttu laiem toimespekter. Samuti mõjutab ravim enamikku enterobakterite tüvesid, mis toodavad laiendatud ja laia spektriga β-laktamaase. Sulbaktaami antibakteriaalne toime võimaldab sellel AMP-l olla kõrge aktiivsus Acinetobacter spp.
Farmakokineetika. Suukaudsed tsefalosporiinid imenduvad seedetraktis hästi. Konkreetne ravim eristub selle biosaadavuse poolest, mis varieerub vahemikus 40–50% (tsefiksiim) ja 95% (tsefakloor, tsefadroksiil ja tsefaleksiini). Toidu olemasolu võib tseftibuteeni, tsefiksiimi ja tsefakloori imendumist mõnevõrra aeglustada. Toit aitab tsefuroksiimaksetiili imendumise ajal aktiivset tsefuroksiimi vabastada. / m kasutuselevõtuga täheldati parenteraalsete tsefalosporiinide head imendumist. Tsefalosporiinide jaotus toimub paljudes elundites (välja arvatud eesnääre), kudedes ja saladustes. Kõrgeid kontsentratsioone täheldatakse kõhukelme-, pleura-, perikardi- ja sünoviaalvedelikes, luudes, pehmetes kudedes, nahas, lihastes, maksas, neerudes ja kopsudes. Tsefoperasoon ja tseftriaksoon toodavad sapis kõrgeima taseme. Tsefalosporiinid, eriti tseftasidiim ja tsefuroksiim, suudavad tungida hästi vesivedelikku, tekitamata silma tagumises kambris terapeutilist taset. III põlvkonna tsefalosporiinidel (tseftasidiim, tseftriaksoon, tsefotaksiim) ja IV põlvkonna tsefalosporiinidel (tsefepiim) on suurim võime läbida BBB-d ja luua ka terapeutilisi kontsentratsioone CSF-s. Tsefuroksiim ületab mõõdukalt BBB-d ainult ajukelme põletiku korral.
Enamikul tsefalosporiinidel (välja arvatud tsefotaksiim, mis biotransformeerub aktiivseks metaboliidiks) puudub võime metaboliseerida. Ravimite eemaldamine toimub peamiselt neerude kaudu, tekitades samal ajal väga kõrge kontsentratsiooni uriinis. Tseftriaksoonil ja tsefoperasoonil on kahekordne eritumine – maksa ja neerude kaudu. Enamiku tsefalosporiinide eliminatsiooni poolväärtusaeg on 1 kuni 2 tundi. Tseftibuteeni, tsefiksiimi eristab pikem periood - 3-4 tundi, tseftriaksoonis suureneb see 8,5 tunnini. Tänu sellele indikaatorile võib neid ravimeid võtta 1 kord päevas. Neerupuudulikkusega kaasneb tsefalosporiinide rühma kuuluvate antibiootikumide (välja arvatud tsefoperasoon ja tseftriaksoon) annustamisskeemi korrigeerimine.
Esimese põlvkonna tsefalosporiinid. Põhimõtteliselt täna tsefasoliin kasutatakse kirurgias perioperatiivse profülaktikana. Seda kasutatakse ka pehmete kudede ja naha infektsioonide korral.
Kuna tsefasoliinil on kitsas toimespekter ja resistentsus tsefalosporiinide suhtes on potentsiaalsete patogeenide seas levinud, ei ole tsefasoliini kasutamise soovitused hingamisteede infektsioonide ja kuseteede infektsioonide raviks praegu piisavalt põhjendatud.
Tsefaleksiini kasutatakse streptokoki põhjustatud tonsillofarüngiidi (teise valiku ravimina), samuti pehmete kudede ja naha kerge kuni mõõduka raskusega kogukonnas omandatud infektsioonide raviks.
II põlvkonna tsefalosporiinid
Tsefuroksiim kasutatud:
kogukonnas omandatud kopsupõletikuga, mis vajab haiglaravi;
Pehmete kudede ja naha kogukonnas omandatud infektsioonidega;
Kuseteede infektsioonid (keskmise ja raske raskusega püelonefriit); antibiootikum tsefalosporiin tetratsükliin tuberkuloosivastane
Perioperatiivse profülaktikana kirurgias.
tsefakloor, tsefuroksiimaksetiil kasutatud:
URT ja NDP infektsioonidega (kogukonnast omandatud kopsupõletik, kroonilise bronhiidi ägenemine, äge sinusiit, CCA);
Kerge, mõõduka raskusega pehmete kudede ja naha kogukonnas omandatud infektsioonidega;
Kuseteede infektsioonid (äge tsüstiit ja püelonefriit lastel, püelonefriit naistel imetamise ajal, kerge ja mõõduka raskusega püelonefriit).
Tsefuroksiimaksetiili ja tsefuroksiimi võib kasutada astmelise ravina.
3. põlvkonna tsefalosporiinid
Tseftriaksoon, tsefotaksiim kasutatud:
Kogukonnas omandatud infektsioonid - äge gonorröa, CCA (tseftriaksoon);
Rasked haigla- ja kogukonnas omandatud infektsioonid - sepsis, meningiit, generaliseerunud salmonelloos, vaagnaelundite infektsioonid, intraabdominaalsed infektsioonid, rasked liigeste, luude, pehmete kudede ja naha infektsioonid, kuseteede infektsioonide rasked vormid, NDP infektsioonid .
Tsefoperasoon, tseftasidiim ette nähtud:
Erineva lokalisatsiooniga raskete kogukonnast omandatud ja haiglanakkuste ravi P. aeruginosa ja teiste mittekäärivate mikroorganismide kinnitatud või võimalike etioloogiliste mõjude korral.
Infektsioonide ravi immuunpuudulikkuse ja neutropeenia taustal (sealhulgas neutropeeniline palavik).
Kolmanda põlvkonna tsefalosporiine võib kasutada parenteraalselt monoteraapiana või koos teiste rühmade antibiootikumidega.
tseftibuteen, tsefiksiim tõhus:
Kuseteede infektsioonid: äge tsüstiit ja püelonefriit lastel, püelonefriit naistel raseduse ja imetamise ajal, kerge ja mõõduka raskusega püelonefriit;
Gramnegatiivsete bakterite põhjustatud mitmesuguste raskete haigla- ja kogukonnas omandatud infektsioonide järkjärgulise ravi suukaudse etapi rollis pärast parenteraalseks manustamiseks mõeldud ravimite püsiva toime saavutamist;
Ülemiste hingamisteede ja ülemiste hingamisteede infektsioonidega (tseftibuteeni võtmine võimaliku pneumokoki etioloogia korral ei ole soovitatav).
Tsefoperasoon/sulbaktaam rakendada:
Sega (aeroobne-anaeroobse) ja multiresistentse mikrofloora poolt põhjustatud raskete (peamiselt haiglaravi) infektsioonide ravis - sepsis, NDP-nakkused (pleura empüeem, kopsuabstsess, kopsupõletik), tüsistunud kuseteede infektsioonid, väikese vaagna intraabdominaalsed infektsioonid;
Neutropeenia ja teiste immuunpuudulikkuse seisundite taustal esinevate infektsioonidega.
IV põlvkonna tsefalosporiinid. Seda kasutatakse raskete, peamiselt haiglate põhjustatud infektsioonide korral, mille on esile kutsunud multiresistentne mikrofloora:
intraabdominaalsed infektsioonid;
Liigeste, luude, naha ja pehmete kudede infektsioonid;
Kuseteede tüsistunud infektsioonid;
NDP infektsioonid (pleura empüeem, kopsuabstsess, kopsupõletik).
Samuti on IV põlvkonna tsefalosporiinid tõhusad infektsioonide ravis neutropeenia taustal, aga ka muude immuunpuudulikkuse seisundite korral.
Vastunäidustused
Mitte kasutada tsefalosporiinide suhtes allergiliste reaktsioonide korral.
5. Karbapeneemide rühm
Karbapeneemid (imipeneem ja meropeneem) on β-laktaamid. Võrreldes penitsilliinid ja tsefalosporiinid, on need bakterite hüdrolüüsiva toime suhtes vastupidavamad sisse-laktamaas, kaasa arvatud ESBL ja neil on laiem tegevusspekter. Neid kasutatakse erineva lokaliseerimisega raskete infektsioonide, sealhulgas haiglane, sagedamini reservravimina, kuid eluohtlike infektsioonide puhul võib seda pidada esmavaliku empiiriliseks raviks.
Toimemehhanism. Karbapeneemidel on bakteriraku seina moodustumise rikkumise tõttu võimas bakteritsiidne toime. Võrreldes teiste β-laktaamidega, suudavad karbapeneemid kiiremini tungida läbi gramnegatiivsete bakterite välismembraani ja lisaks avaldavad neile tugevat PAE-d.
Tegevuse spekter. Karbapeneemid toimivad paljudele grampositiivsetele, gramnegatiivsetele ja anaeroobsetele mikroorganismidele.
Stafülokokid on karbapeneemide suhtes tundlikud (v.a MRSA), streptokokid, sealhulgas S.pneumoniae(ARP-vastase toime poolest on karbapeneemid halvemad vankomütsiin), gonokokid, meningokokid. Imipeneem toimib E.faecalis.
Karbapeneemid on väga aktiivsed enamiku perekonna gramnegatiivsete bakterite vastu Enterobakterid(E. coli, Klebsiella, Proteus, Enterobacter, Citrobacter, Acinetobacter, Morganella), sealhulgas resistentsete tüvede vastu tsefalosporiinid III-IV põlvkonna ja inhibiitoritega kaitstud penitsilliinid. Veidi madalam aktiivsus proteuside, hammaste, H.influenzae. Enamik tüvesid P.aeruginosa algselt tundlik, kuid karbapeneemide kasutamise käigus täheldatakse resistentsuse suurenemist. Seega on Venemaal aastatel 1998-1999 läbi viidud multikeskuse epidemioloogilise uuringu kohaselt haiglatüvede resistentsus imipeneemi suhtes. P.aeruginosa ICU-s oli 18,8%.
Karbapeneemidel on suhteliselt väike toime B.cepacia, stabiilne on S. maltophilia.
Karbapeneemid on väga aktiivsed eoste tekke vastu (v.a C.difficile) ja mitteeoseid moodustavaid (kaasa arvatud B. fragilis) anaeroobid.
Mikroorganismide sekundaarne resistentsus (v.a P.aeruginosa) areneb harva karbapeneemideks. Resistentsete patogeenide puhul (v.a P.aeruginosa) iseloomustab ristresistentsus imipeneemi ja meropeneemi suhtes.
Farmakokineetika. Karbapeneeme kasutatakse ainult parenteraalselt. Need on kehas hästi jaotunud, luues terapeutilise kontsentratsiooni paljudes kudedes ja sekretsioonides. Ajukelme põletikuga tungivad nad BBB-sse, luues CSF-s kontsentratsiooni, mis võrdub 15-20% vereplasma tasemest. Karbapeneemid ei metaboliseeru, need erituvad peamiselt neerude kaudu muutumatul kujul, seetõttu on neerupuudulikkuse korral võimalik nende eliminatsiooni märkimisväärne aeglustumine.
Kuna imipeneem inaktiveeritakse neerutuubulites ensüümi dehüdropeptidaas I toimel ja see ei tekita uriinis terapeutilisi kontsentratsioone, kasutatakse seda kombinatsioonis tsilastatiiniga, mis on dehüdropeptidaas I selektiivne inhibiitor.
Hemodialüüsi ajal eemaldatakse karbapeneemid ja tsilastatiin kiiresti verest.
Näidustused:
1. Rasked infektsioonid, enamasti haiglased, põhjustatud multiresistentsest ja segamikrofloorast;
2. JaNDP-nakkused(kopsupõletik, kopsuabstsess, pleura empüeem);
3. Keeruline kuseteede infektsioon;
4. Jaintraabdominaalsed infektsioonid;
5. Javaagnapiirkonna infektsioonid;
6. FROMepsis;
7. Janaha ja pehmete kudede infektsioonid;
8. Ja luude ja liigeste infektsioonid(ainult imipeneem);
9. Eendokardiit(ainult imipeneem);
10. Bakteriaalsed infektsioonid neutropeeniaga patsientidel;
11. Meningiit(ainult meropeneem).
Vastunäidustused. Allergiline reaktsioon karbapeneemidele. Imipeneem/tsilastatiini ei tohi kasutada ka patsientidel, kellel on tsilastatiini suhtes allergiline reaktsioon.
6. Monobaktaamide rühm
Monobaktaamidest ehk monotsüklilistest β-laktaamidest kasutatakse kliinilises praktikas ühte antibiootikumi - aztreonaam. Sellel on kitsas antibakteriaalse toime spekter ja seda kasutatakse aeroobse gramnegatiivse taimestiku põhjustatud infektsioonide raviks.
Toimemehhanism. Aztreonaamil on bakteritsiidne toime, mis on seotud bakteriraku seina moodustumise rikkumisega.
Tegevuse spekter. Astreonaami antimikroobse toimespektri eripära on tingitud asjaolust, et see on resistentne paljude aeroobse gramnegatiivse taimestiku poolt toodetud β-laktamaaside suhtes ja samal ajal hävitatakse stafülokokkide, bakteroidide ja ESBL β-laktamaaside poolt.
Astreonaami toime paljude perekonna mikroorganismide vastu Enterobakterid (E. coli, Enterobacter, Klebsiella, Proteus, Serration, Citrobacter, Providence, Morganella) ja P.aeruginosa, sealhulgas aminoglükosiidide, ureidopenitsilliinide ja tsefalosporiinide suhtes resistentsete haiglatüvede vastu.
Aztreonaam ei mõjuta Acinetobacter'i, S. maltophilia, B.cepacia, grampositiivsed kokid ja anaeroobid.
Farmakokineetika. Aztreonaami kasutatakse ainult parenteraalselt. See on jaotunud paljudes keha kudedes ja keskkondades. See läbib BBB-d ajukelme põletiku ajal, läbi platsenta ja rinnapiima. See metaboliseerub maksas väga vähesel määral, eritub peamiselt neerude kaudu, muutumatul kujul 60-75%. Poolväärtusaeg normaalse neeru- ja maksafunktsiooni korral on 1,5-2 tundi, maksatsirroosi korral võib see pikeneda 2,5-3,5 tunnini, neerupuudulikkuse korral - kuni 6-8 tundi.Hemodialüüsi ajal on astreonaami kontsentratsioon veres. veri väheneb 25-60%.
Näidustused. Aztreonaam on reservravim aeroobsete gramnegatiivsete bakterite põhjustatud erineva lokaliseerimisega infektsioonide raviks:
1. NDP-nakkused (kogukonnast omandatud ja nosokomiaalne kopsupõletik);
2. intraabdominaalsed infektsioonid;
3. vaagnaelundite infektsioonid;
4. kuseteede infektsioonid;
5. naha, pehmete kudede, luude ja liigeste infektsioonid;
6. sepsis.
Arvestades astreonaami kitsast antimikroobse toimespektriga, tuleb seda raskete infektsioonide empiirilises ravis määrata kombinatsioonis AMP-dega, mis on aktiivsed grampositiivsete kokkide (oksatsilliin, tsefalosporiinid, linkosamiidid, vankomütsiin) ja anaeroobide (metronidasool) vastu.
Vastunäidustused. Allergilised reaktsioonid astreonaamile ajaloos.
7. Tetratsükliini rühm
Tetratsükliinid on üks AMP-de varajastest klassidest, esimesed tetratsükliinid saadi 40ndate lõpus. Praegu on nendele ravimitele iseloomulike tetratsükliinide suhtes resistentsete mikroorganismide ja arvukate HP-de ilmnemise tõttu nende kasutamine piiratud. Tetratsükliinid (looduslik tetratsükliin ja poolsünteetiline doksütsükliin) säilitavad oma suurima kliinilise tähtsuse klamüüdiainfektsioonide, riketsioosi, mõnede zoonooside ja raske akne korral.
Toimemehhanism. Tetratsükliinidel on bakteriostaatiline toime, mis on seotud valkude sünteesi häirega mikroobirakus.
tegevuse spekter. Tetratsükliine peetakse laia antimikroobse toime spektriga AMP-deks, kuid nende pikaajalise kasutamise käigus on paljud bakterid omandanud nende suhtes resistentsuse.
Gram-positiivsetest kokkidest on pneumokokk kõige vastuvõtlikum (välja arvatud ARP). Samal ajal on üle 50% tüvedest resistentsed S.pyogenes, enam kui 70% nosokomiaalsetest stafülokokkide tüvedest ja valdav enamus enterokokkide tüvedest. Kõige vastuvõtlikumad gramnegatiivsed kokid on meningokokid ja M.catarrhalis, ja paljud gonokokid on resistentsed.
Tetratsükliinid mõjutavad mõningaid grampositiivseid ja gramnegatiivseid vardaid – listeria, H. influenzae, H. ducreyi, Yersinia, Campylobacter (kaasa arvatud H. pylori), brutsella, bartonella, vibrioosid (sh koolera), kubemegranuloomi patogeenid, siberi katk, katk, tulareemia. Enamik Escherichia coli, Salmonella, Shigella, Klebsiella, Enterobacter tüvesid on resistentsed.
Tetratsükliinid on aktiivsed spiroheetide, leptospira, borrelia, riketsia, klamüüdia, mükoplasmade, aktinomütseedide ja mõnede algloomade vastu.
Anaeroobsest taimestikust on klostriidid tundlikud tetratsükliinide suhtes (v.a C.difficile), fusobakterid, p.aknes. Enamik bakteroidide tüvesid on resistentsed.
Farmakokineetika. Suukaudsel manustamisel imenduvad tetratsükliinid hästi, doksütsükliin on parem kui tetratsükliin. Doksütsükliini biosaadavus ei muutu ja tetratsükliin väheneb toidu mõjul 2 korda. Ravimite maksimaalne kontsentratsioon vereseerumis tekib 1-3 tundi pärast allaneelamist. Intravenoosse manustamise korral saavutatakse veres oluliselt kõrgem kontsentratsioon kui suukaudsel manustamisel.
Tetratsükliinid jaotuvad paljudes kehaorganites ja keskkondades ning doksütsükliin tekitab kudedes kõrgemaid kontsentratsioone kui tetratsükliin. Kontsentratsioon tserebrospinaalvedelikus on 10-25% seerumi tasemest, kontsentratsioon sapis on 5-20 korda kõrgem kui veres. Tetratsükliinidel on suur võime läbida platsentat ja tungida rinnapiima.
Hüdrofiilse tetratsükliini eritumine toimub peamiselt neerude kaudu, seetõttu on neerupuudulikkuse korral selle eritumine oluliselt häiritud. Lipofiilsem doksütsükliin eritub mitte ainult neerude, vaid ka seedetrakti kaudu ning neerufunktsiooni kahjustusega patsientidel on see tee peamine. Doksütsükliinil on tetratsükliiniga võrreldes 2-3 korda pikem poolväärtusaeg. Hemodialüüsiga eemaldatakse tetratsükliin aeglaselt ja doksütsükliin ei eemaldata üldse.
Näidustused:
1. Klamüüdiainfektsioonid (psittakoos, trahhoom, uretriit, prostatiit, emakakaela põletik).
2. Mükoplasma infektsioonid.
3. Borrelioos (borrelioos, korduv palavik).
4. Riketsioos (Q-palavik, Rocky Mountaini täpiline palavik, tüüfus).
5. Bakteriaalsed zoonoosid: brutselloos, leptospiroos, siberi katk, katk, tulareemia (viimasel kahel juhul - kombinatsioonis streptomütsiini või gentamütsiiniga).
6. NDP infektsioonid: kroonilise bronhiidi ägenemine, kogukonnas omandatud kopsupõletik.
7. Sooleinfektsioonid: koolera, jersinioos.
8. Günekoloogilised infektsioonid: adneksiit, salpingooforiit (rasketel juhtudel kombinatsioonis β-laktaamide, aminoglükosiidide, metronidasooliga).
9. Akne.
10. Rosaatsea.
11. Haavainfektsioon pärast loomahammustust.
12. STI-d: süüfilis (allergiline penitsilliini suhtes), kubeme granuloom, suguelundite lümfogranuloom.
13. Silmapõletikud.
14. Aktinomükoos.
15. Batsillaar angiomatoos.
16. Likvideerimine H. pylori mao ja kaksteistsõrmiksoole peptilise haavandiga (tetratsükliin kombinatsioonis sekretsioonivastaste ravimite, vismutsubtsitraadi ja teiste AMP-dega).
17. Troopilise malaaria ennetamine.
Vastunäidustused:
Vanus kuni 8 aastat.
Rasedus.
Imetamine.
Raske maksahaigus.
Neerupuudulikkus (tetratsükliin).
8. Aminoglükosiidide rühm
Aminoglükosiidid on üks esimesi antibiootikumide klasse. Esimene aminoglükosiid, streptomütsiin, saadi aastal 1944. Praegu on aminoglükosiide kolm põlvkonda.
Aminoglükosiidide peamine kliiniline tähtsus on aeroobsete gramnegatiivsete patogeenide põhjustatud haiglanakkuste, aga ka infektsioosse endokardiidi ravis. Tuberkuloosi ravis kasutatakse streptomütsiini ja kanamütsiini. Neomütsiini kui aminoglükosiidide seas kõige toksilisemat kasutatakse ainult suukaudselt ja paikselt.
Aminoglükosiididel on potentsiaalne nefrotoksilisus, ototoksilisus ja need võivad põhjustada neuromuskulaarset blokaadi. Võttes arvesse riskitegureid, võib kogu päevaannuse ühekordne manustamine, lühikesed ravikuurid ja TDM siiski vähendada HP avaldumise astet.
Toimemehhanism. Aminoglükosiididel on bakteritsiidne toime, mis on seotud ribosoomide valgusünteesi häirega. Aminoglükosiidide antibakteriaalse toime aste sõltub nende maksimaalsest (tipp) kontsentratsioonist vereseerumis. Kombineerituna penitsilliinide või tsefalosporiinidega täheldatakse sünergiat mõnede gramnegatiivsete ja grampositiivsete aeroobsete mikroorganismide suhtes.
Tegevuse spekter. II ja III põlvkonna aminoglükosiide iseloomustab annusest sõltuv bakteritsiidne toime perekonna gramnegatiivsete mikroorganismide vastu Enterobakterid (E. coli, Proteus spp., Klebsiella spp., Enterobakter spp., Serratia spp. jne), samuti mittekäärivad gramnegatiivsed vardad ( P.aeruginosa, Acinetobacter spp.). Aminoglükosiidid on aktiivsed stafülokokkide vastu, välja arvatud MRSA. Streptomütsiin ja kanamütsiin toimivad M.tuberculosis, samas kui amikatsiin on selle vastu aktiivsem M.avium ja muud ebatüüpilised mükobakterid. Streptomütsiin ja gentamütsiin mõjutavad enterokokke. Streptomütsiin on aktiivne katku, tulareemia, brutselloosi patogeenide vastu.
Aminoglükosiidid on nende vastu passiivsed S.pneumoniae, S. maltophilia, B.cepacia, anaeroobid ( Bacteroides spp., Clostridium spp. ja jne). Pealegi vastupanu S.pneumoniae, S. maltophilia ja B.cepacia aminoglükosiididele võib nende mikroorganismide tuvastamiseks kasutada.
Kuigi aminoglükosiidid sisse vitro aktiivne hemofiili, shigella, salmonella, legionella vastu, kliiniline efektiivsus nende patogeenide põhjustatud infektsioonide ravis ei ole tõestatud.
Farmakokineetika. Suukaudsel manustamisel aminoglükosiidid praktiliselt ei imendu, seetõttu kasutatakse neid parenteraalselt (välja arvatud neomütsiin). Pärast i / m manustamist imenduvad need kiiresti ja täielikult. Maksimaalne kontsentratsioon tekib 30 minutit pärast intravenoosse infusiooni lõppu ja 0,5-1,5 tundi pärast intramuskulaarset süstimist.
Aminoglükosiidide tippkontsentratsioonid on erinevatel patsientidel erinevad, kuna need sõltuvad jaotusmahust. Jaotusruumala sõltub omakorda kehakaalust, vedeliku ja rasvkoe mahust ning patsiendi seisundist. Näiteks patsientidel, kellel on ulatuslikud põletused, astsiit, suureneb aminoglükosiidide jaotusruumala. Vastupidi, dehüdratsiooni või lihasdüstroofia korral see väheneb.
Aminoglükosiidid jaotuvad rakuvälisesse vedelikku, sealhulgas seerumis, abstsessi eksudaatidesse, astsiidi-, perikardi-, pleura-, sünoviaal-, lümfi- ja peritoneaalvedelikku. Võimeline tekitama kõrgeid kontsentratsioone hea verevarustusega elundites: maks, kopsud, neerud (kus need kogunevad kortikaalsesse ainesse). Madalat kontsentratsiooni täheldatakse rögas, bronhide sekretsioonis, sapis, rinnapiimas. Aminoglükosiidid ei läbi BBB-d hästi. Ajukelme põletikuga suureneb läbilaskvus veidi. Vastsündinutel saavutatakse CSF-s suurem kontsentratsioon kui täiskasvanutel.
Aminoglükosiidid ei metaboliseeru, need erituvad neerude kaudu muutumatul kujul glomerulaarfiltratsiooni teel, tekitades uriinis kõrge kontsentratsiooni. Eritumise kiirus sõltub patsiendi vanusest, neerufunktsioonist ja kaasuvatest haigustest. Palavikuga patsientidel võib see suureneda, neerufunktsiooni langusega oluliselt aeglustada. Eakatel võib glomerulaarfiltratsiooni vähenemise tagajärjel eritumine samuti aeglustuda. Kõigi aminoglükosiidide poolväärtusaeg normaalse neerufunktsiooniga täiskasvanutel on 2-4 tundi, vastsündinutel - 5-8 tundi, lastel - 2,5-4 tundi Neerupuudulikkuse korral võib poolväärtusaeg pikeneda 70 tunnini või rohkemgi .
Näidustused:
1. Empiiriline teraapia(enamikul juhtudel määratakse kombinatsioonis β-laktaamide, glükopeptiidide või anaeroobsete ravimitega, olenevalt kahtlustatavatest patogeenidest):
Tundmatu etioloogiaga sepsis.
Nakkuslik endokardiit.
Posttraumaatiline ja postoperatiivne meningiit.
Palavik neutropeeniaga patsientidel.
Nosokomiaalne kopsupõletik (kaasa arvatud ventilatsioon).
Püelonefriit.
intraabdominaalsed infektsioonid.
Vaagnaelundite infektsioonid.
Diabeetiline jalg.
Postoperatiivne või traumajärgne osteomüeliit.
Septiline artriit.
Kohalik teraapia:
Silmainfektsioonid - bakteriaalne konjunktiviit ja keratiit.
2. Spetsiifiline teraapia:
Katk (streptomütsiin).
Tulareemia (streptomütsiin, gentamütsiin).
Brutselloos (streptomütsiin).
Tuberkuloos (streptomütsiin, kanamütsiin).
Antibiootikumide profülaktika:
Soolestiku puhastamine enne plaanilist käärsooleoperatsiooni (neomütsiin või kanamütsiin kombinatsioonis erütromütsiiniga).
Aminoglükosiide ei tohi kasutada kogukonnas omandatud kopsupõletiku raviks nii ambulatoorses kui ka statsionaarses ravis. Selle põhjuseks on selle antibiootikumide rühma aktiivsuse puudumine peamise patogeeni - pneumokoki - vastu. Nosokomiaalse kopsupõletiku ravis määratakse aminoglükosiidid parenteraalselt. Aminoglükosiidide endotrahheaalne manustamine ettearvamatu farmakokineetika tõttu ei too kaasa kliinilise efektiivsuse suurenemist.
Aminoglükosiidide määramine šigelloosi ja salmonelloosi raviks (nii suukaudselt kui ka parenteraalselt) on ekslik, kuna need on kliiniliselt ebaefektiivsed intratsellulaarselt lokaliseeritud patogeenide suhtes.
Aminoglükosiide ei tohi kasutada tüsistusteta kuseteede infektsioonide raviks, välja arvatud juhul, kui patogeen on resistentne muude vähemtoksiliste antibiootikumide suhtes.
Samuti ei tohi aminoglükosiide kasutada paikselt nahainfektsioonide ravis, kuna mikroorganismides tekib kiire resistentsus.
Aminoglükosiidide kasutamist voolu äravooluks ja kõhuõõne niisutamiseks tuleks vältida nende tugeva mürgisuse tõttu.
Aminoglükosiidide annustamisreeglid. Täiskasvanud patsientidele on aminoglükosiidide määramiseks kaks režiimi: traditsiooniline kui neid manustatakse 2-3 korda päevas (näiteks streptomütsiin, kanamütsiin ja amikatsiin - 2 korda; gentamütsiin, tobramütsiin ja netilmitsiin - 2-3 korda) ja kogu päevaannuse ühekordne manustamine.
Kogu aminoglükosiidi ööpäevase annuse ühekordne manustamine võimaldab optimeerida ravi selle ravimirühmaga. Arvukad kliinilised uuringud on näidanud, et ravi efektiivsus ühe aminoglükosiidide režiimiga on sama, mis traditsioonilise ravi korral, ja nefrotoksilisus on vähem väljendunud. Lisaks vähenevad ühekordse päevase annuse manustamisega majanduslikud kulud. Seda aminoglükosiidide raviskeemi ei tohi siiski kasutada infektsioosse endokardiidi raviks.
Aminoglükosiidide annuse valikut mõjutavad sellised tegurid nagu patsiendi kehakaal, infektsiooni asukoht ja raskusaste ning neerufunktsioon.
Parenteraalseks manustamiseks tuleb kõigi aminoglükosiidide annused arvutada kehakaalu kilogrammi kohta. Arvestades, et aminoglükosiidid on rasvkoes halvasti jaotunud, tuleb patsientidel, kelle kehakaal ületab ideaalväärtust rohkem kui 25%, annust kohandada. Sel juhul tuleks tegeliku kehakaalu järgi arvutatud ööpäevast annust empiiriliselt vähendada 25%. Samal ajal suurendatakse alatoidetud patsientidel annust 25%.
Meningiidi, sepsise, kopsupõletiku ja muude raskete infektsioonide korral määratakse aminoglükosiidide maksimaalsed annused, kuseteede infektsioonide korral - minimaalne või keskmine. Maksimaalseid annuseid ei tohi anda eakatele.
Neerupuudulikkusega patsientidel tuleb aminoglükosiidide annust tingimata vähendada. See saavutatakse kas ühekordse annuse vähendamise või süstide vaheliste intervallide suurendamisega.
Terapeutiliste ravimite jälgimine. Kuna aminoglükosiidide farmakokineetika on ebastabiilne ja sõltub mitmest põhjusest, viiakse TDM läbi maksimaalse kliinilise efekti saavutamiseks, vähendades samal ajal AR-i tekke riski. Samal ajal määratakse aminoglükosiidide maksimaalne ja jääkkontsentratsioon vereseerumis. Maksimaalne kontsentratsioon (60 minutit pärast intramuskulaarset süstimist või 15-30 minutit pärast intravenoosse manustamise lõppu), millest sõltub ravi efektiivsus, peaks tavapärase annustamisrežiimi korral olema vähemalt 6-10 μg / ml gentamütsiini, tobramütsiini ja netilmitsiin , kanamütsiini ja amikatsiini puhul - vähemalt 20-30 mcg / ml. Jääkkontsentratsioonid (enne järgmist manustamist), mis näitavad aminoglükosiidide kumulatsiooni astet ja võimaldavad jälgida ravi ohutust, peaksid gentamütsiini, tobramütsiini ja netilmitsiini puhul olema alla 2 μg / ml, kanamütsiini ja amikatsiini puhul - alla 10 μg / ml. TDM on eriti vajalik raskete infektsioonidega patsientidel ja teiste aminoglükosiidide toksilise toime riskitegurite esinemisel. Päevase annuse väljakirjutamisel ühekordse süstina kontrollitakse tavaliselt aminoglükosiidide jääkkontsentratsiooni.
Vastunäidustused: Allergilised reaktsioonid aminoglükosiididele.
9. Levomütsetiinid
Levomütsetiinid on laia toimespektriga antibiootikumid. Levomütsetiinide rühma kuuluvad Levomütsetiin ja Synthomycin. Esimene looduslik antibiootikum levomütsetiin saadi 1947. aastal kiirgava seente Streptomyces venezualae kultuurist ja 1949. aastal pandi paika keemiline struktuur. NSV Liidus nimetati seda antibiootikumi "levomütsetiiniks", kuna see on vasakukäeline isomeer. Paremale pöörav isomeer ei ole bakterite vastu efektiivne. Selle rühma antibiootikum, mis saadi sünteetiliselt 1950. aastal, sai nimeks "Synthomycin". Süntomütsiini koostis sisaldas vasaku- ja paremakäeliste isomeeride segu, mistõttu on süntomütsiini toime klooramfenikooliga võrreldes 2 korda nõrgem. Süntomütsiini kasutatakse eranditult väliselt.
Toimemehhanism. Levomütsetiinidele on iseloomulik bakteriostaatiline toime ja need häirivad spetsiifiliselt valgusünteesi, kinnituvad ribosoomidele, mis põhjustab mikroobirakkude paljunemisfunktsiooni pärssimist. Sama omadus luuüdis põhjustab erütrotsüütide ja leukotsüütide moodustumise peatumist (võib põhjustada aneemiat ja leukopeeniat), samuti hematopoeesi pärssimist. Isomeeridel on kesknärvisüsteemile vastupidine toime: vasakukäeline isomeer surub kesknärvisüsteemi alla ja parempoolne isomeer ergastab seda mõõdukalt.
Tegevusring. Antibiootikumid-levomütsetiinid on aktiivsed paljude gramnegatiivsete ja grampositiivsete bakterite vastu; viirused: Chlamydia psittaci, Chlamydia trachomatis; Spirochaetales, Rickettsiae; bakteritüved, mis ei allu penitsilliini, streptomütsiini, sulfoonamiidide toimele. Neil on väike mõju happeresistentsetele bakteritele (tuberkuloosi patogeenid, mõned saprofüüdid, pidalitõbi), algloomadele, Clostridium'ile, Pseudomonas aeruginosale. Ravimiresistentsuse areng selle rühma antibiootikumide suhtes on suhteliselt aeglane. Levomütsetiinid ei ole võimelised tekitama ristresistentsust teiste kemoterapeutiliste ravimite suhtes.
Prenderdamine. Levomütsetiine kasutatakse trahhoomi, gonorröa, erinevat tüüpi kopsupõletiku, meningiidi, läkaköha, riketsioosi, klamüüdia, tulareemia, brutselloosi, salmonelloosi, düsenteeria, paratüüfuse, kõhutüüfuse jne raviks.
10. Glükopeptiidide rühm
Glükopeptiidid on looduslikud antibiootikumid vankomütsiin ja teikoplaniin. Vankomütsiini on kliinilises praktikas kasutatud alates 1958. aastast, teikoplaniini - alates 80. aastate keskpaigast. Viimasel ajal on huvi glükopeptiidide vastu suurenenud sageduse suurenemise tõttu haiglanakkused põhjustatud grampositiivsete bakterite poolt. Praegu on glükopeptiidid valitud ravimid põhjustatud infektsioonide korral MRSA, MRSE, samuti enterokokkide suhtes resistentsed ampitsilliin ja aminoglükosiidid.
Toimemehhanism. Glükopeptiidid häirivad bakteriraku seina sünteesi. Neil on aga bakteritsiidne toime enterokokkide, osade streptokokkide ja KNS toimivad bakteriostaatiliselt.
Tegevuse spekter. Glükopeptiidid on aktiivsed grampositiivsete aeroobsete ja anaeroobsete mikroorganismide vastu: stafülokokid (sh. MRSA, MRSE), streptokokk, pneumokokk (sh ARP), enterokokk, peptostreptokokk, listeria, corynebacterium, klostridium (kaasa arvatud C.difficile). Gramnegatiivsed mikroorganismid on glükopeptiidide suhtes resistentsed.
Antimikroobse toime spektri järgi on vankomütsiin ja teikoplaniin sarnased, kuid mõningaid erinevusi on loomuliku aktiivsuse ja omandatud resistentsuse tasemes. Teikoplaniin in vitro poole aktiivsem S. aureus(kaasa arvatud MRSA), streptokokid (sh S.pneumoniae) ja enterokokid. Vankomütsiin sisse vitro poole aktiivsem KNS.
Viimastel aastatel on tuvastatud mitu riiki S. aureus vähenenud tundlikkusega vankomütsiini või vankomütsiini ja teikoplaniini suhtes.
Enterokokid arendavad vankomütsiini suhtes resistentsust kiiremini välja: praegused intensiivraviosakonna resistentsuse määrad USA-s on E.faecium vankomütsiinile on umbes 10% või rohkem. Siiski on kliiniliselt oluline, et mõned VRE jäävad teikoplaniini suhtes tundlikuks.
Farmakokineetika. Suukaudsel manustamisel glükopeptiidid praktiliselt ei imendu. Biosaadavus teikoplaniini i / m manustamisega on umbes 90%.
Glükopeptiide ei metaboliseeru, need erituvad muutumatul kujul neerude kaudu, seetõttu on neerupuudulikkuse korral vaja annust kohandada. Ravimeid hemodialüüsiga ei eemaldata.
Pool elu normaalse neerufunktsiooniga vankomütsiinil on 6-8 tundi, teikoplaniinil - 40 tundi kuni 70. Teikoplaniini pikk poolväärtusaeg võimaldab välja kirjutada üks kord päevas.
Näidustused:
1. Põhjustatud infektsioonid MRSA, MRSE.
2. Stafülokoki infektsioonid β-laktaamide allergia korral.
3. Põhjustatud rasked infektsioonid Enterokokk spp., C.jeikeium, B.cereus, F.meningosepticum.
4. Nakkuslik endokardiit põhjustatud viridestseeruvatest streptokokkidest ja S. bovis, allergiaga β-laktaamide suhtes.
5. Nakkuslik endokardiit põhjustatud E.faecalis(koos gentamütsiin).
6. Meningiit põhjustatud S.pneumoniae, vastupidav penitsilliinid.
Stafülokoki etioloogia kahtlusega eluohtlike infektsioonide empiiriline ravi:
Trikuspidaalklapi või proteesklapi infektsioosne endokardiit (kombinatsioonis gentamütsiin);
Sarnased dokumendid
Antibiootikumid tsükliliste polüpeptiidide rühmast. Penitsilliinide, tsefalosporiinide, makroliidide, tetratsükliinide, aminoglükosiidide ja polümüksiinide rühma preparaadid. Antibiootikumide kombineeritud kasutamise põhimõtted, nende ravist tulenevad tüsistused.
abstraktne, lisatud 08.04.2012
Penitsilliini avastamise ajalugu. Antibiootikumide klassifikatsioon, nende farmakoloogilised, kemoterapeutilised omadused. Tehnoloogiline protsess antibiootikumide saamiseks. Bakterite resistentsus antibiootikumide suhtes. Kloramfenikooli, makroliidide, tetratsükliinide toimemehhanism.
abstraktne, lisatud 24.04.2013
Antibiootikumide klassifikatsioon rakuseina toimemehhanismi järgi. Tsütoplasmaatilise membraani funktsioonide inhibiitorite uurimine. Tetratsükliinide antimikroobse spektri arvestamine. Mikroorganismide resistentsuse kujunemise suundumused praegu maailmas.
abstraktne, lisatud 08.02.2012
Antibiootikumide avastamise ajalugu. Antibiootikumide toimemehhanism. Antibiootikumide selektiivne toime. Antibiootikumiresistentsus. Tänapäeval tuntud peamised antibiootikumide rühmad. Peamised kõrvaltoimed antibiootikumidele.
aruanne, lisatud 03.11.2009
Uimastite uurimine üldnimetuse "antibiootikumid" all. Antibakteriaalsed kemoterapeutilised ained. Antibiootikumide avastamise ajalugu, nende toimemehhanism ja klassifikatsioon. Antibiootikumide kasutamise tunnused ja nende kõrvaltoimed.
kursusetöö, lisatud 16.10.2014
Ratsionaalse antibiootikumiravi põhimõtted. Antibiootikumide rühmad: penitsilliinid, tetratsükliinid, tsefalosporiinid, makroliidid ja fluorokinoloonid. Poolsünteetiliste penitsilliinide kaudne toime. Tsefalosporiinide antimikroobne toimespekter, peamised tüsistused.
esitlus, lisatud 29.03.2015
Antibakteriaalsete ainete kasutamise tunnused bakterite põhjustatud nakkushaiguste raviks ja ennetamiseks. Antibiootikumide klassifikatsioon antimikroobse toime spektri järgi. Antibiootikumide kasutamise kahjulike mõjude kirjeldused.
esitlus, lisatud 24.02.2013
Antibiootikumide pioneerid. Antibiootikumide levik looduses. Antibiootikumide roll looduslikes mikrobiotsenoosides. Bakteriostaatiliste antibiootikumide toime. Bakterite resistentsus antibiootikumide suhtes. Antibiootikumide füüsikalised omadused, nende klassifikatsioon.
esitlus, lisatud 18.03.2012
Antibiootikumide klassifikatsioon bioloogilise toime spektri järgi. Beeta-laktaamantibiootikumide omadused. HIV-nakkuse bakteriaalsed tüsistused, nende ravi. Looduslikud ühendid, millel on kõrge antibakteriaalne toime ja lai toimespekter.
abstraktne, lisatud 20.01.2010
Bioloogilise päritoluga keemilised ühendid, millel on mikroorganisme kahjustav või hävitav toime väga väikeses kontsentratsioonis vastavalt antibioosi põhimõttele. Antibiootikumide allikad ja nende farmakoloogilise toime suund.
Kliinilised - farmakoloogilised omadused
beeta-laktaamantibiootikumid
Penitsilliinide, tsefalosporiinide, karbapeneemide ja monobaktaamide struktuuris on β-laktaamtsükkel, mis määrab nende tugeva bakteritsiidse toime ja võimaluse ristallergia tekkeks. Penitsilliinid ja tsefalosporiinid võivad inaktiveerida mikroorganismid (sh soolefloora), mis toodavad ensüümi β-laktamaasi (penitsillinaas), mis hävitab β-laktaami ringi. Tänu kõrgele kliinilisele efektiivsusele ja madalale toksilisusele on β-laktaamantibiootikumid enamiku infektsioonide ravis juhtival kohal.
Penitsilliinid
Klassifikatsioon.
1. Looduslikud (looduslikud) penitsilliinid- bensüülpenitsilliinid, fenoksümetüülpenitsilliinid ja pika toimeajaga penitsilliinid (durant penitsilliinid).
2. Poolsünteetilised penitsilliinid:
● isoksasolpenitsilliinid - antistafülokoki penitsilliinid (oksatsilliin, kloksatsilliin, flukloksatsilliin);
● amidinopenitsilliinid (amdinotsilliin, pivamdinotsilliin, bakamdinotsilliin, atsidotsilliin);
● aminopenitsilliinid - laiendatud toimespektriga penitsilliinid (ampitsilliin, amoksitsilliin, talampitsilliin, bakampitsilliin, pivampitsilliin);
● antipseudomonaalsed antibiootikumid:
- karboksüpenitsilliinid (karbenitsilliin, karfetsilliin, karindatsilliin, tikartsilliin),
- ureidopenitsilliinid (aslotsilliin, metsotsilliin, piperatsilliin);
● inhibiitoritega kaitstud penitsilliinid (amoksitsilliin + klavulaanhape, ampitsilliin + sulbaktaam, tikartsilliin + klavulaanhape, piperatsilliin + tasobaktaam).
Bensüülpenitsilliinid madal toksilisus ja mitte kallis, tekitavad kiiresti kõrge kontsentratsiooni paljudes elundites ja kudedes, sealhulgas rakkude sees (seetõttu on need hädaabi vahendid); halvemini tungivad luu- ja närvikoesse, halvasti läbi BBB. Kuid meningiidi ja aju hüpoksiliste seisundite korral võivad nad tungida BBB-sse ajuveresoonte põletikulise kapillaaride vasodilatatsiooni tõttu ja seetõttu kasutatakse neid meningoentsefaliidi raviks.
Bensüülpenitsilliini naatriumsoola manustatakse intramuskulaarselt, intravenoosselt, endolumbaalselt (aju membraanide all - intratekaalne) ja kehaõõnes. Bensüülpenitsilliini kaaliumi ja novokaiini soola manustatakse ainult intramuskulaarselt. Kaaliumisoola ei tohi manustada intravenoosselt, kuna ravimist vabanevad kaaliumiioonid võivad põhjustada südametegevuse depressiooni ja krampe. Ravimi novokaiini sool lahustub vees halvasti, moodustab veega suspensioone ja selle sisenemine anumasse on vastuvõetamatu.
Bensüülpenitsilliinide määramise sagedus - 6 korda päevas (pärast 1 elukuud) ja ravimi novokaiinisoola (bensüülpenitsilliini prokaiin) - 2 korda päevas.
Fenoksümetüülpenitsilliin (FOMP) see on happekindel ja seda kasutatakse suukaudselt, kuid see ei tekita veres kõrgeid kontsentratsioone, seetõttu ei kasutata seda raskete infektsioonide raviks. Tavaliselt ei kasutata FOMP-i monoteraapiana, vaid kombineerituna teiste antibiootikumidega. Näiteks hommikul ja õhtul manustatakse intramuskulaarselt bensüülpenitsilliini kaaliumsoola ja pärastlõunal (2-3 korda) määratakse FOMP per os.
Pikaajalised penitsilliinipreparaadid kasutatakse profülaktilistel eesmärkidel. Bitsilliin - 1 (bensatiinbensüülpenitsilliin või bensatiinipenitsilliin G) lahustub vees halvasti, mistõttu kasutatakse seda ainult intramuskulaarseks süstimiseks 1–2 korda nädalas. Bitsilliin - 3 on bensüülpenitsilliini kaaliumi- või novokaiinisoolade kombinatsioon bitsilliiniga - 1 võrdsetes osades, igaüks 100 tuhat ühikut. Ravimit manustatakse intramuskulaarselt 1-2 korda nädalas. Bitsilliin - 5 on ka kombinatsioon bensüülpenitsilliini novokaiini soolast ja bitsilliinist - 1 vahekorras 1 kuni 4. Selle intramuskulaarne süstimine tehakse 1 kord 4 nädala jooksul.
Bitsilliini - 1 aeglase imendumise tõttu algab selle toime alles 1-2 päeva pärast manustamist. Bitsilliinidel - 3 ja - 5 on neis sisalduva bensüülpenitsilliini tõttu antimikroobne toime juba esimestel tundidel.
Looduslike penitsilliinide kõige sagedasem kõrvaltoime on allergilised reaktsioonid (võimalik anafülaktiline šokk). Seetõttu on ravimite väljakirjutamisel vaja hoolikalt koguda allergia ajalugu ja jälgida patsienti 30 minutit. pärast ravimi esimest süstimist. Mõnel juhul tehakse nahatestid.
Ravimid avaldavad antagonismi sulfoonamiididega ja sünergismi aminoglükosiididega grampositiivsete kokkide vastu (välja arvatud pneumokokid!), kuid ei ühildu nendega ühes süstlas ega ühes infusioonisüsteemis.
Isoksasolpenitsilliinid(antistafülokoki penitsilliinid) on penitsillinaasi toime suhtes resistentsed, st aktiivsed penitsilliiniresistentsed stafülokoki tüved- Staphylococcus aureus (PRSA), Pealegi metitsilliiniresistentsed stafülokoki tüved (MRSA).PRSA – probleemis mängivad suurt rolli stafülokokid haiglane(intrahaigla, haigla) infektsioonid. Teiste mikroorganismide puhul on nende toimespekter sama, mis looduslikel penitsilliinidel, kuid antimikroobne toime on palju väiksem. Preparaate manustatakse nii parenteraalselt kui ka suukaudselt 1-1,5 tundi enne sööki, kuna need ei ole vesinikkloriidhappe suhtes eriti vastupidavad.
Amidinopenitsilliinid aktiivne gramnegatiivsete enterobakterite vastu. Nende toimespektri suurendamiseks kombineeritakse neid antibiootikume isoksasolpenitsilliinide ja looduslike penitsilliinidega.
Aminopenitsilliinid- laia toimespektriga antibiootikumid, kuid PRSA on nende suhtes resistentne, mistõttu need ravimid ei lahenda haiglanakkuse probleemi. Seetõttu on loodud kombineeritud preparaadid: ampioks (ampitsilliin + oksatsilliin), klonak - R (ampitsilliin + kloksatsilliin), sultamitsilliin (ampitsilliin + sulbaktaam, mis on β-laktamaasi inhibiitor), klonak - X (amoksitsilliin + kloksatsilliin), augmentiin ja selle analoog amoksiklav (amoksitsilliin + klavulaanhape).
Antipseudomonaalsed penitsilliinid on ette nähtud ainult teiste antipseudomonaalsete ravimite puudumisel ja ainult Pseudomonas aeruginosa kinnitatud tundlikkuse korral nende suhtes, kuna need on toksilised ja arenevad kiiresti teisejärguline(indutseeritud antibiootikumi enda poolt) vastupanu patogeen. Ravimid ei mõjuta stafülokokke. Seetõttu kombineeritakse neid vajadusel isoksasolpenitsilliinidega. On kombineeritud ravimeid: timentiin (tikartsilliin + klavulaanhape) ja tasotsiin (piperatsilliin + tasobaktaam β-laktamaasi inhibiitorina).
● Inhibiitoriga kaitstud penitsilliinid- kombineeritud preparaadid, mis sisaldavad β-laktamaasi inhibiitoreid (klavulaanhape, sulbaktaam, tasobaktaam). Kõige võimsam neist on tasotsiin. Need ravimid jaotuvad kehas hästi, luues kõrge kontsentratsiooni kudedes ja vedelikes (sh kopsudes, pleura- ja kõhukelmeõõntes, keskkõrvas, põskkoobastes), kuid tungivad halvasti BBB-sse. Klavulaanhappest on võimalik äge maksakahjustus: transaminaaside aktiivsuse tõus, palavik, iiveldus, oksendamine.
Looduslikud penitsilliinid, isoksasolpenitsilliinid, amidinopenitsilliinid, aminopenitsilliinid on vähetoksilised, neil on lai valik ravitoimeid. Nende ravimisel on ohtlikud ainult nii vahetu kui ka hilinenud tüüpi allergilised reaktsioonid.
Karboksüpenitsilliinid ja ureidopenitsilliinid on väikese terapeutilise toimega ravimid, st ravimid, millel on range annustamisskeem. Nende kasutamisega võivad kaasneda allergilised reaktsioonid, neuro- ja hematotoksilisuse sümptomid, nefriit, düsbioos, hüpokaleemia.
Kõik penitsilliinid ei sobi kokku paljude ainetega, seetõttu tuleks nende manustamine teha eraldi süstlaga.
Tsefalosporiinid
Neid ravimeid kasutatakse laialdaselt kliinilises praktikas, kuna neil on tugev bakteritsiidne toime, lai terapeutiline ulatus, erineva astmega resistentsus stafülokoki β-laktamaaside suhtes ja madal toksilisus.
Laia toimespektriga antibiootikumid on tänapäeval kõige populaarsemad ravimid. Nad väärivad sellist populaarsust tänu oma mitmekülgsusele ja võimele toime tulla korraga mitme ärritajaga, mis avaldavad negatiivset mõju inimeste tervisele.
Arstid ei soovita selliseid vahendeid kasutada ilma esialgsete kliiniliste uuringuteta ja ilma arstide soovitusteta. Antibiootikumide ebanormaalne kasutamine võib olukorda veelgi teravdada ja põhjustada uusi haigusi, samuti avaldada negatiivset mõju inimese immuunsusele.
Uue põlvkonna antibiootikumid
Antibiootikumide kasutamise risk tänu kaasaegsele meditsiini arengule on praktiliselt viidud nullini. Uutel antibiootikumidel on täiustatud valem ja toimepõhimõte, mille tõttu nende aktiivsed komponendid mõjutavad ainult patogeenset ainet rakutasandil, häirimata inimkeha kasulikku mikrofloorat. Ja kui varem kasutati selliseid aineid võitluses piiratud arvu patogeensete ainete vastu, siis täna on need kohe tõhusad terve rühma patogeenide vastu.
Antibiootikumid jagunevad järgmistesse rühmadesse:
- tetratsükliinrühm - tetratsükliin;
- aminoglükosiidide rühm - streptomütsiin;
- amfenikooli antibiootikumid - kloramfenikool;
- penitsilliini seeria ravimid - Amoksitsilliin, Ampitsilliin, Bilmitsiin või Tikartsükliin;
- karbapeneemide rühma antibiootikumid - imipeneem, meropeneem või ertapeneem.
Antibiootikumi tüübi määrab arst pärast haiguse põhjalikku uurimist ja kõigi selle põhjuste uurimist. Ravi arsti poolt määratud ravimiga on efektiivne ja ilma komplikatsioonideta.
Tähtis: isegi kui selle või teise antibiootikumi kasutamine aitas teid varem, ei tähenda see, et kui teil tekivad sarnased või täiesti identsed sümptomid, peaksite võtma sama ravimit.
Parimad uue põlvkonna laia toimespektriga antibiootikumid
Tetratsükliin
Sellel on lai valik rakendusi;
Mille vastu tetratsükliin aitab?
bronhiidi, tonsilliidi, farüngiidi, prostatiidi, ekseemi ja erinevate seedetrakti ja pehmete kudede infektsioonidega.

Kõige tõhusam antibiootikum krooniliste ja ägedate haiguste korral;
Päritoluriik - Saksamaa (Bayer);
Ravimil on väga lai kasutusala ja Vene Föderatsiooni tervishoiuministeerium lisab selle oluliste ravimite loetellu;
Praktiliselt puuduvad kõrvaltoimed.
Amoksitsilliin

Kõige kahjutu ja mitmekülgsem ravim;
Seda kasutatakse nii iseloomuliku temperatuuri tõusuga haiguste kui ka muude haiguste korral;
Kõige tõhusam:
- hingamisteede ja ENT organite infektsioonid (sh sinusiit, bronhiit, tonsilliit, keskkõrvapõletik);
- seedetrakti infektsioonid;
- naha ja pehmete kudede infektsioonid;
- urogenitaalsüsteemi infektsioonid;
- Lyme'i tõbi;
- düsenteeria;
- meningiit;
- salmonelloos;
- sepsis.

Tootmisriik - Suurbritannia;
Mis aitab?
bronhiit, tonsilliit, sinusiit, samuti mitmesugused hingamisteede infektsioonid.
Amoksiklav

Efektiivne ravim, millel on väga lai kasutusala, praktiliselt kahjutu;
Peamised eelised:
- minimaalsed vastunäidustused ja kõrvaltoimed;
- meeldiv maitse;
- kiirus;
- ei sisalda värvaineid.

Kiire toimega ravim, millel on väga lai kasutusala;
See on kõige tõhusam võitluses hingamisteede infektsioonidega, nagu tonsilliit, sinusiit, bronhiit, kopsupõletik. Seda kasutatakse ka võitluses naha ja pehmete kudede nakkushaiguste, urogenitaal- ja soolehaiguste vastu.

Väga aktiivne gramnegatiivsete mikroorganismide vastu;
Tootmisriik - Venemaa;
See on kõige tõhusam võitluses grampositiivsete ja gramnegatiivsete bakterite, mükoplasmade, legionella, salmonella, aga ka sugulisel teel levivate patogeenide vastu.
Avikaz

Kiire toimega ravim, millel pole praktiliselt mingeid kõrvaltoimeid;
Tootmisriik - USA;
Kõige tõhusam kuseteede ja neerude haiguste ravis.
Seade on jaotatud ampullides (süstides), mis on üks kiiremini toimivaid antibiootikume;
Kõige tõhusam ravim järgmiste haiguste raviks:
- püelonefriit ja inf. kuseteede;
- nakatada. väikese vaagna haigused, endometriit, operatsioonijärgne inf-yah ja septilised abordid;
- naha ja pehmete kudede bakteriaalsed kahjustused, sealhulgas diabeetiline jalg;
- kopsupõletik;
- septitseemia;
- kõhuõõne infektsioonid.
Doriprex

Sünteetiline antimikroobne ravim, millel on bakteritsiidne toime;
Päritoluriik - Jaapan;
See ravim on kõige tõhusam järgmiste haiguste ravis:
- haiglane kopsupõletik;
- rasked intraabdominaalsed infektsioonid;
- keeruline inf. kuseteede süsteem;
- püelonefriit, keerulise kuluga ja baktereemiaga.
Antibiootikumide klassifikatsioon toimespektri ja kasutuseesmärgi järgi
Antibiootikumide kaasaegne klassifikatsioon rühmade kaupa: tabel
| Põhirühm | Alamklassid |
| Beeta-laktaamid | |
| 1. Penitsilliinid | loomulik; Antistafülokokk; Antipseudomonaalne; Laiendatud toimespektriga; inhibiitoritega kaitstud; Kombineeritud. |
| 2. Tsefalosporiinid | 4 põlvkonda; MRSA-vastased tsefeemid. |
| 3. Karbapeneemid | - |
| 4. Monobaktaamid | - |
| Aminoglükosiidid | Kolm põlvkonda. |
| makroliidid | neljateistkümneliikmeline; 15-liikmeline (asoolid); Kuusteist liiget. |
| Sulfoonamiidid | Lühike tegevus; Keskmine toime kestus; Pikanäitlemine; Eriti pikk; Kohalik. |
| Kinoloonid | Fluorimata (1. põlvkond); Teiseks; Hingamisteede (3.); Neljandaks. |
| Tuberkuloosivastane | Põhirida; reservrühm. |
| Tetratsükliinid | loomulik; Poolsünteetiline. |
Järgnevalt on toodud selle seeria antibiootikumide tüübid ja nende klassifikatsioon tabelis.
| Grupp | Vastavalt toimeainele eraldatakse preparaadid: | Pealkirjad |
| Loomulik | Bensüülpenitsilliin | Bensüülpenitsilliini Na ja K soolad. |
| Fenoksümetüülpenitsilliin | Metüülpenitsilliin | |
| Pikaajalise tegevusega. | ||
| Bensüülpenitsilliin prokaiin | Bensüülpenitsilliini novokaiini sool. | |
| Bensüülpenitsilliin / bensüülpenitsilliin prokaiin / Bensatiini bensüülpenitsilliin | Bensitsilliin-3. Bitsilliin-3 | |
| Bensüülpenitsilliin prokaiin/bensatiin bensüülpenitsilliin | Bensitsilliin-5. Bitsilliin-5 | |
| Antistafülokokk | Oksatsilliin | Oksatsilliini AKOS, oksatsilliini naatriumisool. |
| penitsillinaasi suhtes resistentne | kloksaptsilliin; Alukloksatsilliin. |
|
| Spread Spekter | Ampitsilliin | Ampitsilliin |
| Amoksitsilliin | Flemoxin Solutab, Ospamox, Amoksitsilliin. | |
| Antipseudomonaalse aktiivsusega | Karbenitsilliin | Karbenitsilliini, karfetsilliini, karindatsilliini dinaatriumsool. |
| Uriedopenitsilliinid | ||
| Piperatsilliin | Pitsilliin, Pipracil | |
| aslotsilliin | Naatriumaslotsilliin, Securopen, metslotsilliin.. | |
| inhibiitoritega kaitstud | Amoksitsilliin/klavulanaat | Kaasamoksiklav, Augmentin, Amoksiklav, Ranklav, Enhancin, Panklav. |
| Amoksitsilliin sulbaktaam | Trifamox IBL. | |
| Amlitsilliin/sulbaktaam | Sulatsilliin, unasiin, ampisid. | |
| Piperatsilliin/tasobaktaam | Tasotsiin | |
| Tikartsilliin/klavulanaat | Timentin | |
| Penitsilliinide kombinatsioon | Ampitsilliin/oksatsilliin | Ampiox. |
Antibiootikumid toime kestuse järgi:
Antibiootikumide rühmad ja põlvkonna peamiste ravimite nimetused.
| Põlvkonnad | Ettevalmistus: | Nimi |
| 1 | Tsefasoliin | Kefsool. |
| tsefaleksiin* | Tsefaleksiin-AKOS. | |
| tsefadroksiil* | Durocef. | |
| 2 | Tsefuroksiim | Zinacef, Cefurus. |
| Tsefoksitiin | Mefoksin. | |
| Tsefotetaan | Tsefotetaan. | |
| tsefakloor* | Zeklor, Vercef. | |
| Tsefuroksiim-aksetiil* | Zinnat. | |
| 3 | Tsefotaksiim | Tsefotaksiim. |
| Tseftriaksoon | Rofecin. | |
| Tsefoperasoon | Medocef. | |
| Tseftasidiim | Fortum, tseftasidiim. | |
| Tsefoperasoon/sulbak-tama | Sulperazon, Sulzoncef, Bakperazon. | |
| Cefditorena* | Spectracef. | |
| Cefixime* | Suprax, Sorcef. | |
| tsefpodoksiim* | Proksetil. | |
| tseftibuteen* | Cedex. | |
| 4 | tsefepima | Maxim. |
| Tsefpiroom | Caten. | |
| 5 | tseftobiprool | Zefter. |
| Tseftaroliin | Zinforo. |
Antibiootikumid- rühm looduslikku päritolu ühendeid või nende poolsünteetilisi ja sünteetilisi analooge, millel on antimikroobne või kasvajavastane toime.
Praeguseks on selliseid aineid teada mitusada, kuid meditsiinis on neist rakendust leidnud vaid vähesed.
Antibiootikumide peamised klassifikatsioonid
Antibiootikumide klassifikatsiooni alusel Samuti on mitmeid erinevaid põhimõtteid.
Vastavalt nende saamise meetodile jagunevad need:
- looduslikul;
- sünteetiline;
- poolsünteetilised (algfaasis saadakse need looduslikult, seejärel süntees viiakse läbi kunstlikult).
Antibiootikumide tootjad:
- valdavalt aktinomütseedid ja hallitusseened;
- bakterid (polümüksiinid);
- kõrgemad taimed (fütontsiidid);
- loomade ja kalade koed (erütriin, ekteritsid).
Tegevuse suund:
- antibakteriaalne;
- seenevastane;
- kasvajavastane.
Vastavalt toimespektrile - mikroorganismide tüüpide arv, millele antibiootikumid mõjutavad:
- laia toimespektriga ravimid (3. põlvkonna tsefalosporiinid, makroliidid);
- kitsa toimespektriga ravimid (tsükloseriin, linkomütsiin, bensüülpenitsilliin, klindamütsiin). Mõnel juhul võivad need olla eelistatavad, kuna need ei pärsi normaalset mikrofloorat.
Klassifikatsioon keemilise struktuuri järgi
Keemilise struktuuri järgi Antibiootikumid jagunevad järgmisteks osadeks:
- beeta-laktaamantibiootikumide jaoks;
- aminoglükosiidid;
- tetratsükliinid;
- makroliidid;
- linkosamiidid;
- glükopeptiidid;
- polüpeptiidid;
- polüeenid;
- antratsükliini antibiootikumid.
molekuli selgroog beeta-laktaamantibiootikumid moodustab beeta-laktaamtsükli. Need sisaldavad:
- penitsilliinid ~ rühm looduslikke ja poolsünteetilisi antibiootikume, mille molekul sisaldab 6-aminopenitsillaanhapet, mis koosneb 2 ringist - tiasolidoon ja beetalaktaam. Nende hulgas on:
Biosünteetiline (penitsilliin G - bensüülpenitsilliin);
- aminopenitsilliinid (amoksitsilliin, ampitsilliin, bekampitsilliin);
Poolsünteetilised "stafülokokivastased" penitsilliinid (oksatsilliin, metitsilliin, kloksatsilliin, dikloksatsilliin, flukloksatsilliin), mille peamine eelis on resistentsus mikroobsete beeta-laktamaaside, peamiselt stafülokokkide suhtes;
- tsefalosporiinid on looduslikud ja poolsünteetilised antibiootikumid, mis on saadud 7-aminotsefalospoorhappest ja sisaldavad tsefeemi (ka beetalaktaami) ringi,
st oma struktuurilt on nad lähedased penitsilliinidele. Need jagunevad iefalosporiinideks:
1. põlvkond - tseporiin, tsefalotiin, tsefaleksiin;
- 2. põlvkond - tsefasoliin (kefsool), tsefamesiin, tsefaman-dol (mandool);
- 3. põlvkond - tsefuroksiim (ketocef), tsefotaksiim (klaforaan), tsefuroksiimaksetiil (zinnat), tseftriaksoon (longa-cef), tseftasidiim (fortum);
- 4. põlvkond - tsefepiim, tsefpir (tsefroom, keiten) jne;
- monobaktaamid - astreonaam (asaktaam, mittebaktaam);
- karbopeneemid - meropeneem (meroneem) ja imipineem, mida kasutatakse ainult koos spetsiifilise neerudehüdropeptidaasi inhibiitoriga tsilastatiini - imipineemi / tsilastatiini (tienaam).
Aminoglükosiidid sisaldavad aminosuhkruid, mis on glükosiidsidemega seotud ülejäänud molekuliga (aglükooni fragmendiga). Need sisaldavad:
- sünteetilised aminoglükosiidid - streptomütsiin, gentamütsiin (garamütsiin), kanamütsiin, neomütsiin, monomütsiin, sisomütsiin, tobramütsiin (tobra);
- poolsünteetilised aminoglükosiidid - spektinomütsiin, amikatsiin (amikiin), netilmitsiin (netilliin).
molekuli selgroog tetratsükliinid on polüfunktsionaalne hüdronaftatseeni ühend üldnimetusega tetratsükliin. Nende hulgas on:
- looduslikud tetratsükliinid - tetratsükliin, oksütetratsükliin (klinimütsiin);
- poolsünteetilised tetratsükliinid - metatsükliin, kloortetriin, doksütsükliin (vibramütsiin), minotsükliin, rolitetratsükliin. Grupi ravimid makroliid sisaldavad oma molekulis makrotsüklilist laktoonitsüklit, mis on seotud ühe või mitme süsivesikujäägiga. Need sisaldavad:
- erütromütsiin;
- oleandomütsiin;
- roksitromütsiin (ruliid);
- asitromütsiin (sumamed);
- klaritromütsiin (klatsiid);
- spiramütsiin;
- diritromütsiin.
To linkosamiid hõlmavad linkomütsiini ja klindamütsiini. Nende antibiootikumide farmakoloogilised ja bioloogilised omadused on väga lähedased makroliididele ja kuigi need on keemiliselt täiesti erinevad ravimid, klassifitseerivad mõned meditsiiniallikad ja farmaatsiaettevõtted, mis toodavad keemiaravi ravimeid, näiteks delatsiin C, linkosamiinid makroliidide hulka.
Grupi ravimid glükopeptiidid sisaldavad oma molekulis asendatud peptiidühendeid. Need sisaldavad:
- vankomütsiin (vankatsiin, diatratsiin);
- teikoplaniin (targotsiid);
- daptomütsiin.
Grupi ravimid polüpeptiidid nende molekul sisaldab polüpeptiidühendite jääke, sealhulgas:
- gramitsidiin;
- polümüksiinid M ja B;
- batsitratsiin;
- kolistiini.
Grupi ravimid niisutamine sisaldavad oma molekulis mitut konjugeeritud kaksiksidet. Need sisaldavad:
- amfoteritsiin B;
- nüstatiin;
- levoriin;
- natamütsiin.
antratsükliini antibiootikumidele Vähivastased antibiootikumid hõlmavad:
- doksorubitsiin;
- karminomütsiin;
- rubomütsiin;
- aklarubitsiin.
Praktikas kasutatakse laialdaselt mitmeid teisi antibiootikume, mis ei kuulu ühtegi loetletud rühma: fosfomütsiin, fusidiinhape (fusidiin), rifampitsiin.
Antibiootikumide, aga ka teiste kemoterapeutiliste ainete antimikroobse toime aluseks on mikroobirakkude metabolismi rikkumine.
Antibiootikumide antimikroobse toime mehhanism
Vastavalt antimikroobse toime mehhanismile Antibiootikumid võib jagada järgmistesse rühmadesse:
- rakuseina sünteesi inhibiitorid (mureiin);
- tsütoplasma membraani kahjustamine;
- valkude sünteesi inhibeerimine;
- nukleiinhapete sünteesi inhibiitorid.
Rakuseina sünteesi inhibiitoritele seotud:
- beetalaktaamantibiootikumid - penitsilliinid, tsefalosporiinid, monobaktaamid ja karbopeneemid;
- glükopeptiidid - vankomütsiin, klindamütsiin.
Bakteriraku seina sünteesi blokeerimise mehhanism vankomütsiini poolt. erineb penitsilliinide ja tsefalosporiinide omast ega konkureeri seega nendega seondumiskohtade pärast. Kuna loomarakkude seintes ei ole peptidoglükaani, on need antibiootikumid makroorganismile väga madala toksilisusega ja neid saab kasutada suurtes annustes (megateraapia).
Antibiootikumidele, mis kahjustavad tsütoplasma membraani(fosfolipiidide või valgu komponentide blokeerimine, rakumembraanide läbilaskvuse rikkumine, membraanipotentsiaali muutused jne), hõlmavad:
- polüeenantibiootikumid - neil on väljendunud seenevastane toime, muutes rakumembraani läbilaskvust, interakteerudes (blokeerides) steroidkomponentidega, mis moodustavad selle seentes, mitte bakterites;
- polüpeptiidantibiootikumid.
Suurim antibiootikumide rühm on valkude sünteesi pärssimine. Valgu sünteesi rikkumine võib toimuda kõigil tasanditel, alustades DNA-st teabe lugemise protsessist ja lõpetades interaktsiooniga ribosoomidega - transport-t-RNA seondumise blokeerimine ribosoomide struuma subühikutega (aminoglükosiidid), 508 ribosoomide (makroliidide) subühikutega. ) või informatsiooniga i-RNA (ribosoomide 308 alaühikul - tetratsükliinid). Sellesse rühma kuuluvad:
- aminoglükosiidid (näiteks aminoglükosiid gentamütsiin, inhibeerides valkude sünteesi bakterirakus, võib häirida viiruste valgukatte sünteesi ja seetõttu võib olla viirusevastane toime);
- makroliidid;
- tetratsükliinid;
- klooramfenikool (levomütsetiin), mis häirib valkude sünteesi mikroobiraku poolt aminohapete ribosoomidesse ülekandmise staadiumis.
Nukleiinhapete sünteesi inhibiitorid Neil ei ole mitte ainult antimikroobne, vaid ka tsütostaatiline toime ja seetõttu kasutatakse neid kasvajavastaste ainetena. Üks sellesse rühma kuuluvatest antibiootikumidest, rifampitsiin, inhibeerib DNA-st sõltuvat RNA polümeraasi ja blokeerib seeläbi valkude sünteesi transkriptsiooni tasemel.
Antibiootikumid on bioloogilist päritolu keemilised ühendid, millel on selektiivne mikroorganisme kahjustav või hävitav toime.
1929. aastal kirjeldas A. Fleming esmakordselt stafülokokkide lüüsi Petri tassidel, mis olid saastunud perekonna Penicillium seentega ning 1940. aastal saadi esimesed penitsilliinid nende mikroorganismide kultuurist. Ametlike hinnangute kohaselt on inimkonda viimase neljakümne aasta jooksul tutvustatud mitu tuhat tonni penitsilliini. Just nende laialdase kasutamisega kaasnevad antibiootikumiravi laastavad tagajärjed, piisaval protsendil juhtudest, kui seda tehakse mitte vastavalt näidustustele. Praeguseks on enamiku arenenud riikide elanikest 1-5% penitsilliinide suhtes ülitundlikud. Alates 1950. aastatest on kliinikutest saanud beetalaktamaasi tootvate stafülokokkide paljunemise ja selektsiooni kohad, mis praegu domineerivad ja moodustavad ligikaudu 80% kõigist stafülokoki infektsioonidest. Mikroorganismide resistentsuse pidev areng on uute ja uute antibiootikumide loomise peamine stimuleeriv põhjus, mis raskendab nende klassifitseerimist.
Antibiootikumide klassifikatsioon
1. Antibiootikumid, mille struktuuris on beeta-laktaamtsükkel
a) penitsilliinid (bensüülpenitsilliin, fenoksümetüülpenitsilliin, metitsilliin,
oksatsilliin, ampitsilliin, karboksüülitsilliin)
b) tsefalosporiinid (tsefasoliin, tsefaleksiin)
c) karbapeneemid (imipeneem)
d) Monobaktaamid (astreonaam)
2. Makroliidid, mis sisaldavad makrotsüklilist laktoonitsüklit (erythromi
tsin, oleandomütsiin, spiramütsiin, roksitromütsiin, asitromütsiin)
4. Tetratsükliinid, mis sisaldavad 4 kuueliikmelist tsüklit (tetratsükliin, metatsükliin
lin, doksütsükliin, morfotsükliin) aminoglükosiidid, mis sisaldavad aminosuhkru molekule (gentami-
cyn, kanamütsiin, neomütsiin, streptomütsiin)
5. Polüpeptiidid (polümüksiinid B, E, M)
6. Erinevate rühmade antibiootikumid (vankomütsiin, famitsidiin, levomütsetiin, rifa-
mitsiin, linkomütsiin jne)
Beeta-laktaamantibiootikumid
Penitsilliinid
Kuigi ajalooliselt olid penitsilliinid esimesed antibiootikumid, on need siiani selle klassi kõige laialdasemalt kasutatavad ravimid. Penitsilliinide antimikroobse toime mehhanism on seotud rakuseina moodustumise häiretega.
Eraldage looduslikud (bensüülpenitsilliin ja selle soolad) ja poolsünteetilised penitsilliinid. Poolsünteetiliste antibiootikumide rühmas on omakorda:
Penitsillinaasiresistentsed ravimid, millel on domineeriv toime
grampositiivsed bakterid (oksatsilliin),
Laia toimespektriga ravimid (ampitsilliin, amoksitsilliin),
Laia toimespektriga ravimid, mis on tõhusad sünergia vastu
küünepulgad (karbenitsilliin).
Bensüülpenitsilliin on valitud ravim pneumokokkide, streptokokkide, meningokokkide, treponema pallidum'i ja stafülokokkide põhjustatud infektsioonide korral, mis ei tooda beetalaktamaasi. Enamik neist patogeenidest on tundlikud bensüülpenitsilliini suhtes päevaste annuste 1-10 miljonit ühikut. Enamikule gonokokkidele on iseloomulik resistentsuse tekkimine penitsilliinide suhtes ja seetõttu ei ole need praegu eelistatud ravimid tüsistusteta gonorröa raviks.
Oksatsilliin on oma toimespektrilt sarnane bensüülpenitsilliiniga, kuid see on efektiivne ka penitsillinaasi (beeta-laktamaasi) tootvate stafülokokkide vastu. Erinevalt bensüülpenitsilliinist on oksatsilliin efektiivne ka suukaudsel manustamisel (happekindel) ja kooskasutamisel suurendab oluliselt ampitsilliini (kombineeritud preparaat Ampiox) efektiivsust. Ampitsilliini kasutatakse annustes 250-500 mg 4 korda päevas, banaalsete kuseteede infektsioonide suukaudseks raviks, mille peamisteks põhjustajateks on tavaliselt gramnegatiivsed bakterid, ning sega- või sekundaarsete kuseteede infektsioonide raviks. ülemised hingamisteed (sinusiit, keskkõrvapõletik, bronhiit). Karbenitsilliini peamine eristav eelis on selle efektiivsus Pseudomonas aeruginosa ja Proteuse vastu ning sellest tulenevalt saab seda kasutada mädanevates (gangrenoossetes) nakkusprotsessides.
Penitsilliinid võivad olla kaitstud bakteriaalsete beetalaktamaaside toime eest, kui neid manustada koos beetalaktamaasi inhibiitoritega, nagu klavulaanhape või sulbaktaam. Need ühendid on struktuurilt sarnased beeta-laktaamantibiootikumidega, kuid neil endil on tühine antimikroobne toime. Need inhibeerivad tõhusalt mikroorganismide beeta-laktamaasi, kaitstes seeläbi hüdrolüüsitavaid penitsilliinide inaktiveerimist nende ensüümide poolt ja suurendades seeläbi nende efektiivsust.
Kahtlemata on penitsilliinid kõigist antibiootikumidest kõige vähem toksilised, kuid allergilisi reaktsioone esineb sagedamini kui teisi antibiootikume. Tavaliselt ei ole need ohtlikud nahareaktsioonid (lööve, punetus, sügelus), eluohtlikud rasked anafülaktilised reaktsioonid on harvad (umbes 1 juhtum 50 000 patsiendist) ja tavaliselt intravenoossel manustamisel. Kõiki selle rühma ravimeid iseloomustab rist-ülitundlikkus.
Kõik penitsilliinid suurtes annustes ärritavad närvikudet ja suurendavad järsult neuronite erutatavust. Sellega seoses peetakse praegu penitsilliinide sisestamist seljaaju kanalisse põhjendamatuks. Harvadel juhtudel, kui bensüülpenitsilliini annust ületatakse rohkem kui 20 miljoni ühiku võrra päevas, ilmnevad ajustruktuuride ärrituse tunnused.
Suukaudseks manustamiseks mõeldud penitsilliinide seedetrakti ärritav toime avaldub düspeptiliste sümptomitena, eriti iivelduse, oksendamise, kõhulahtisuse korral, on kõige tugevam laia toimespektriga ravimite puhul, kuna nende kasutamisel tekib sageli superinfektsioon (kandidoos). Ärritav toime manustamisviisidel ilmneb intramuskulaarse süstimise korral tihendamise, lokaalse valu ja intravenoosse manustamise korral - tromboflebiit.
Tsefalosporiinid
Tsefalosporiinide struktuuri tuumaks on 7-aminotsefalosporaanhape, mis on äärmiselt sarnane penitsilliinide struktuuri aluseks oleva 6-aminopenitsillaanhappega. See keemiline struktuur määras kindlaks antimikroobsete omaduste sarnasuse penitsilliinidega, millel on resistentsus beetalaktamaaside toime suhtes, samuti antimikroobse toime mitte ainult grampositiivsete, vaid ka gramnegatiivsete bakterite vastu.
Antimikroobse toime mehhanism on täiesti sarnane penitsilliinide omaga. Tsefalosporiinid jagunevad traditsiooniliselt "põlvkondadeks", mis määravad nende antimikroobse toime põhispektri.
Esimese põlvkonna tsefalosporiinid (tsefaleksiin, tsefradiin ja tsefadroksiil) on väga aktiivsed grampositiivsete kokkide, sealhulgas pneumokokkide, viridestsentsete streptokokkide, hemolüütilise streptokoki ja Staphylococcus aureuse vastu; samuti seoses gramnegatiivsete bakteritega - Escherichia coli, Klebsiella, Proteus. Neid kasutatakse kuseteede infektsioonide, lokaliseeritud stafülokoki infektsioonide, polümikroobsete lokaliseeritud infektsioonide, pehmete kudede abstsesside raviks. Teise põlvkonna tsefalosporiine (tsefuroksiim, tsefamandool) iseloomustab laiem toimespekter gramnegatiivsete bakterite vastu ja need tungivad paremini enamikku kudedesse. Kolmanda põlvkonna ravimid (tsefotaksiim, tseftriaksoon) on veelgi laiema toimespektriga, kuid vähem tõhusad grampositiivsete bakterite vastu; Selle rühma tunnuseks on nende võime tungida läbi hematoentsefaalbarjääri ja sellest tulenevalt kõrge efektiivsus meningiidi korral. Neljanda põlvkonna tsefalosporiine (tsefpiroom) peetakse reservantibiootikumideks ja neid kasutatakse multiresistentsete bakteritüvede põhjustatud infektsioonide ja raskete püsivate haiglanakkuste korral.
Kõrvalmõjud. Nagu ka penitsilliinide suhtes, avaldub ülitundlikkus tsefalosporiinide suhtes sageli kõikidel variantidel. Sel juhul on võimalik ka risttundlikkus penitsilliinide ja tsefalosporiinide suhtes. Lisaks on võimalikud lokaalsed ärritavad toimed, hüpoprotrombineemia ja suurenenud verejooks, mis on seotud K-vitamiini metabolismi häirega, ning teturamilaadsed reaktsioonid (etüülalkoholi metabolism on häiritud äärmiselt toksilise atseetaldehüüdi akumuleerumisega).
Karbapeneemid
See on uus ravimite klass, mis on struktuurilt sarnased beetalaktaamantibiootikumidega. Selle ühendite klassi esimene esindaja on imipeneem. Ravimit iseloomustab lai antimikroobse toime spekter ja kõrge aktiivsus nii grampositiivsete, gramnegatiivsete kui ka anaeroobsete mikroorganismide vastu. Imipeneem on beetalaktamaasi suhtes resistentne.
Imipeneemi kasutamise peamised näidustused on hetkel täpsustamisel. Seda kasutatakse teiste saadaolevate antibiootikumide suhtes resistentsuse korral. Pseudomonas aeruginosa tekitab kiiresti resistentsuse imipeneemi suhtes, seetõttu tuleb seda kombineerida aminoglükosiididega. See kombinatsioon on efektiivne neutropeeniaga palavikuga patsientide raviks. Imipeneem peaks olema reservantibiootikum ja see on ette nähtud ainult raskete haiglanakkuste (sepsis, peritoniit, kopsupõletik) raviks, eriti mikroobide resistentsuse korral teiste antibiootikumide või tundmatu patogeeni suhtes, agranulotsütoosi või immuunpuudulikkusega patsientidel.
Imipeneemi efektiivsust saab suurendada, kombineerides seda tsilastatiiniga, mis vähendab selle eritumist neerude kaudu (kombineeritud ravim tienam).
Kõrvaltoimed ilmnevad iivelduse, oksendamise, nahalööbe, süstekoha ärrituse kujul. Penitsilliinide suhtes ülitundlikud patsiendid võivad olla ülitundlikud ka imipeneemi suhtes.
Monobaktaamid
Selle antibiootikumide rühma esindajaks on astreonaam, mis on väga tõhus antibiootikum gramnegatiivsete mikroorganismide (E. coli, Salmonella, Klebsiella, Haemophilus influenzae jt) vastu. Seda kasutatakse septiliste haiguste, meningiidi, sellisest taimestikust põhjustatud ülemiste hingamisteede ja kuseteede infektsioonide raviks.
Aminoglükosiidid
Selle rühma antibiootikumid on vees lahustuvad ühendid, mis on lahuses stabiilsed ja leeliselises keskkonnas aktiivsemad. Suukaudsel manustamisel imenduvad need halvasti, seetõttu kasutatakse neid kõige sagedamini parenteraalselt. Neil on bakteritsiidne toime, mis on tingitud valgu sünteesi pöördumatust pärssimisest mikroorganismi ribosoomidel pärast ravimi tungimist mikroobirakku. Aminoglükosiidid on tõhusad enamiku grampositiivsete ja paljude gramnegatiivsete bakterite vastu.
Kõik aminoglükosiidid toimivad ainult rakuvälistele mikroorganismidele ja nende tungimine mikroobirakku on aktiivne transpordist, energiast, pH-st ja hapnikust sõltuv protsess. Aminoglükosiidid on efektiivsed ainult mikroorganismide vastu, mis teostavad sellist mehhanismi rakupinnal, näiteks Escherichia coli. Bakterid, millel selline mehhanism puudub, ei ole aminoglükosiidide suhtes tundlikud. See seletab aminoglükosiidide aktiivsuse puudumist anaeroobide suhtes, aminoglükosiidide toime puudumist abstsesside korral (abstsessiõõnes, kudede nekroosi piirkondades), luude, liigeste, pehmete kudede infektsioone, kui esineb hapestumine. mikroobide elupaik, vähenenud hapnikuvarustus, vähenenud energia metabolism. Aminoglükosiidid on efektiivsed, kus normaalne pH, pO2, piisav energiavarustus – veres, neerudes. Aminoglükosiidide mikroobirakku tungimise protsessi hõlbustavad oluliselt rakuseinale mõjuvad ravimid, nagu penitsilliinid, tsefalosporiinid.
Aminoglükosiide kasutatakse gramnegatiivsete soolebakterite põhjustatud infektsioonide (kopsupõletik, bakteriaalne endokardiit) või gramnegatiivsete ja teiste antibiootikumide suhtes resistentsete bakterite sepsise kahtluse korral. Streptomütsiin ja kanamütsiin on tõhusad tuberkuloosivastased ravimid.
Kõrvaltoimeteks on see, et kõigil aminoglükosiididel on erineva raskusastmega oto- ja nefrotoksiline toime. Ototoksilisus avaldub esmalt kuulmise halvenemises (kõrvakõrva kahjustus) seoses kõrgsageduslike helide või vestibulaarsete häiretega (liigutuste koordinatsiooni häired, tasakaalukaotus). Nefrotoksilist toimet diagnoositakse kreatiniini taseme tõusuga veres või kreatiniini kliirensi suurenemisega neerude kaudu. Väga suurtes annustes avaldavad aminoglükosiidid kurareetaolist toimet kuni hingamislihaste halvatuseni.
Tetratsükliinid
Tetratsükliinid on suur antibiootikumide perekond, millel on sarnane struktuur ja toimemehhanism. Rühma nimi tuleneb keemilisest struktuurist, millel on neli sulanud rõngast.
Antibakteriaalse toime mehhanism on seotud valgu sünteesi pärssimisega ribosoomides, see tähendab, et selle saavutamiseks on vajalik ravimi tungimine mikroorganismi. Kõigil tetratsükliinidel on bakteriostaatiline toime ja neil on lai antibakteriaalne toime. Nende toimespekter hõlmab paljusid grampositiivseid ja gramnegatiivseid baktereid, aga ka riketsiat, klamüüdiat ja isegi amööba.
Kahjuks on praegu paljudel bakteritel tekkinud resistentsus selle antibiootikumide rühma suhtes nende algselt ebamõistlikult laialdase kasutamise tõttu. Resistentsus on reeglina seotud tetratsükliinide mikroorganismidesse tungimise takistamisega.
Tetratsükliinid imenduvad peensoole ülaosast üsna hästi, kuid piima, kaltsiumi-, raua-, mangaani- või alumiiniumkatiooniderikaste toitude samaaegne tarbimine, samuti tugevalt aluseline keskkond nõrgendavad nende imendumist oluliselt. Ravimid jaotuvad kehas suhteliselt ühtlaselt, kuid läbivad halvasti hematoentsefaalbarjääri. Ravimid tungivad aga hästi läbi hematoplatsentaarse barjääri ja on võimelised seonduma loote kasvavate luude ja hammastega. Eritub peamiselt sapiga ja osaliselt neerude kaudu.
Kõrvaltoimed - iiveldus, oksendamine, kõhulahtisus, mis on tingitud enda soolefloora allasurumisest. Laste luude ja hammaste arengu rikkumine kaltsiumiioonide seondumise tõttu. Pikaajalisel kasutamisel on võimalik toksiline toime maksale ja neerudele, samuti valgustundlikkuse areng.
makroliidid
Selle antibiootikumide rühma vana põlvkonna esindajad on erütromütsiin ja oleandomütsiin. Need on kitsa toimespektriga antibiootikumid, mis on efektiivsed peamiselt grampositiivsete bakterite vastu, pärssides valgusünteesi. Ravimid lahustuvad vees halvasti, seetõttu kasutatakse neid reeglina sees. Tablett peab aga olema kaetud maomahla kahjustava toime eest. Ravim eritub peamiselt neerude kaudu. Erütromütsiin on valitud ravim difteeria, samuti hingamisteede ja urogenitaalsüsteemi klamüüdiainfektsioonide korral. Lisaks on selle ravimirühma väga sarnase toimespektri tõttu penitsilliinide asendaja nende suhtes allergia korral.
Viimastel aastatel on kasutusele võetud selle rühma uue põlvkonna ravimid - spiramütsiin (rovamütsiin), roksitromütsiin (rulid), asitromütsiin (sumamed). Need on laia toimespektriga ravimid, millel on peamiselt bakteritsiidne toime. Suukaudsel manustamisel on neil hea biosaadavus, need tungivad hästi kudedesse ja akumuleeruvad spetsiifiliselt nakkus- ja põletikulise protsessi kohtadesse. Neid kasutatakse ülemiste hingamisteede nakkushaiguste, keskkõrvapõletiku, põskkoopapõletiku jne mitteraskete vormide korral.
Makroliidid on üldiselt vähetoksilised ravimid, kuid ärritava toime tulemusena võivad nad suukaudsel manustamisel põhjustada düspepsiat ja veenisisesel manustamisel flebiiti.
Polümüksiinid
Sellesse rühma kuuluvad polüpeptiidsed antibiootikumid, mis on efektiivsed gramnegatiivse taimestiku vastu. Tõsise nefrotoksilisuse tõttu ei soovitata kasutada kõiki polümüksiinid peale B ja E. Nende toimemehhanism on kleepumine gramnegatiivsete mikroorganismide rakuseinale ja selle tõttu toitainete läbilaskvuse rikkumine. Grampositiivsed bakterid on polümüksiinide toime suhtes resistentsed, kuna need ei sisalda seinas lipoide, mis on vajalikud nende antibiootikumide fikseerimiseks. Need ei imendu soolestikust ja parenteraalsel manustamisel avaldub nende tugev nefrotoksilisus. Seetõttu kasutatakse neid kas lokaalselt või lokaalselt – pleuraõõne, liigeseõõne jne. Need erituvad peamiselt neerude kaudu. Muud kõrvaltoimed on vestibulaarsed häired ja sensoorsed häired.