Bakteriaalne. Saade nahainfektsioonid viiakse läbi kontaktmehhanismi abil. Rahvarohketes kohtades ja ebasanitaarsetes tingimustes levivad haigused kiiresti. Nahainfektsioone võivad põhjustada paljud mikroorganismid. Kõige levinumad on Staphylococcus aureus ja Streptococcus pyogenes.
Bakterid, mis põhjustavad naha ja pehmete kudede infektsioone:
- S. aureus: impetiigo, furunkuloos, mitteavanev pais, toksiline epidermaalne nekrolüüs, äge paronühhia
- S. pyogenes: tselluliit, erüsiipel, impetiigo
- C. diphtheriae: difteeria (nahavorm)
- M. tuberculosis: luupus vulgaris
- M. marinum: kroonilised haavandilised nahakahjustused
- M. ulcerans: hävitavad haavandid (Buruli haavand)
- C. minutissimum: erütrasma
- Pseudomonas aeruginosa: põletuste koloniseerimine
- Erysipelothrix rhusiopathiae: erysipeloid
Kell tselluliit põhjustatud S. pyogenes, S. aureus, Pasteurella multocida, harvem elutsevate vibrioonide poolt. merevesi, ja gramnegatiivsed batsillid, mõjutavad kõik naha kihid. Mikroorganismid sisenevad inimkehasse kahjustatud naha, haavade ja putukahammustuste kaudu. Bakterioloogiliste tulemuste saamiseni tuleb alustada empiirilist ravi flukloksatsilliiniga. Rasketel juhtudel intravenoosselt antibakteriaalsed ravimid(bensüülpenitsilliin ja flukloksatsilliin).
Nekrotiseeriv fastsiit- kiiresti progresseeruv infektsioon, mis mõjutab ka nahka ja nahaalust kude. Haigus areneb segainfektsiooni tagajärjel, mida põhjustavad aeroobsed ja anaeroobsed mikroorganismid, samuti S. pyogenes monoinfektsiooni tõttu. Haigus areneb kiiresti ja võib väga lühikese aja jooksul põhjustada patsiendi surma. lühikest aega. Ravis mängib olulist rolli nakatunud nekrootiliste kudede edukas ekstsisioon bensüülpenitsilliini, kolmanda põlvkonna tsefalosporiinide ja metronidasooliga ravi ajal.
erütrasma- pindmine infektsioon, mis tekib jäsemete painutuspindadel ja mille põhjustajaks on Corynebacterium minutissimum. Kahjustused fluorestseerivad ultraviolettvalguses. Patogeeni saab isoleerida kultuuri abil. Ravi on erütromütsiin või tetratsükliin.
erysipelas - strep-infektsioon mis mõjutab orgaanilisi nahapiirkondi näol või jalgadel. Uuringu käigus täheldatakse tavaliselt leukotsüütide arvu suurenemist perifeerses veres. Ravi jaoks on ette nähtud suukaudne amoksitsilliin ja flukloksatsilliin; rasketel juhtudel võib see osutuda vajalikuks intravenoosne manustamine antibiootikumid.
Erysipeloid on Erysipelothrix rhusiopathiae põhjustatud zoonootiline infektsioon. Kohalikku fookust (tavaliselt sõrmed) iseloomustab punakasvioletse erüteemi teke. Riskirühma kuuluvad lihunikud (nakatunud lihaga töötamisel kannatavad sõrmed, sagedamini sead) ja kalurid. Enamasti taandub haigus iseenesest, kuid penitsilliini või tetratsükliini suukaudne kasutamine võib paranemisprotsessi kiirendada, sekundaarse baktereemia tekkeks on antibiootikumide määramine kohustuslik.
põletused võib põhjustada infektsioone Pseudomonas aeruginosa, S. aureus, S. pyogenes ja mõnikord ka soolebakteritega. Võimalik on nakatumine antibiootikumiresistentsete mikroorganismide vormidega. Bakteriaalne infektsioon võib põhjustada siirdatud naha äratõukereaktsiooni ja sekundaarset baktereemiat.
Paronühhia. Paronühhia ehk periungaalse koe põletik on levinud haigus, mis tuleneb bakterite (nt S. aureus) invasioonist küünenaha vigastuse kohtades. See põhjustab valu, turset, millele järgneb väikese abstsessi moodustumine. Abstsess dreneeritakse ja määratakse antibiootikumravi (flukloksatsilliin jne).
Nahainfektsioonide põhjusedSüsteemsete infektsioonide nahailmingud
peal nahka süsteemsete infektsioonide ilmingud võivad kajastuda. Eeskuju võib olla petehhiaalne lööve koos meningokoki septitseemiaga - raske sepsise vaieldamatu märk. Pseudomonas aeruginosa septitseemiaga patsientidel tekivad nahal gangrenoossed kolded (gangrenoosne ektüüm). Vähem väljendunud nahamuutused endokardiidil (küünte põhjas esinev hemorraagia). Stafülokoki septitseemia korral tekivad nahainfarkti piirkonnad ja mõnega viirushaigused nahalööbed muutuvad iseloomuliku kliinilise pildi osaks (tuulerõuged ja leetrid).
Sest viirus herpes simplex nahk - esmane fookus infektsioonid. Mõned Staphylococcus aureuse ja beetahemolüütiliste streptokokkide tüved põhjustavad süsteemsed haigused, mis on põhjustatud toksiinide toimest ja millega kaasnevad mitmesugused nahamuutused: koos sündroomiga toksiline šokk- generaliseerunud ja lööve peopesadel, sarlakid - lööve koos nasolabiaalse kolmnurga kahvatusega ja vastsündinutel põletatud naha sündroomiga - tugev koorumine.
Tüükad kui nahainfektsioon
Inimese papilloomiviiruse mõjutab naharakke ja suurendab nende paljunemist, mille tulemuseks on tüüka (papilloom) moodustumine. Papilloomid on papulaarsed, laigulised ja mosaiiksed, aga ka plantaarne (sarvjas) soolatüügas. Haigus edastatakse otsesel kokkupuutel patsiendiga, samuti tavaliste esemete kaudu, eriti kõrge õhuniiskuse korral (koos ujudes basseinis).
Kondüloomide edasikandumine (kondüloomid) viiakse läbi seksuaalselt. Diagnoos põhineb kliinilised tunnused. Kondüloomiviiruse määramiseks kasutatakse immunofluorestsentsreaktsiooni ja polümeraasi ahelreaktsiooni.
Papilloomiviirused põhjus pahaloomulised kasvajad emakakael (tüüp 16 ja 18) ja kõri (tüüp 6 ja 11). Praegu on olemas vaktsiinid viiruste tüüpide 16 ja 18 vastu, mis moodustavad pikaajalise immuunsuse.
Papilloomid aja jooksul kaovad nad ise, jätmata arme (erandiks on vähenenud immuunsusega inimesed). Väga sageli kasutatakse eneseraviks kohalikke keratolüütilisi aineid ( salitsüülhape). Suguelundite tüükade puhul kasutatakse podophyllum thyroid*. Alternatiivina kasutatakse krüoteraapiat, mis kiirendab papilloomide kadumist. Moksibussiooni ei soovitata praegu kasutada sagedane kasutamineühel patsiendil.
Mõned tüved rõugeviirused kahjustada nahka ja põhjustada iseloomulikud sümptomid(Näiteks, molluscum contagiosum ja nakkav pustuloosne dermatiit).
Dermatofütoosid - naha seeninfektsioonid
Dermatofütoosi kliinilised tunnused. dermatofütoosiga ( ringuss) tekivad naastud, millega kaasneb sügelus ja punetus. Aja jooksul nende läbimõõt suureneb ja keskele moodustub kahvatu laik. Küünte kroonilise kahjustuse korral täheldatakse küünte värvimuutust ja hõrenemist ning peanaha haiguste korral kiilaspäisust ja armistumist. Haiguse nimetuse aluseks on nakkuskoht, näiteks pea dermatofütoos (tinea capitis - rõngasuss), keha dermatofütoos (tinea corporis).
Naha seeninfektsioonide laboratoorne diagnostika. Infektsiooni jaoks nahka Pange tähele kahjustatud piirkondade sära ultraviolettvalguses.
V laboris toimetada kahjustatud nahapiirkondadest kuivad kraabid, küüne- ja juukseproovid. Naatriumhüdroksiidi lahuses kuumutamisel muutuvad need värviliseks ja mikroskoopia ajal muutuvad nähtavaks seente hüüfid. Dermatofüüdid kasvavad Saburad dekstroosiagaril 30°C juures neli nädalat.
Identifitseerimine põhineb kolooniate morfoloogilised omadused, mikroskoopilise pildi tunnused (värvimine laktofenoolsinisega), biokeemilised uuringud, samuti 18S ribosomaalse RNA geeni sekveneerimine.
Atoopilise dermatiidi korral on soodsad tingimused nakkuse tekkeks nahal. Sageli kasvatatakse nahalt või ninaneelu limaskestalt Staphylococcus aureus(Staphylococcus aureus), Staphylococcus epidermalis (Staphylococcus epidermalis) ja oportunistlikud seened (Malassezia furfur, Candida, Rhodotomla rubra). Mikroobsed toksiinid toetavad allergilist põletikku. Sellist dermatiiti ravitakse halvasti.
Mis on nahainfektsioonid?
Stafülokokid põhjustavad stafülodermat, streptokokid streptodermat. Kõige sagedasem nahainfektsioon on segatüüpi - streptostafüloderma.
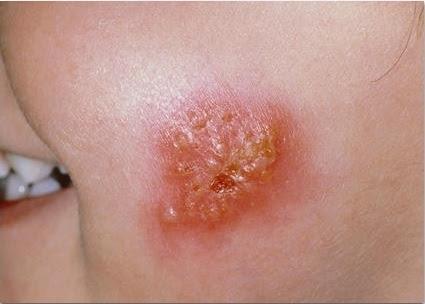
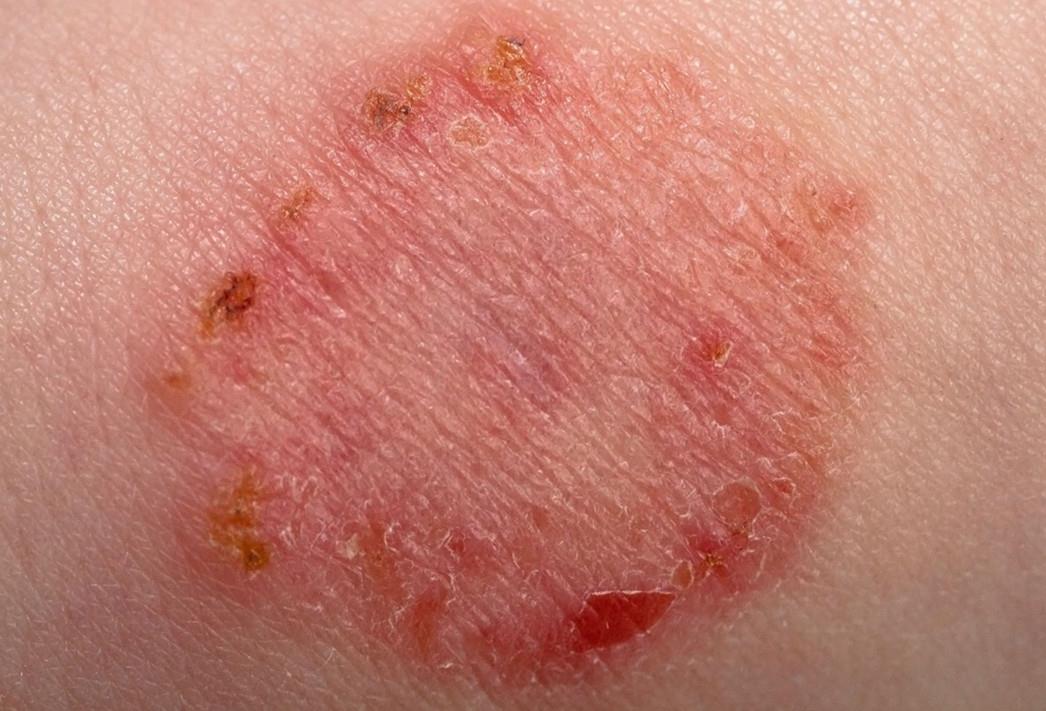
Pindmine stafüloderma- need on väikesed vesiikulid, millel on punasel taustal verine-mädane eritis, valged pustulid karvade ümber, näärmepõletik kaenlaalustes, kuulmekäikudes, päraku ümbruses ja suguelundites.
 |
 |
||
| Foto. Pindmise stafüloderma erinevad etapid. Kõik saab alguse ühest väikesest tuberkuloosist, mille ümber tärgavad ahelas uued elemendid. Muhud muutuvad mullideks ja mullid muutuvad koorikuteks. | |||
Sügav stafüloderma- need on keemised, karbunklid, nahaabstsessid.
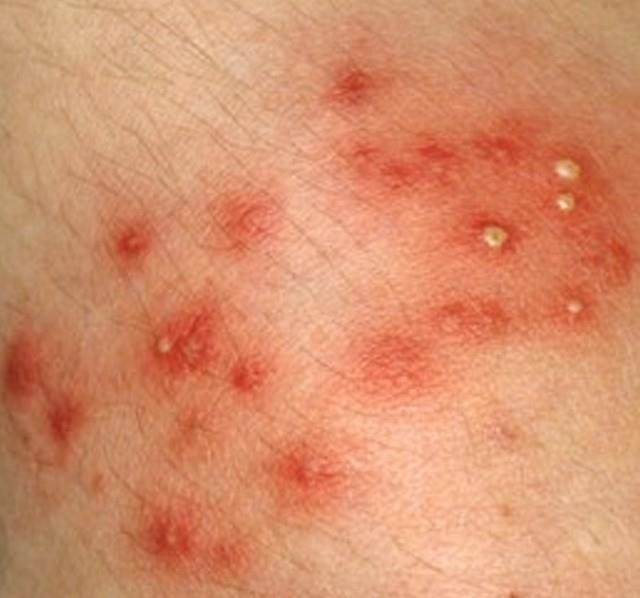 |
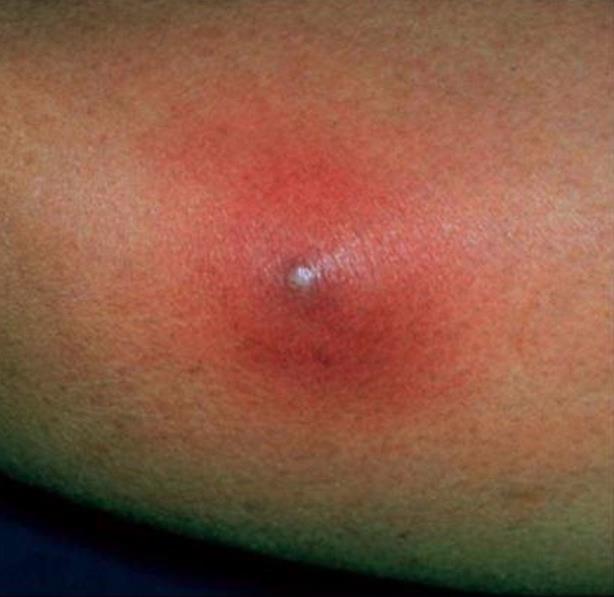 |
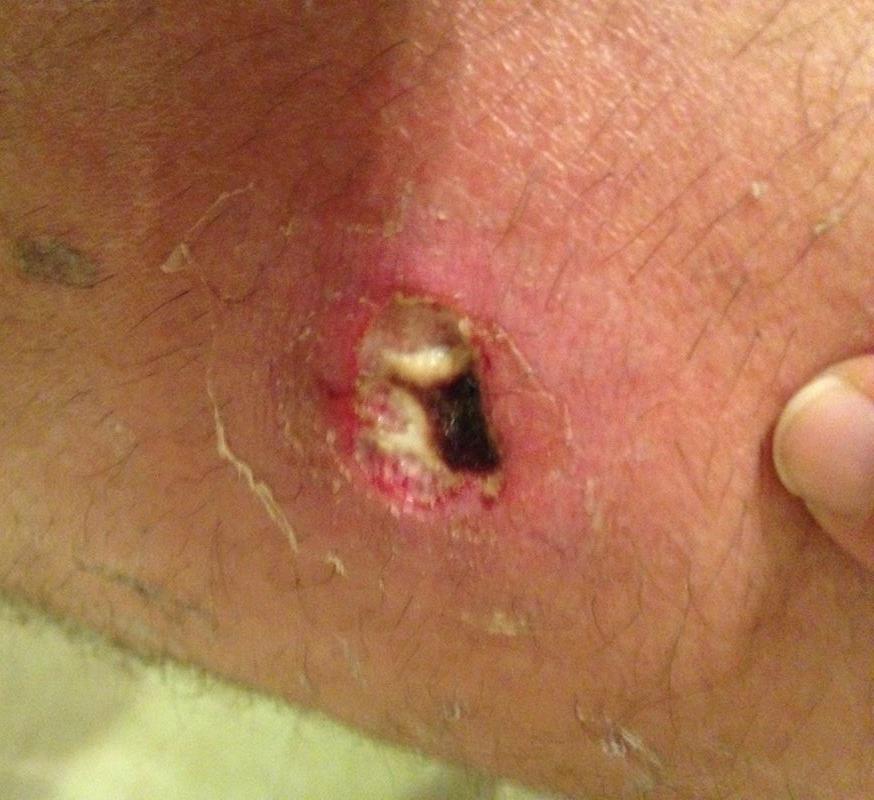 |
|
| Foto. A on follikuliit. B, C - furunkel. | |||
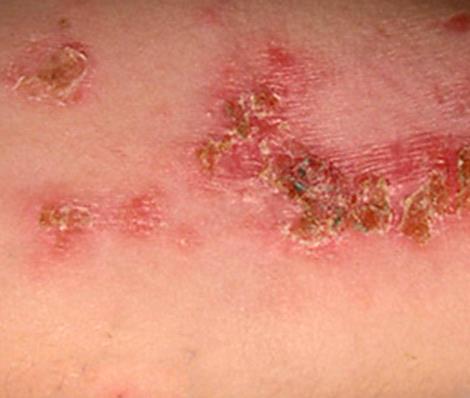
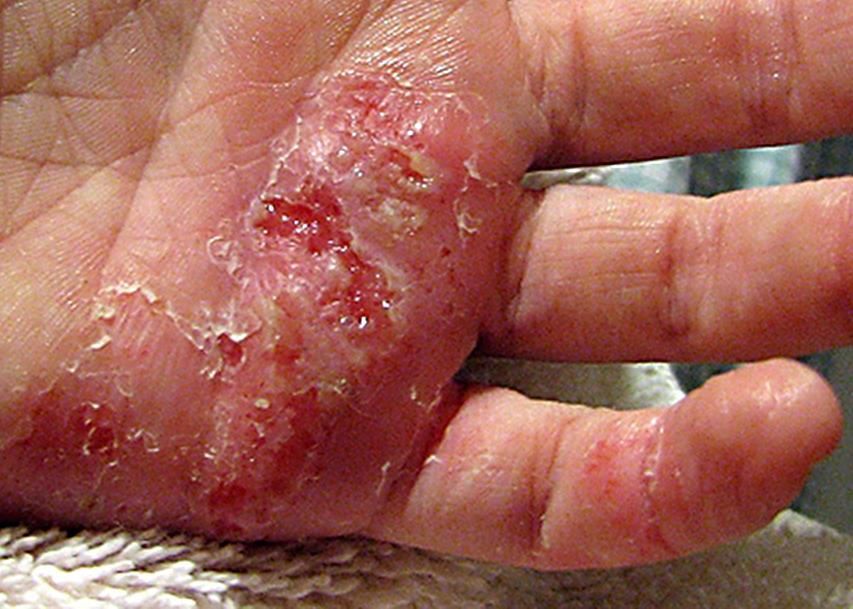
streptoderma- need on punasel taustal lõdvad villid, mis avanevad kiiresti ja moodustavad pruuni koorikuga haavandeid.
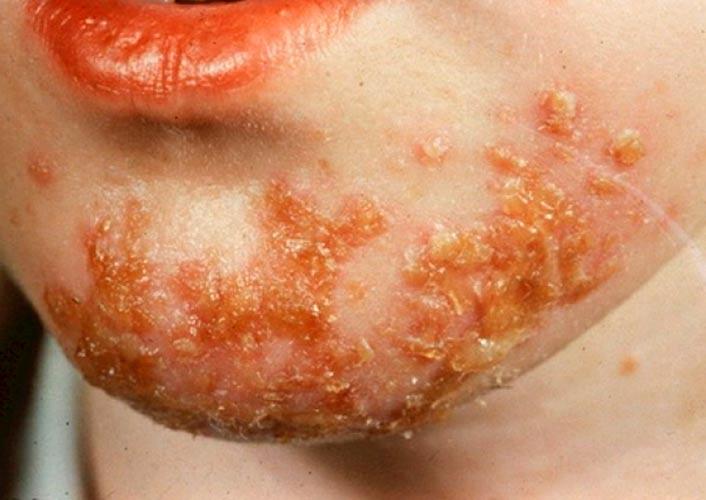 |
 |
 |
|
| Foto. Naha streptoderma. | |||
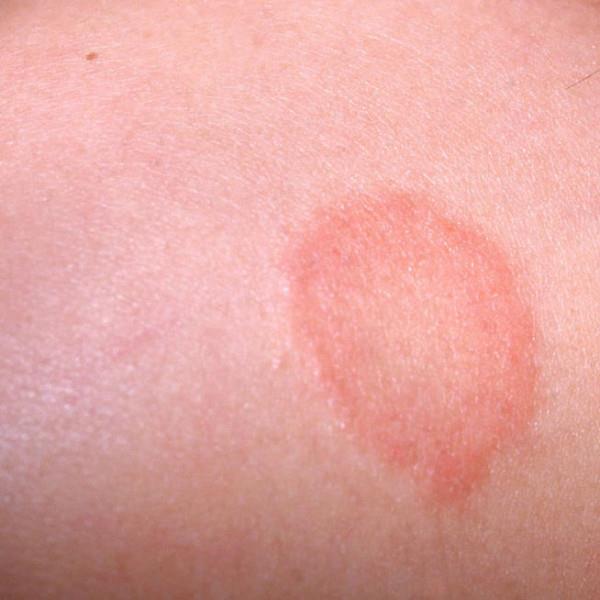
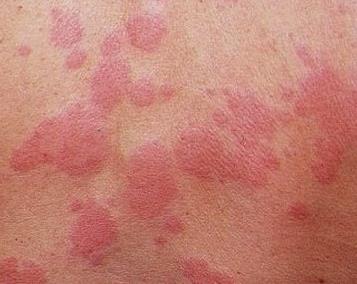
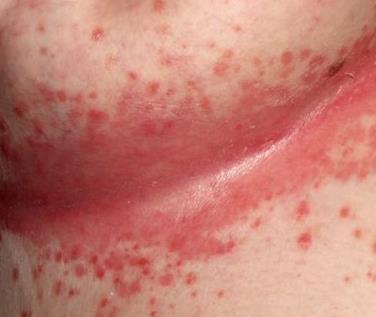
Naha seeninfektsioon- Need on erkpunased laigud, millel on selged kõrgendatud servad ja väga väikesed täpid-mullid; praod ja ärritus valgete laikudega; krambid suunurkades, lõhed ja põletik huultel valge kattega.
 |
 |
 |
|
| Foto. Naha seeninfektsioon. | |||
Kreemid, salvid, pihustid nahainfektsioonide raviks
Ravi jaoks nakkuslikud tüsistused atoopilise dermatiidi korral kasutatakse Tridermi kreemi (odavad analoogid - Akriderm, Candiderm, Kanizon plus), Pimafukorti (sarnased ravimid, ainult ilma seenevastase komponendita - Cortomycetin, Hyoxysone, Oxycort), Skin-cap (odavad analoogid - Zinocap, Desetin, tsingi salv, Sudocrem).
Triderm sisaldab hormooni (beetametasoondipropionaat 0,05%), antibiootikumi (gentamütsiinsulfaat 0,1%) ja seenevastast ainet (klotrimasool). Hormoonil on põletikuvastane ja sügelemisvastane toime. Antibiootikum tapab baktereid, sealhulgas Staphylococcus aureust. seenevastane aine pärsib seente kasvu. Tridermi kantakse lööbekolletele lastele alates 2. eluaastast ja täiskasvanutest 2-3 korda päevas 7-14 päeva jooksul.
Esimese eluaasta lastele on ravim soovitatav Pimafukort mis sisaldab hormooni hüdrokortisooni, seenevastane ravim natamütsiin, aga ka antibiootikum neomütsiin. Vahendit kantakse kahjustatud nahapiirkondadele 2-4 korda päevas mitte rohkem kui 10-14 päeva jooksul.
Pärast ravi tridermi või pimafukortiga saate üle minna pikaajaline ravi kreem Nahakate. Mittehormonaalne ravim Nahakate sisaldab aktiveeritud tsinki. Sellel on põletikuvastane, antimikroobne ja seenevastane toime (vt.).
Tähtis!!! Ravi viiakse läbi kuni infektsioonikolde täieliku kadumiseni.
Atoopilise dermatiidi ravikosmeetika
Pärast nakkuskollete eemaldamist viiakse läbi kohalik hooldusravi meditsiinilise kosmeetikaga.
DARDIA (lipo-piim, lipo-kreem, lipo-palsam), Mustela Stell Atopia, A-Derma liin, Aven (Derma-libur, Sicalfate), Vichy (lipidioos, nutrilozhi), Laboratoires Nygy-Charlieu (topikrem), Avene ( Trixera), Uriage (Cu-Zn-kreem, sprei), La Roche-Posay (Lipikar, Hydranorm) jne.
Pärast suplemist on vaja peale kanda niisutajaid ja pehmendavaid aineid, järgides “3 minuti reeglit” – kanda märjale nahale niisutajat 3 minuti jooksul pärast suplemist.
Antibiootikumid nahainfektsioonide jaoks
- kui tekib nahainfektsioon koos palaviku ja joobeseisundiga;
- kui sisse üldine analüüs vere põletikulised muutused;
- sügava stafülodermaga - furunkuloos, karbunklid, abstsessid;
- kui 3-5 päeva jooksul välistest ainetest mõju ei ilmne.
Makroliidid (Sumamed, Vilprafen, Klacid) ehk tsefalosporiinid II ja III põlvkond(Supraks, Zinnat, rasketel juhtudel - tseftriaksoon intravenoosselt). Ravikuur on 5-7 päeva.
Antibiootikumravi kombineeritakse väliste ainetega. Nahka töödeldakse Miramistiini, Kloorheksidiini, Fukortsini, briljantrohelise, sinise, Chlorfilipti, Bactrobani, süntüümilise emulsiooni, Levomikoliga.
Tähtis!!! Stafülokokk nahalt kaapimisel kaebuste puudumisel, samuti pindmine stafüloderma ei ole näidustus antibiootikumide võtmiseks. Ravi piirdub välise raviga.
Määrake seenevastased pillid
- kandidoosi invasiivsete vormidega (CKA määramine vereseerumis);
- dermatomütseedide nahast külvamisel mis tahes kontsentratsioonis;
- kui puudub mõju väliselt seenevastane ravi 3-5 päeva.
Flukonasooli (Diflucan, Flucostat, Mycosyst jt) kasutatakse kandidooside raviks. See on lubatud lastele alates sünnist. Flukonasool on aktiivne perekonna Candida, Rhodotorula ja Malassezia furfur pärmilaadsete seente, samuti ravimi suhtes tundlike dermatomütseedide vastu. Flukonasooli määratakse 3-5 mg / kg päevas 7-14 päeva jooksul (kapslid või suspensioon).
Terbinafiin (Lamisil jt) on ette nähtud dermatomütseedide ja hallitusseente (Aspergillus, Penicillium) nakatumiseks, samuti flukonasooli suhtes resistentsete kandidoossete infektsioonide korral. Ravim on lubatud alates 2 aastast. Annused: 2-5 aastat - 62,5 mg päevas; 5-12 aastat - 125 mg päevas; 12-15 aastat - 250 mg päevas. Kursus on 10-14 päeva - kerge kuluga, 2-3 nädalat - mõõdukaga, 3-4 nädalat - koos raske kurss.
Belousova T.A., Kayumova L.N., Goryachkina M.V.
Epidemioloogia
Bakteriaalsed infektsioonid nahka, põhjustades selle mädapõletikku, tuvastas Prantsuse teadlane H. Leloir 1891. aastal nakkuslike dermatooside rühmas püodermatiidi nime all (pyon - mäda, derma - nahk). Välismaal nimetatakse püodermat tavaliselt ulatuslikuks naha ja pehmete kudede infektsioonide rühmaks (SSTI), mis hõlmab lisaks naha ja adnexaalsete moodustiste infektsioonidele ka nahaaluse rasvkoe ja aluskudede infektsioone.
Majanduslikult arenenud riikides moodustab ICMT 1/3 kõigist nakkushaigused. Kodumaiste uuringute kohaselt moodustavad pustuloossed nahainfektsioonid tööealiste inimeste dermatoloogilisest patoloogiast 30–40%, sõjaväelastel ulatub see arv 60% -ni. Laste dermatoloogilises praktikas see patoloogia on üks sagedasemaid ja moodustab 30–50% kõigist arstikülastustest.
Etioloogia
ICMT peamine allikas on mikroorganismid, mis saastavad ja koloniseerivad nahapinda. Grampositiivsed kokid S. aureus ja S. Pyogenes, mis on võimelised tungima epidermise paksusesse selle kahjustuse korral, mängivad kahtlemata juhtivat rolli pustuloossete nahainfektsioonide etioloogias. Veelgi enam, S. aureus on kõige rohkem tavaline patogeen, S. pyogenes'e infektsioonid on mõnevõrra vähem levinud ja segainfektsioon mis hõlmavad mõlemat mikroorganismi. Välismaiste mitmekeskuseliste uuringute tulemuste kohaselt on lisaks S. aureus'ele S. pyogenes, Corynebacterium diphtheriae, P. aeruginosa, Enterobacteriaceae, Streptococcus spp. Väidetava patogeeni etioloogilise rolli määramisel on suur tähtsus infektsiooni tüübil. Erinevalt primaarsest püodermast on sekundaarsetel püodermadel, nagu enamikul nekrotiseerivatel ICMT infektsioonidel, polümikroobne etioloogia.
Nakkuse tekkes mängib olulist rolli mikroorganismi virulentsus ja bakteriaalse saastatuse määr. On näidatud, et nakkuse tekkimise tõenäosus on otseselt võrdeline mikroorganismi bakteriaalse saastumise ja virulentsuse astmega ning pöördvõrdeline mikroorganismi tugevusega. kaitsereaktsioon organism. Koloniseerimise tõenäosus suureneb allergiliste nahahaiguste esinemisel. Niisiis tuvastatakse atoopilise dermatiidiga patsientidel 90% juhtudest S. aureuse kahjustatud piirkondade koloniseerimine.
Patogenees
Ühe või teise püoderma vormi esinemisel mängivad suurt rolli patogeeni tüüp, selle virulentsus, makroorganismi seisund, aga ka mitmesugused endogeensed ja eksogeensed eelsoodumustegurid, mis vähendavad naha barjääri ja kaitsefunktsioone. .
Stafülokokkide ja streptokokkide virulentsuse määravad mitmed patogeensed toksiinid ja ensüümid, mida nad eritavad (koagulaas, leukotsidiin, streptokinaas, hüaluronidaas, streptolüsiin, hemolüsiinid jne), mis hõlbustavad patogeenide tungimist nahka, põhjustavad kahjustusi ja koorumist. kõikidest epidermise kihtidest põhjustavad pärisnaha ja selle all olevate kudede hemolüüsi ja nekroosi, häirides nende normaalset ainevahetust.
ICMT tekkes ja arengus suur tähtsus omavad keha reaktsioonivõimet, selle resistentsuse mehhanisme mikroobide agressiooni suhtes. Immunokompetentse süsteemi puudulikkus on sel juhul reeglina sekundaarne (omandatud). See võib moodustuda premorbiidsel perioodil mineviku või kaasuva tausta tõttu rasked haigused. Haigused endokriinsüsteem(rasvumine, diabeet, hüpofüüsi-neerupealiste süsteemi, kilpnäärme, sugunäärmete ebapiisav aktiivsus) aitavad kaasa keha infektsioonivastase kaitse mehhanismide vähenemisele. Rohkem kui pooled kroonilise püodermaga patsientidest (52%) kuritarvitavad süsivesikuid (tavaliselt kergesti seeditavaid), mis põhjustab pankrease isolaarse aparatuuri pidevat ülekoormust ja võib kaasa aidata häirete tekkele. süsivesikute ainevahetus erineval määral süsivesikute kogunemine kudedesse, mis on püokokkidele soodsaks toitainekeskkonnaks. Märkimisväärne roll on ka naha seborroilisel seisundil. Sebumi hulga suurenemise ja selle muutumise tõttu keemiline koostis esineb naha steriliseerimisomaduste vähenemine ja püogeensete kokkide aktiveerumine.
Vähese tähtsusega pustuloossete nahahaiguste tekkes on kroonilised nakkushaigused. erinevaid kehasid ja kuded: periodontaalne haigus, kaaries, igemepõletik, tonsilliit, farüngiit, urogenitaaltrakti infektsioonid, düsbakterioos, soole mürgistus, mis vähendavad organismi üldist ja kohalikku antibakteriaalset resistentsust ning aitavad kaasa sellele järgneva spetsiifilise sensibilisatsiooni tekkele patsientidel, mis süvendab nakkusprotsessi kulg. Märkimisväärset rolli kroonilise püoderma kujunemisel mängivad kesk- ja vegetatiivsed haigused närvisüsteem, vaimne või füüsiline ülekoormus, "kurnavad haigused" - alkoholism, nälg, alatoitumus (valkude, vitamiinide, mineraalsoolad, hüpovitaminoos, eriti A ja C. A-vitamiin osaleb keratiini moodustumise protsessis, C-vitamiin reguleerib läbilaskvust veresoonte sein, on kortikosteroidide sünergist). Olulist rolli püoderma kujunemisel mängivad mitmesugused kaasasündinud või omandatud immuunpuudulikkusest tulenevad immuunpuudulikkuse seisundid (HIV-infektsioon, glükokortikosteroidide, tsütostaatikumide ja immunosupressantide võtmine). Rakkude antibakteriaalse kaitse defektid neutrofiilide fagotsüütilise aktiivsuse pärssimise, kemotaksise kahjustuse, samuti opsooniliste tegurite vähenemise näol vereseerumis ja immunoglobuliinides soodustavad kroonilist infektsiooni ja sagedasi retsidiive.
T-rakulise immuunsüsteemi rikkumised on ICMT patogeneesis ülimalt olulised. Immunoloogilise reaktiivsuse spetsiifiliste mehhanismide häired põhinevad T-lümfotsüütide arvu vähenemisel perifeerses veres, CD3 ja CD4 rakkude arvu vähenemisel ning nende suhete muutumisel monotsüütidega, mis viib nõrgenemiseni. T-rakuline immuunvastus. Ebaõnnestumine immuunsussüsteem Patsiendi (immunoloogiline tasakaalustamatus) ja patogeeni antigeenne mimikri põhjustavad sageli kroonilist infektsiooni ja bakterikandja moodustumist ning antibiootikumide ebaratsionaalne kasutamine põhjustab patogeeni resistentsust.
Märkimisväärne tähtsus bakteriaalsete nahainfektsioonide tekkes on kahjulik mõju keskkond mis rikuvad naha terviklikkust ja loovad "sissepääsuvärava" nakkuse tungimiseks. Need hõlmavad peamiselt kõrge või madala temperatuuri, kõrge õhuniiskuse mõju, mis põhjustab naha leotamist, suurenenud saastumist ja mikrotrauma. professionaalsed tegurid(õlid, tsement, söetolm). Nakatumise sissepääsuvärav tekib leibkonna mikrotraumade (lõiked, süstid), sügelevate dermatoosidega kriimustustega. Nahabarjääri rikkumine sarvkihi kuivuse ja hõrenemise näol aitab kaasa mikroorganismide tungimisele naha sügavatesse kihtidesse ja aluskudedesse, mis viib püoderma protsessi arenguni.
ICMT kliinilised sordid
ICMT-d on üsna arvukad ja heterogeensed kliiniline pilt rühm haigusi, mis põhjustavad erineva sügavuse, levimuse ja raskusastmega kahjustusi. Kõigile ühine iseloomulik tunnus on kohaliku olemasolu mädane põletik, rasketel juhtudel, millega kaasneb süsteemse põletikulise reaktsiooni tekkimine. Kliinilised vormid sõltuvad etioloogilise teguri tüübist, anatoomilisest lokalisatsioonist, nahalisanditest kinnipidamisest, kahjustuse sügavusest ja piirkonnast, protsessi kestusest.
Kodumaises dermatoloogias aktsepteeritakse primaarse püoderma klassifikatsiooni, mille J. Jadasson pakkus välja juba 1934. aastal ja mis on ehitatud etioloogilisel põhimõttel. See eristab: stafülodermiat, mis mõjutab peamiselt nahka lisandite ümber (rasulised juuksefolliiklid, higinäärmed); mõjutav streptoderma sile nahk valdavalt looduslike avade ja strepto-stafülokoki segainfektsioonide ümbruses. Igas kolmes rühmas eristatakse sõltuvalt kahjustuse sügavusest pindmised ja sügavad vormid. Enamgi veel, pustuloossed haigused nahk jaguneb primaarseks, mis tekib muutumatul nahal, ja sekundaarseks, mis areneb tüsistustena juba olemasoleva dermatoosi taustal, tavaliselt sügelev (sügelised, ekseem, atoopiline dermatiit). Kursuse kestuse järgi eristatakse ägedat ja kroonilist püodermat. Stafülokoki püoderma on tavaliselt seotud naha lisanditega (juuksefolliiklid, apokriinnäärmed). Neid iseloomustab sügava pustuli moodustumine, mille keskele moodustub õõnsus, mis on täidetud mädane eksudaat. Perifeerias on erütematoosne-ödematoosne tsoon põletikuline nahk. Mädane protsess lõpeb armi moodustumisega. Streptokoki püoderma arenevad sagedamini siledale nahale, looduslike avade ümber (suuõõs, nina) ja algavad konfliktide tekkega - pindmiselt paiknev põis lõtv volditud rehviga, mille sees on seroosne-mädane sisu. Konflikti õhukesed seinad avanevad kiiresti ja sisu valgub naha pinnale, tõmbudes meekollasteks kihilisteks koorikuteks. Protsess kipub autoinkulatsiooni tagajärjel levima perifeeriasse. Mehed põevad sagedamini stafülodermat, naised ja lapsed streptodermat.
V väliskirjandus praktilisest vaatenurgast on kõik ICMTd jagatud kolme põhirühma: primaarne püoderma, mida valdavalt põhjustavad S. aureus ja püogeensed b-hemolüütilised streptokokid (peamiselt A-rühm) ning arenevad muutumatul nahal (follikuliit, impetiigo, erüsiipel); sekundaarne püoderma, mis areneb nahakahjustuste või kaasneva somaatilise patoloogia taustal (näiteks haavandid, diabeetiline jalahaavand, loomahammustuste järgsed infektsioonid, operatsioonijärgsed haavad ja traumajärgsed infektsioonid), samuti dermatooside taustal, millega kaasneb sügelus ja kriimustada ( allergiline dermatiit, psoriaas, sügelised jne); Nekrootilised infektsioonid esindavad kõige rohkem raske vorm ICMT (polümikroobse etioloogiaga tselluliit – sünergiline tselluliit, nekrotiseeriv fastsiit, münekroos – gaasigangreen). Selle patoloogia puhul on kahjustuse sügavuse ja ulatuse kindlaksmääramine kirurgi prioriteet, sest ainult kirurgilise raviga saab kõige täpsemalt kindlaks teha nakkuse tõelise astme. Nende patsientide esialgne ravi on sama. See seisneb varases kirurgilises sekkumises ja piisava antimikroobse ravi määramises.
ICMT ravi
Bakteriaalsete nahainfektsioonidega patsientide ravi peab olema kompleksne (etiotroopne ja patogeneetiline) ning see tuleb läbi viia pärast põhjalikku anamnestilist, kliinilist ja kliinilist uurimist. laboratoorne uuring haige. Vajab tuvastada ja ravida kaasnevad haigused, fokaalse infektsiooni fookuste uurimine ja pikaajalise püsiva protsessi korral - immunostaadi uuringud. ICMT-ga patsientide etiotroopse ravi peamine ja ainus meetod on antibiootikumid. Ägedate pindmiste aeg-ajalt esinevate protsesside (impetiigo, follikuliit, paronühhia) korral võib ravi piirduda antibiootikumide ja antiseptikumide lokaalse kasutamisega. Kõigil muudel juhtudel on vajalik süsteemne antibiootikumravi.
Süsteemse antibiootikumravi määramise näidustused on püoderma sügavad vormid: keeb (eriti lokaliseerimisega näol ja kaelal), karbunkel, hidradeniit, erüsiipel, tselluliit. Loetletud bakteriaalsete nahainfektsioonide vormidel on pikk, sageli krooniline retsidiveeruv kulg, protsessi kõrge levimus ja nendega kaasnevad sageli üldise mürgistuse sümptomid palaviku, peavalu, nõrkuse ja piirkondlike tüsistuste tekkega ( lümfadeniit, lümfangiit). Nagu etiotroopne aine antibiootikume kasutatakse bakteriaalse iseloomuga dermatoosi - Lyme'i tõve - ravis. Need on akne vulgarise ravis valitud ravimid. Dermatoveneroloogilises praktikas kasutatakse antibiootikume laialdaselt nii nakkuslike dermatooside kui ka sugulisel teel levivate infektsioonide (STI-de) põhjustatud haiguste raviks.
Enne antibakteriaalse ravimi väljakirjutamist on soovitav nakatada mäda, määrates kindlaks isoleeritud mikroorganismi tundlikkuse erinevate antibiootikumide suhtes ja uuringu tulemuste põhjal määrata sobiv ravim. Kuid see ei ole alati teostatav, eriti kui esineb nakkusoht või selle tüsistused. Nagu tänapäevase kirjanduse ja meie enda analüüs kliiniline kogemus Tänapäeval kasutatakse naha bakteriaalsete infektsioonide ravis kõige sagedamini järgmisi antibiootikumide rühmi: 1. β-laktaamid: a) looduslik penitsilliin, selle durantsed vormid ja poolsünteetilised penitsilliinid; b) tsefalosporiinid (1-4 põlvkonda). 2. Makroliidid. 3. Tetratsükliinid. 4. Fluorokinoloonid.
V viimased aastad penitsilliini ja selle durantseid preparaate kasutatakse ICMT ravis harva, kuna valdav enamus püokoki tüvedest on omandanud võime toota ensüümi b-laktamaasi (penitsillinaasi), mis pärsib penitsilliini antibakteriaalset toimet. Lisaks kuuluvad β-laktaamid ravimite hulka, millel on kõrge allergiliste reaktsioonide sagedus.
Tetratsükliine, aminoglükosiide kasutatakse praegu palju harvemini. Selle põhjuseks on nende antibiootikumide suhtes resistentsete mikroorganismide tüvede suur arv (mis tähendab nende madalat terapeutilist aktiivsust), samuti tõsiste kõrvaltoimete esinemine. Tuleb meeles pidada, et tetratsükliinid on vastunäidustatud rasedusele, lastele ja maksapuudulikkusega patsientidele.
Fluorokinoloone on ette nähtud peamiselt sugulisel teel levivate haiguste raviks, kuna kõrge tundlikkus nende jaoks urogenitaalsete infektsioonide patogeenid ja püoderma puhul kasutatakse ainult siis, kui teised antibiootikumide rühmad on ebaefektiivsed. Kesknärvisüsteemi haiguste, rasedate naiste, aga ka pediaatriliste haiguste korral on nende kasutusala piiratud - neid määratakse peamiselt tervislikel põhjustel. Arvesse tuleks võtta ka fluorokinoloonide valgustundlikkust suurendavat toimet ja sellega seotud ettevaatusabinõusid, eriti kevadel ja suvel.
Kaasaegne meditsiinipraktika seab teatud nõuded antibiootikumi valikule. Esiteks peab ravim olema lai valik antimikroobne toime ja minimaalselt väljendatud antibiootikumiresistentsus mikroobsete ainete suhtes, ei ole raske kõrvalmõjud, neil on minimaalne allergiliste reaktsioonide tekkerisk, patsiendile mugav kasutada (suukaudse vormi olemasolu, mugav annustamisrežiim) ja taskukohane. Lisaks on väga oluline, et antibiootikumil ei oleks kliiniliselt olulisi koostoimeid teiste antibiootikumidega ravimid. Praeguseks vastavad antibiootikumid - makroliidid - täielikult nendele nõuetele.
Makroliidide farmakoterapeutilise toime klassifikatsioon ja mehhanismid
Makroliide on laialdaselt kasutatud üle 50 aasta kliiniline praktika. Esiteks looduslik antibiootikum sellest rühmast - erütromütsiin (Streptomyces erythreuse metaboliit) saadi 1952. aastal. Makroliide saab klassifitseerida nende keemilise struktuuri ja päritolu järgi. alus keemiline struktuur selle antibiootikumide klassi puhul on makrotsükliline laktoonitsükkel. Sõltuvalt süsinikuaatomite arvust tsüklis jagunevad makroliidid 14-, 15- ja 16-liikmelisteks.
Makroliide on 3 põlvkonda:
esimene põlvkond: erütromütsiin, oleandomütsiin;
teine põlvkond: spiramütsiin, roksitromütsiin, josamütsiin, klaritromütsiin jne;
kolmas põlvkond: asitromütsiin (Azitral).
Makroliidide antibakteriaalne toime põhineb mikroobirakkude ribosomaalsete valkude sünteesi katkemisel ja seeläbi patogeeni paljunemisprotsessi pärssimisel. Peamiselt on neil bakteriostaatiline toime, mistõttu on soovitav neid välja kirjutada põletiku ägedas faasis. Makroliide nimetatakse "koe antibiootikumideks", st. kehas levides kogunevad nad peamiselt mitte vereringesse, vaid nendesse elunditesse ja kudedesse, kus esineb põletik, tekitades seeläbi kõrged kontsentratsioonid ravim. Organismis hästi jaotunud makroliidid suudavad ületada histohematoloogilised barjäärid (välja arvatud hematoentsefaalbarjäär), ületades selles oluliselt β-laktaamantibiootikume. Kuid laialdane (ja sageli põhjendamatu) kasutamine tõi kiiresti kaasa erütromütsiiniresistentsete patogeenide, eriti stafülokokkide tüvede suure protsendi. See omakorda vähendas oluliselt erütromütsiini kasutamist kliinilises praktikas.
Huvi makroliidide vastu tekkis taas 1980. aastate alguses, pärast seda, kui sellesse rühma ilmusid uued antibiootikumide põlvkonnad - asaliidid (eriti asitromütsiin). Asitromütsiin sünteesiti 1983. aastal erütromütsiinist. Oma farmakokineetiliste omaduste poolest ületas ravim kõiki oma eelkäija näitajaid ja sai esimeseks esindajaks. uus grupp antibiootikumid - asaliidid. Asitromütsiini ainulaadsus põhineb selle erakordsel farmakokineetikal. Asitromütsiin on stabiilne happeline keskkond tänu sellele imendub see pärast suukaudset manustamist hästi. Samaaegne tarbimine toiduga vähendab imendumist 50%, seega võetakse ravimit 1 tund enne või 2 tundi pärast sööki. Asitromütsiini molekuli lipofiilsus annab lisaks kõrge tase imendumine soolestikus ja ka ravimi suurepärane tungimine kudedesse. Samuti on tagatud asitromütsiini kiire tungimine verest kudedesse madal tase asitromütsiini seondumine verevalkudega, mis võimaldab saavutada kiiret terapeutiline toime infektsioonidega, mis mõjutavad rakke ja kudesid. Ravimi kõrge kontsentratsioon kahjustatud piirkonnas, 10–100 korda kõrgem kui vereringes, võimaldab teil aktiivselt mõjutada patogeenset fookust, tagades seeläbi kiire kliinilise toime ja kiire taastumise. Kaasaegsed makroliidid (eriti asitromütsiin) on kõige tõhusamad selliste patogeenide nagu S. pyogenus, S. aureus, S. pneumoniae, mõnede gramnegatiivsete mikroorganismide (gonokokkide) ja ka rakusiseste patogeenide (eelkõige Chlamidia trachomatis ja Ureaplasma urealyticum), mis põhjustab nende suurt nõudlust dermatoveneroloogilises praktikas.
Tähtsus Teise põlvkonna makroliidide antibakteriaalsel toimel on nende koostoime neutrofiilidega. Tänu oma võimele tungida neutrofiilidesse ja tekitada neis kõrgeid kontsentratsioone, muudavad paljud makroliidid positiivselt nende rakkude funktsioone, mõjutades eelkõige kemotaksist, fagotsütoosi ja tapmisaktiivsust. Sama hästi kui antimikroobne toime neil antibiootikumidel on mõõdukas põletikuvastane toime. Aktiveerides makrofaagide seeria rakke, suudavad nad neisse tungida ja kui fagotsüütrakud migreeruvad põletikukoldesse, sisenevad sinna koos nendega. Nende ravimite ainulaadsus seisneb ka selles, et neil on väljendunud antibiootikumijärgne toime, see tähendab, et nad säilitavad kõrge kontsentratsiooni põletikukoldes 5-7 päeva pärast ärajätmist. See sanogeneetiline toime võimaldas välja töötada lühikesed ravikuurid, mis ei ületa 3-5 päeva, ja mugava annustamisskeemi (1 kord päevas). See omakorda tagab ravile vastavuse ja parandab patsiendi elukvaliteeti. Asitromütsiini postbiootiline toime on kõige tugevam, mis võimaldab tekitada infektsioonikoldes antibiootikumi kontsentratsiooni, mis ületab kordades MIC aktiivsete patogeenide suhtes nii ägedate kui ka ägedate haiguste ravis. kroonilised infektsioonid. V Hiljuti tõendeid asitromütsiini immunomoduleeriva toime kohta saadi tervetel vabatahtlikel tehtud katses. Immunomoduleeriva toime esimene faas seisneb neutrofiilide degranulatsioonis ja oksüdatiivses plahvatuses, mis aitas kaasa kaitsemehhanismide aktiveerimisele. Patogeenide likvideerimiseni jõudmisel vähenes IL-8 tootmine ja neutrofiilide apoptoosi stimuleerimine, mis minimeeris põletikulise vastuse raskust.
Makroliidid, nii looduslikud kui ka poolsünteetilised, avaldavad minimaalset mõju normaalne mikrofloora Inimkeha ja ei põhjusta düsbioosi. Seetõttu peetakse asitromütsiini mitte ainult väga tõhusaks, vaid ka kõige tõhusamaks ohutu antibiootikum minimaalse arvu vastunäidustustega kohtumisel. Kõrvaltoimed tervikuna võttes on need äärmiselt haruldased ja ei ületa 5%. Kõige sagedasemad kõrvaltoimed on kõrvaltoimed seedetrakti(iiveldus, raskustunne epigastimaalses piirkonnas), mis reeglina on mõõdukad, ei nõua ravimi ärajätmist ja mööduvad pärast sööki ravimite võtmisel kiiresti.
Asitromütsiini kliiniline efektiivsus
Nagu näitavad võrdlevad uuringud, on ICMT-s kasutatud antibiootikumide hulgas ambulatoorne praktika, uue põlvkonna kõige tõhusamad makroliidid, peamiselt 15- ja 16-liikmelised (asitromütsiin, josamütsiin, roksitromütsiin). Asitromütsiini kasutamisest kodumaises dermatoveneroloogilises praktikas on juba kogunenud 20-aastane positiivne kogemus. Dermatoloogias on need stafülokokkide ja streptokokkide naha ja pehmete kudede kahjustuste (furunkel, impetiigo, tselluliit) põhiraviks ning venereoloogilises praktikas - STI-de ravis. Erinevalt enamikust makroliididest ei ole asitromütsiinil kliiniliselt olulisi ravimite koostoimeid. See ei seondu tsütokroom P450 kompleksi ensüümidega, mistõttu see ei reageeri ravimite koostoime seda rada mööda metaboliseeruvate ravimitega. See omadus on oluline, sest reaalses kliinilises praktikas on enamikul ICMT-ga haigetel tausta- või kaasuvad haigused, mille puhul nad saavad asjakohast ravi. Samuti tuleb rõhutada, et koos hea tolerantsuse ja väljendunud puudumisega kõrvaltoimed makroliididel (asitromütsiinil) on teiste antibiootikumide rühmade ees veel üks kindel eelis - see on see, et seda saab määrata rasedatele ja lastele.
Praegu on kliinilises praktikas üks enim kasutatavaid ravimeid ravim Azitral (asitromütsiin), mida toodab ravimifirma Shreya bioteadused. Azitraal (asitromütsiin) sarnaneb algse asitromütsiiniga, mis on asaliidide alarühma esimene esindaja ICMT ja urogenitaalsete infektsioonide ravis kasutatavate makroliidantibiootikumide rühmast. Uuringud on näidanud, et ravimi kliiniline efektiivsus, manustatuna ühekordse annusena 500 mg 3 päeva jooksul, on võrreldav enamkasutatavate ravimite omaga. antibakteriaalsed ained. See võimaldab vähendada tavalist antibiootikumravi kulgu 2-3 korda ja Azitrali ainulaadne farmakokineetiline profiil tagab ühekordse ravi. päevane tarbimine ja kõrge vastavus ravile.
Farmakokineetika iseärasuste ja omapärase antimikroobse toimespektri tõttu, mis hõlmab peamisi kuseteede infektsioonide patogeene, on asitromütsiin esmavaliku ravim kaasuvate STI-de, sealhulgas kroonilise tüsistunud urogenitaalse klamüüdia ja PID ravis. mitterasedad naised, ja alternatiivsed vahendid selle haiguse raviks raseduse ajal. 1 g asitromütsiini (Azitral) ühekordse annuse korral ületab selle kontsentratsioon nädala jooksul eesnäärme ja emaka kudedes C. trachomatise MIC (0,125 μg / ml) 42,5 korda ja emakakaela kanal- 12 korda, mis on terapeutiline kontsentratsioon selle infektsiooni raviks. Veelgi enam, isegi 2 nädala pärast ületab asitromütsiini terapeutiline kontsentratsioon eesnäärmekoes C. trachomatise MIC-i 13,6 korda. Autorid tõestasid, et just sellise sissevõtmisega kudedes, kus C. trachomatis vegeteerub, säilib ravimi kõrge terapeutiline kontsentratsioon 6-8 arengutsükli jooksul. Saadud andmed viitavad Azitrali pulssteraapia kõrgele efektiivsusele (1 g üks kord nädalas, kuuri annus 3 g). v kompleksne ravi krooniline klamüüdia uretroprostatiit ja sellega seotud mükoureaplasma ja gardnerella infektsioon. Oluline on märkida, et ravim Azitral on patsientidele hästi talutav, taskukohane ja seetõttu saab seda laialdaselt kasutada tüsistunud urogenitaalse klamüüdia ja PID ravis.
Asitromütsiini efektiivsuse, ohutuse ja talutavuse uurimine 30 lapsel vanuses 6 kuud kuni 3 aastat stafülokoki infektsioonid erinev lokaliseerimine ENT organid ja nahk näitasid, et asitromütsiin (Azitral) ei ole efektiivsuselt madalam kui antistafülokoki penitsilliinid. Sama hästi kui kõrge efektiivsusega, mida iseloomustab peamise kiire ja püsiv pöörddünaamika kliinilised sümptomid ja kohalik põletikulised muutused 100% juhtudest oli ravim hästi talutav ja puudus kõrvalmõjud kõigil lastel. Lai valik antimikroobset toimet, farmakokineetilised omadused, kõrvalnähtude väike protsent ja mitmed eelised teiste makroliidide ees määravad ravimi kasutamise prioriteedi erinevate nahahaiguste korral. nakkuslikud protsessid(impetiigo, furunkuloos, follikuliit, tselluliit, paronühhia) lastel. Asitromütsiini efektiivsus pediaatriline praktika, mida on tõestanud kliinilised uuringud, võimaldab meil seda soovitada alternatiivina b-laktaamantibiootikumidele ja lastele, kellel on raske allergiline ajalugu - valikravimina.
Üks olulisemaid farmakoökonoomilisi näitajaid, mis määrab antibiootikumi valiku, on kulu/efektiivsuse suhe. Seda määratletakse kulude suhtena uimastiravi(suukaudsete ravimite puhul võrdub see kursuse annuse maksumusega) edukalt ravitud patsientide osakaalu. Tuleb märkida, et Azitral on üks olemasolevad ravimid asitromütsiin näitab optimaalset hinna ja kvaliteedi suhet.
On teada, et antibiootikumravi ebaefektiivsuse määrab suuresti tundlikkuse vähenemine kasutatava ravimi suhtes. Praegu puudub asitromütsiini suhtes kliiniliselt oluline resistentsus. Antibiootikumiresistentsuse, asitromütsiini ja teiste makroliidide suhtes resistentsuse jälgimise järgi uusim põlvkond patogeenide hulgas ei ületa ICMT 2-10%. Venemaal isoleeritud S. pyogenes'e tüvede tundlikkus antibiootikumi asitromütsiini suhtes on 92%. Nagu on näidanud mitmed uuringud, on asitromütsiini kliiniline efektiivsus suurem kui tetratsükliinidel ja b-laktaamantibiootikumidel. 5-päevase asitromütsiini ja 10-päevase tsefaleksiini kuuri efektiivsuse võrdlev kliiniline ja mikrobioloogiline uuring sügava stafülodermia korral näitas makroliidi kõrgemat terapeutilist aktiivsust. Patogeeni likvideerimist asitromütsiini kasutamisega täheldati 94%, tsefaleksiiniga 90% juhtudest, kliinilist paranemist - vastavalt 56 ja 53% juhtudest. Samal ajal ei ületa kõrvaltoimete sagedus, mis tavaliselt ei nõua ravimi kasutamise katkestamist, 5%, mis on oluliselt madalam võrreldes erütromütsiini (kuni 14%) või b-laktaamide suukaudsete vormidega.
Seega on asitromütsiinil lai antimikroobse toime spekter, kõrge bakteriostaatiline toime selle suhtes tundlike infektsioonide vastu, kõrge biosaadavus koos selektiivse toimega põletikukoldes, sellel on madal toksilisus, minimaalne kõrvaltoime ja mugav manustamisviis. Seetõttu vastab ravim ratsionaalse antibiootikumiravi kaasaegsetele nõuetele ja seda võib soovitada tõhus rakendus dermatoveneroloogilises praktikas.
Kirjandus
1. Jones M.E., Karlowsky J.A., Draghi D.C, Thornsberry C., Sahm D.F., Nathwani D. Epidemioloogia ja tundlikkus antibiootikumidele Naha ja pehmete kudede infektsioone põhjustavate bakterite kohta USA-s ja Euroopas: sobiva antimikroobse ravi juhend. Int J Antimicrob Agent 2003; 22:406-19.
2. N.N. Muraškin, M.N. Gluzmina, L.S. Galustyan. Pustuloossed nahakahjustused laste dermatoloogi praktikas: värske pilk vanale probleemile. RZhKVB: Teaduslik ja praktiline ajakiri, 2008, nr 4, lk. 67-71.
3. Belkova Yu.A. Püoderma ambulatoorses praktikas. Haigused ja patogeenid. Kliiniline mikrobioloogia ja antimikroobne keemiaravi: nr 3, 7. köide, lk. 255-270, 2005.
4. T.A. Belousova, M.V. Gorjatškin. Bakteriaalsed nahainfektsioonid: optimaalse antibiootikumi valimise probleem. RMJ 2005, 13. köide, nr 16, lk. 1086-1089.
5. Takha T.V., Nazhmutdinova D.K. Püoderma antibiootikumiravi ratsionaalne valik. RMJ 2008, 16. köide, nr 8, lk. 552-555.
6. Novoselov V.S., Plieva L.R. Püoderma. RMJ 2004, 12. köide, nr 5, lk. 327-335.
7. Masjukova S.A., Gladko V.V., Ustinov M.V., Vladimirova E.V., Tarasenko G.N., Sorokina E.V. Bakteriaalsed nahainfektsioonid ja nende tähendus dermatoloogi kliinilises praktikas. Consilium medicum 2004, 6. köide, nr 3, lk. 180-185.
8. T.Fail. Naha ja pehmete kudede infektsioonide diagnoosimine ja antimikroobne ravi. Ohio, USA. Kliiniline mikrobioloogia ja antimikroobne keemiaravi: nr 2, 5. köide, lk. 119-125, 2003
9. Shlyapnikov S.A., Fedorova V.V. Makroliidide kasutamine naha ja pehmete kudede kirurgiliste infektsioonide korral. GRM, 2004.-kd.12, nr 4, s204-207
10. Guchev I.A., Sidorenko S.V., Frantsuzov V.N. Ratsionaalne antimikroobne kemoteraapia naha ja pehmete kudede infektsioonide korral. Antibiootikumid ja keemiaravi. 2003, v.48, 10, lk 25-31
11. Parsad D., Pandhi R., Dogras S. Juhend makroliidide valikuks ja sobivaks kasutamiseks nahainfektsiooni korral Am J Clin Dermatol 2003; 4:389-97
12. Jakovlev S.V., Ukhtin S.A. Asitromütsiin: põhiomadused, manustamisrežiimide optimeerimine farmakokineetika ja parameetrite põhjal. Antibiootikumid ja keemiaravi. 2003 v. 48, nr 2. - Koos. 22-27
13. Turovsky A.B., Kolbanova I.G. Makroliidid infektsioonide ravis hingamisteed kõrva-nina-kurguarsti ametikohalt: "poolt" ja "vastu" Consilium medicum, 2010, nr 4, köide 12, lk 11-14.
14. Prokhorovich E.A. Asitromütsiin. Alates kliiniline farmakoloogia kliinilisse praktikasse. RMJ 2006, 14. köide, nr 7, lk. 567-572
15. Berdnikova N.G. Asitromütsiini (Azitral) kasutamise tegelikud aspektid kogukonnas omandatud kopsupõletiku ravis täiskasvanutel. RMJ 2006, 14. köide, nr 22, lk. 1625-1628.
16. Hrjanin A.A., Reshetnikov O.V. Makroliidid klamüüdiainfektsiooni ravis rasedatel naistel (tõhusus, ohutus, tasuvus). RMJ 2008, 16. köide, nr 1, lk. 23-27.
17. Serov V.N., Dubnitskaja L.V., Tjutjunnik V.L. Põletikulised haigused vaagnaelundid: diagnostilised kriteeriumid ja ravi põhimõtted. RMJ 2011, 19. köide, nr 1, lk. 46-50.
18. Talašova S.V. Mõned aspektid antibakteriaalsete ravimite kasutamisest pediaatrias makroliidide näitel. RMJ 2009, 17. köide, nr 7, lk. 464-466
19. Mazankova L.N., Iljina N.O. Asaliidide koht pediaatrilises praktikas. RMJ 2008, 16. köide, nr 3, lk. 121-125.
20. Solovjov A.M., Pozdnjakov O.L., Tereštšenko A.V. Miks peetakse asitromütsiini urogenitaalse klamüüdiainfektsiooni ravis valitud ravimiks. RMJ 2006, 14. köide, nr 15, lk. 1160-1164.
21. Gurov A.V., Izotova G.N., Juškina M.A. Ravimi Azitrali kasutamise võimalused ülemiste hingamisteede mäda-põletikuliste haiguste ravis. RMJ 2011, 19. köide, nr 6, lk. 405.
22. Klani R. Asitromütsiini ja tsefaleksiini topeltpime topeltnäiv võrdlus naha ja nahastruktuuri infektsioonide ravis. Eur.J. Clin. mikrobiol. Infect.Dis. 1999 okt. 10 (10) – lk 880-84
Antibiootikumide kasutamine nahahaiguste korral on sageli inimesele ainus ravi. Antibakteriaalsed ained on tuntust kogunud kõrvalmõjude rohkuse tõttu, mis on sageli patoloogiliste protsesside ja uute haiguste esilekerkimise põhjuseks. Siiski ei ole võimalik nende ravimite kasutamisest keelduda.
Rakendus erinevate haiguste korral
Kõik haigused jagunevad 2 suurde rühma - nakkuslikud ja mittenakkuslikud. See jaotus on mõnevõrra meelevaldne, kuna on patoloogiaid, mille areng võib olla sekundaarse nakkusliku iseloomuga.
Reeglina kasutatakse antibakteriaalseid ravimeid järgmiste haiguste vastu võitlemiseks:
- vastsündinute pemfigus;
- erysipelas;
- krooniline atroofiline akrodermatiit;
- lümfotsütoom;
- herpetiformne impetiigo;
- erütematoosluupus ägedas ja alaägedas staadiumis;
- sklerodermia, nii hajus kui ka piiratud;
- lichen planus;
- ekseem;
- furunkuloos;
- nakatunud vigastused.
Narkootikumid dermatoloogias
Tänapäeval kasutatakse nahahaiguste raviks erinevate rühmade antibiootikume. Algselt kasutati püodermahaiguste vastu võitlemiseks antibakteriaalseid ravimeid. Hiljem on nende rakendusala selles valdkonnas märkimisväärselt laienenud. Sellel olid segased tagajärjed. Ühest küljest on suurenenud nende inimeste hulk, kellel õnnestus ebameeldivatest vaevustest vabaneda. Teisest küljest nad ilmusid resistentsed tüved patogeenid, suurenenud kõrvaltoimed ja allergilised reaktsioonid.
Nahahaiguste vastu võitlemisel on praegu tavaks kasutada järgmisi antibiootikumide rühmi:
- 1. Penitsilliin. Need ravimid on kõige traditsioonilisemad ja populaarsemad vahendid vabanemiseks nahahaigused nakkuslikku päritolu. Sest nad ei ole vastupidavad maomahl, saab neid kasutada ainult intramuskulaarse süstina.
- 2. Levinuim ravim on Bensüülpenitsilliini kaalium või naatriumsool. Seda manustatakse 250 000–500 000 RÜ sagedusega 1 kord iga 3–4 tunni järel või 300 000–500 000 RÜ regulaarsusega 2 korda päevas.
- 3. Nii ühekordsed kui päevane annus Bensüülpenitsilliin määratakse sõltuvalt vanusekategooria, kehaehitus, patsiendi kaal, raja iseärasused patoloogiline protsess, samuti ravimi eeldatavat efektiivsust antud konkreetsel juhul. Lisaks bensüülpenitsilliinile kasutatakse Novocini, mis on bensüülpenitsilliini novokaiini soola suspensioon isotoonilises naatriumkloriidi lahuses. Seda antibiootikumi kasutatakse ka intramuskulaarselt 300 000 RÜ sagedusega 3-4 korda päevas. On veel 3 vormi penitsilliini antibiootikumid- Foksümetüleenitsilliin ja bitsilliin. Nahahaiguste ravis neid aga laialdaselt ei kasutata.
- 4. Poolsünteetiliste penitsilliinide rühm. Kõige sagedamini kasutatakse neid ravimeid stafülokokkide ja streptokokkide põhjustatud nakkuslike dermatooside raviks. Lisaks kasutatakse neid antibiootikume keeruliste mitteinfektsioossete dermatooside korral. Selle penitsilliini ainete rühma väärtus seisneb selles, et nende toime on sarnane bensüülpenitsilliini omaga, kuid see suurendab nende efektiivsust nende mikroorganismide tüvede vastu, mis on resistentsed loodusliku penitsilliini suhtes.
- 5. Oksatsilliin. Seda ravimit ei hävitata agressiivses keskkonnas seedeelundkond, seega saab seda kasutada nii intramuskulaarselt kui ka suukaudseks manustamiseks mõeldud tablettidena. Sel põhjusel manustatakse oksatsilliini sageli ühe tabletina 1 tund enne sööki või 2-3 tundi pärast sööki. Täiskasvanu annus on 0,25-0,5 g, manustamisrütm on iga 4-5 tunni järel. Kursuse kestus - ühest nädalast kuni 20 päevani. Kursuse kestus sõltub paljudest teguritest ja jääb vahemikku 7 kuni 20 päeva.
- 6. Ampitsilliin. Seda peetakse väga laia toimespektriga ravimiks. Seedesüsteemi toime suhtes resistentsuse astme järgi sarnaneb see oksatsilliiniga. Soovitatav on juua seda annuses 0,5 g 4–6 korda päevas, olenemata toidu tarbimisest.
- 7. Ampiox. See preparaat sisaldab ampitsilliini ja oksatsilliini vahekorras 2:1. Ampioxi erilist efektiivsust täheldati, kui seda kasutati stafülokoki päritolu dermatoosi vastu.
Kõrvaltoimed ja vastunäidustused
Mida tugevam on mõju ravimtoode seda rohkem kõrvalmõjusid. Seda reeglit illustreerivad hästi ettevalmistused penitsilliini rühm.
Kõige sagedamini kui kõrvalmõju ilmuvad erinevaid valikuid allergiad. Inimene võib kogeda lämbumist, köha, nohu, pisaravoolu, kuid ilmingute sageduses on esikohal allergilised nahalööbed. Need sisaldavad:
- naha punetus;
- nõgestõbi;
- lööve, mis on iseloomulik nakkushaigustele nagu leetrid, sarlakid, punetised.
Kui penitsilliini rühma ravimeid kasutatakse naha väliseks kokkupuuteks, võib tekkida allergilise päritoluga kontaktdermatiit.
Penitsilliini rühma antibiootikumide kasutamisega seotud lööbe korral on vaja need ravimid täielikult loobuda, välja kirjutada antihistamiinikumid, kaltsiumkloriid, kortikosteroidid.

Kui penitsilliini kasutuselevõtt on raske allergiline reaktsioon, kasutage spetsiaalset ensüümi - penitsillinaasi. See aine hävitab kiiresti ja tõhusalt penitsilliini, mis eemaldab ka selle kõrvalmõju.
Antibiootikumide pikaajaline kasutamine põhjustab düsbakterioosi ja selle tulemusena beriberi. Selle toime vähendamiseks ja keha tugevdamiseks määratakse tavaliselt vitamiiniteraapia tõhustatud kuur.
Ja mõned saladused...
Kas teil on kunagi olnud probleeme Dermatiit või puudus? Otsustades selle järgi, et loete seda artiklit, on teil palju kogemusi. Ja muidugi teate kohe, mis see on:
- kriimustus tüütus
- ärgates hommikul järjekordse sügeleva naastuga uues kohas
- püsiv talumatu sügelus
- ranged toitumispiirangud
- põletikuline, konarlik nahk, laigud....
Nüüd vastake küsimusele: kas olete sellega rahul? Kas on võimalik taluda? Ja kui palju raha olete juba ebaefektiivse ravi eest "lekkinud"? Täpselt nii – on aeg neile lõpp teha! Kas sa nõustud? Seetõttu otsustasime avaldada intervjuu Elena Malõševaga, milles ta paljastab üksikasjalikult saladuse, kust need probleemid tulevad ja kuidas neid lahendada. Loe artiklit...
Dotsenko N.Ya., meditsiiniteaduste kandidaat, professor
ICMT olemuse kindlakstegemine läbiviimisega bakterioloogiline kultuur kohustuslik rasketel juhtudel, nagu mitmed keemised ja karbunklid, paise asukoht näol, sekundaarsed ja nekrotiseerivad infektsioonid. SIMT-i ravi sisaldab kolme põhikomponenti - lokaalne ravi, kirurgiline sekkumine ja antibiootikumravi.
Primaarne püoderma
tselluliit - äge põletik nahk ja/või nahaalune kude nende tihenemine, hüperemia, tursed ilma raku nekroosi või mädanemiseta, millega sageli kaasneb lümfangiit ja piirkondlik lümfadenopaatia. Furunkel - äge perifokaalne põletik juuksefolliikul, esineb sagedamini näol, kaelal, rinnal ja tuharatel. Kordumist raskendab furunkuloosi areng.
Enne paisu mädast sulamist on soovitatav puhata, antiseptilised sidemed (ihtiool ei ole näidustatud - soodustab infiltraadi abstsessi teket). Kui aga protsess on lokaliseeritud, näiteks nina eelõhtul, asetatakse ninna 10% süntomütsiini emulsioon. Keemise pindmise asukohaga saate eemaldada nekrootiline varras. Näo furunkel ähvardab meningeaalsete tüsistustega, seega on kõik manipulatsioonid selles piirkonnas piiratud. Sellise keemise lokaliseerimisega on kõne ja närimine piiratud. Süsteemne antibiootikumravi on näidustatud ainult keemise asukoha korral näol. Karbunkel - paise konglomeraat, mis moodustub infektsiooni subkutaanse leviku tagajärjel koos naha sügavate kihtide mädase-nekrootilise põletiku tekkega, sageli koos nekrootiliste masside tagasilükkamisega. Karbunkuli ravi on tavaliselt kirurgiline. Kui põletik progresseerub hoolimata piisavast sisselõikest, on näidustatud antibiootikumravi.
Hüdradeniit (" emase udara”) - lokaalne valulik apokriinsete näärmete põletik, tavaliselt lokaliseeritud kaenlaaluses või kubemes.
Ravi infiltratsiooni staadiumis on konservatiivne (puhkus, kahjustuse pesemine on välistatud, antibiootikumravi, ultraviolettkiirgus, naha ravi alkoholi või antiseptikumidega), fluktuatsiooni ilmnemisega – abstsessi avanemine. Seega viiakse süsteemne antibiootikumravi läbi keetmise lokaliseerimisega näol (ja kaelal) koos hüdradeniidiga. Karbunkuli puhul on esmatähtis kirurgiline sekkumine. Kergetel juhtudel on ette nähtud fenoksümetüülpenitsilliin, amoksitsilliin või makroliidid. Stafülokoki tselluliidi korral määratakse kergetel juhtudel suukaudselt tsefaleksiin, amoksitsilliin / klavulanaat, rasketel juhtudel teise põlvkonna tsefalosporiine (tsefamandool, tsefuroksiim), mille kliiniline efektiivsus on tõestatud. Korduvate keetmise korral viiakse läbi pidev antibiootikumravi 1-2 kuud. (bitsilliin või makroliidid 1 nädala jooksul iga kuu).
Viimasel ajal on metitsilliiniresistentsete S. aureus'e (MRSA) tüvede arv suurenenud. Hoolimata selliste juhtumite harvaesinemisest ambulatoorsete patsientide seas (1%), võib ICMT kõrge levimuse ja nende edasise suurenemise tõttu tekkida probleeme raviga, kuna MRSA-vastaste ravimite arsenal piirdub kotrimoksasooliga (trimetoprim / sulfametoksasool). , tetratsükliinid ja oksasolidinoonide rühma kuuluv ravim (linesoliid). On näidatud, et S.aureus'e tüved, mis on eraldatud pindmiste STI-dega hospitaliseeritud patsientidelt, on väga resistentsed tetratsükliini, gentamütsiini, tsiprofloksatsiini, klindamütsiini, klooramfenikooli, erütromütsiini suhtes, säilitades samas tundlikkuse fusidiinhappe ja mupirotsiini suhtes.
Sekundaarne ICMT, mis tekkis kaasuvate haiguste taustal
Lamatised - isheemiline nekroos ja kudede haavandumine luu eendi kohal, mis on pikka aega olnud pideva välissurve all. Kui patoloogilises materjalis on kooki floora, määratakse antibiootikumid, nagu streptokoki või stafülokoki tselluliidi korral. Gramnegatiivse infektsiooni või sepsise korral kasutatakse amoksitsilliini/klavulanaati, imipeneemi/tsilastatiini ja IV põlvkonna tsefalosporiini tsefepiimi.
Diabeetilise jala sündroom (DFS) on diabeetilise neuropaatia, mikro- ja makroangiopaatia, osteoartropaatia põhjustatud anatoomiliste ja funktsionaalsete muutuste kompleks, mis viib jala pehmete kudede nakatumiseni koos mädase-põletikulise protsessi tekkega, mis lõpuks lõpeb jäseme amputatsioon. Mõjutatud piirkondadest külvatakse sageli aeroobset taimestikku, sageli polümikroobset.
Nakatunud ja nakatumata jalahaavandeid on raske eristada, sest isegi sügava infektsiooni korral ei esine enamikul patsientidest palavikku, leukotsütoosi ja ESR-i suurenemist. Ühelt poolt ei välista nende märkide puudumine nakatumise võimalust, teisalt viitab nende olemasolu haavandi juuresolekul alati märkimisväärsele kahjustusele.
SDS-i ravi põhimõtted: ainevahetuse kontroll, hügieen, haava puhastamine mitteelujõulistest kudedest, hüperkeratoos, jala mahalaadimine, kohalik ravi, antibiootikumravi. Kergete infektsioonide korral suukaudne manustamine amoksitsilliin, klindamütsiin, tsefuroksiim või tsefaleksiin. Raskematel juhtudel kasutatakse intravenoosset imipeneemi / tsilastatiini, ampitsilliini / sulbaktaami, klindamütsiini või III-IV põlvkonna fluorokinoloone (levofloksatsiini, moksifloksatsiini).
Kui moodustub abstsess, kirurgiline sekkumine. Raskeid infektsioone iseloomustab massiivne tselluliit, lümfadeniit koos septilise seisundi tekkega. Valitud antibiootikumid - imipeneem / tsilastatiin, efektiivne ampitsilliin / sulbaktaam kombinatsioonis aminoglükosiididega, III-IV põlvkonna tsefalosporiinid.
2002. aastal tehti süstemaatiline ülevaade 25 randomiseeritud kontrollitud uuringust, milles hinnati paiksete ja süsteemne ravi troofilised haavandid alajäsemed, lamatised ja diabeetiline jalg. Allopurinooli ja dimetüülsulfoksiidi kasutamine, sidemed alates aktiveeritud süsinik hõbedaga, vaske sisaldav tripeptiid ja hõbesulfadiasiin suurendas alajäsemete troofiliste haavandite paranemise tõenäosust võrreldes platseebo ja teiste paiksete preparaatidega. Oksükinoloonsalvi määrimine aitas kaasa lamatiste paranemisele. Autorid jõudsid järeldusele, et kohalik rakendus mõned antibakteriaalsed ained soodustavad krooniliste paranemist haavandilised kahjustused nahka. Nad soovitavad süsteemse infektsiooni nähtude korral ravi süsteemsete antibiootikumidega. Erysipelas(RV), erysipelas - nakkushaigus põhjustatud b-hemolüütilisest streptokokist (rasketel juhtudel - polümikroobsed ühendused). Iseloomulik on naha, limaskestade fokaalne seroosne või seroos-hemorraagiline põletik, palavik, mürgistus.
Lokaalsete ilmingute olemuse järgi eristatakse erütematoosset, erütematoosset-bulloost, erütematoosset-hemorraagilist ja bulloosset-hemorraagilist vormi; vastavalt kulgemise paljususele - esmane, korduv, korduv; vastavalt kohalike ilmingute levimusele - lokaliseeritud, laialt levinud, ekslemine, metastaatiline; vastavalt kursuse raskusastmele - kerge, mõõdukas ja raske.
Raske RV koos mürgistuse või laialt levinud nahakahjustustega (eriti bulloos-hemorraagilise vormiga) ja sagedased retsidiivid olenemata joobeastmest ja lokaalse protsessi iseloomust, samuti raskete kaasuvate haiguste, lapsepõlve ja vanaduse korral on vajalik haiglaravi. Jäsemetel lokaliseeruvate bulloossete vormide puhul on soovitatav RV lokaalne ravi. Terved villid lõigatakse sisse, pärast eksudaadi vabanemist kantakse neile mitu korda päevas sidemed 0,1% rivanooli või 0,02% furatsiliiniga. Tihe sidumine on vastuvõetamatu.
Antibiootikumide kohalik kasutamine RV-s ei ole soovitatav, kuna selle kasutusviisiga ei hävita nad mikrofloorat, vaid muudavad selle koostist.
RV süsteemne antibiootikumravi on kohustuslik ja seda tehakse ambulatoorselt uute makroliidide või tsefaklooriga 7-10 päeva jooksul. Võib-olla doksütsükliini kasutamine talumatusega - furazolidoon. Haiglas kasutatakse bensüülpenitsilliini, tsefasoliini või linkomütsiini 7-10 päeva. Rasketel juhtudel on ette nähtud abstsessi, flegmoni, tsefalosporiinide teke II-III põlvkond kaitstud penitsilliinid, sealhulgas kombinatsioonis teise põlvkonna fluorokinoloonidega (tsiprofloksatsiin, ofloksatsiin) või monoteraapia III-IV põlvkonna fluorokinoloonidega. Korduva RV ravi viiakse läbi kaitstud penitsilliinide, III-IV põlvkonna fluorokinoloonidega.
Bitsilliini profülaktika (bensatiini bensüülpenitsilliin 2,4 miljonit ühikut) takistab streptokoki L-vormide muutumist bakteriaalseteks vormideks. Kolme või enama ägenemise korral aastas viiakse bitsilliini profülaktika läbi aastaringselt 2-3 aastat 3-4-nädalase intervalliga. (esimestel kuudel on vaheaeg 2 nädalat). Hooajaliste ägenemiste korral alustatakse antibiootikumravi kuu aega enne haigestumuse hooaja algust 3-4-nädalase intervalliga. kuni 3-4 kuud aastas.
Nekrotiseeriv ICMT
Iseärasused:
Surm - kuni 50%;
Reeglina polümikroobne etioloogia koos toksiinide tootmisega, mis pärsivad makroorganismi immuunsust;
Infektsiooni lokaliseerimine tüüpilistel juhtudel - perineum ja alajäsemed;
Kudede kiire levik (sh subfastsiaalne) ja sageli mädane lagunemine koos gaaside moodustumisega, mädase eksudaadi puudumine;
Nakkuse tegelik leviku määr määratakse alles kirurgilise ravi käigus.
Nekrotiseeriva ICMT tüüpiline esindaja on nekrotiseeriv fastsiit, mis on põhjustatud toksiine tootvast rühma A streptokokist, mis väljendub septilise šoki, DIC, pehmete kudede nekroosi ja lööbega. Teisest küljest tekib ligikaudu 1/2 streptokoki toksilise šoki sündroomiga patsientidest nekrotiseeriv fastsiit, mis eristab seda teistest infektsioonidest, eriti stafülokoki toksilise šoki sündroomist. Nekrotiseeriva ICMT ravis on prioriteediks varajane kirurgiline sekkumine – elujõuliste kudede eemaldamine. soodne keskkond patogeeni paljundamiseks. Valitud antibiootikumid: inhibiitoritega kaitstud antipseudomonaalsed penitsilliinid (piperatsilliin/tasobaktaam, tikartsilliin/klavulanaat) ja karbapeneemid. Soovitav on lisada klindamütsiini antibakteriaalsesse ravirežiimi, võttes aluseks selle teoreetiliselt tõestatud võime pärssida A-rühma streptokokkide poolt toodetud toksiinide sünteesi.
Seega koosneb ICMT ravi kirurgilisest sekkumisest, lokaalsest ravist ja antibiootikumravist. ECMT patogeenide koostise ja tundlikkuse muutumise tõttu antimikroobne ravi tuleks läbi viia, võttes arvesse nende seiret. ICMT süsteemsete antibiootikumide määramise näidustused on kliiniliselt väljendunud üldise põletikulise reaktsiooni olemasolu või protsessi ohtlik lokaliseerimine. Antibiootikumide valikul lähtutakse nende mõistliku kasutamise põhimõtetest: kergetel juhtudel - b-laktaamid, makroliidid suu kaudu, infektsiooniga mõõdukas- kaitstud penitsilliinid, tsefalosporiinid II-III põlvkond, fluorokinoloonid, eluohtlike infektsioonide korral - karbapeneemid, tsefalosporiinid või fluorokinoloonid III-IV põlvkond.
Kirjandus
1. Bereznjakov I.G. Antibiootikumide mõistliku kasutamise põhimõtted. Clinical Antibiotic Therapy, nr 1 (2004).
2. Tutchenko M.I., Ignatovsky Yu.V., Schastniy V.M. Beshikhovi põletiku medikamentoosne ravi raske kaasuva patoloogiaga vaevuste korral. Clinical Antibiotic Therapy, nr 4 (2002).
3. Toimik T. Naha ja pehmete kudede infektsioonide diagnoosimine ja antimikroobne ravi. Clinical Microbiology and Antimicrobial Chemotherapy, nr 2 (2003).
4. Shapiro A.V. Antibiootikumid ja nende kasutamine mäda-põletikuliste haiguste korral. Likuvannya ta diagnostika, nr 1 (1999).
5. Leibovici L. Ülevaade: mõne aktuaalne rakendamine antimikroobsed ained soodustab krooniliste haavandiliste nahakahjustuste paranemist. Rahvusvaheline ajakiri meditsiinipraktika, №3 (2002).